Содержание
- 2. Жоспары І. Кіріспе ІІ. Негізгі бөлім ІІІ. Қорытынды IV. Қолданылған әдебиеттер тізімі
- 3. В соответствии с утвержденным порядком проведения экспертизы лекарственных средств, изделий медицинского назначения и медицинской техники прием
- 4. Первичная экспертиза лекарственных средств, изделий медицинского назначения и медицинской техники проводится в Департаменте первичной экспертизы лекарственных
- 5. Обязательные поля для записи на прием*: Наименование заявителя Наименование лекарственного средства, изделия медицинского назначения и медицинской
- 6. *В случае если заявитель по каким-либо причинам не может осуществить сдачу регистрационного досье, образцов и СО,
- 7. До подачи заявления на экспертизу заявитель по желанию получает в государственной экспертной организации научную и предрегистрационную
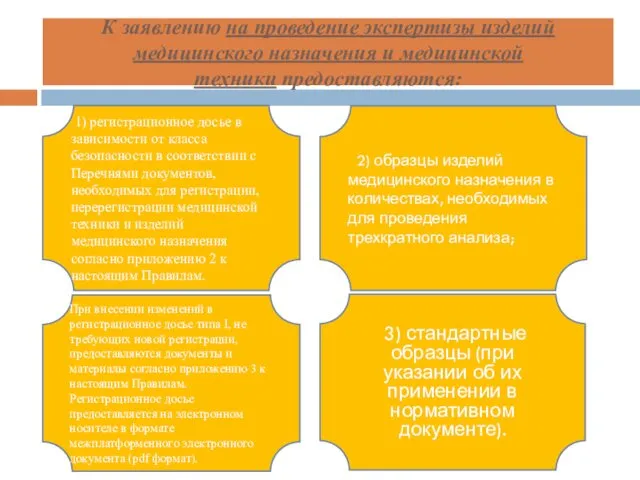
- 8. К заявлению на проведение экспертизы изделий медицинского назначения и медицинской техники предоставляются: 1) регистрационное досье в
- 9. Специалист ДПЭЛС, ИМН и МТ в «ОДНОМ ОКНЕ» осуществляет:
- 10. Не принимаются: иммунобиологические медицинские препараты и их стандарты наркотические препараты, прекурсоры и их стандарты препараты, требующие
- 11. Заявление не будет принято в случаях: отсутствия материалов и документов ЭРД согласно установленным требованиям; несоответствия формата
- 12. После приема ЭРД, электронного регистрационного досье, образцов, стандартных образцов, специфических реагентов, расходных материалов специалист ДПЭЛС, ИМН
- 13. Документы Модуля 1 (кроме пунктов 1.4, 1.5, 1.6) формата ОТД, Модуля 3 формата ОТД: спецификации (3.2.P.5.1.),
- 14. Регистрационное досье в формате ОТД составляется: организациями-производителями дальнего зарубежья; организациями-производителями стран СНГ - через два года
- 15. Каждый модуль на электронном носителе должен быть представлен отдельным файлом (папкой) с ссылочными закладками на разделы
- 16. На экспертизу при перерегистрации лекарственного средства предоставляются Модули 1-3 формата ОТД или части 1 - 2
- 17. Материалы Модулей 4 и 5 формата ОТД и частей 3 и 4 Списка должны соответствовать требованиям
- 18. Документы группируются строго по перечню с нумерацией страниц. Экспертиза проводится после оплаты полной стоимости за экспертизу
- 19. Первичная экспертиза документов и материалов проводится в течение 35 дней при регистрации ЛС, 20 дней при
- 20. После окончания первичной экспертизы формируется письмо заявителю с результатами первичной экспертизы и приложением дополнительных материалов (НД,
- 21. Первичная экспертиза регистрационного досье лекарственного средства включает в себя: 1) оценку полноты, достоверности и правильности оформления
- 22. 4) экспертизу названия на предмет отсутствия в нем: графических сходств с ранее зарегистрированными лекарственными препаратами и
- 23. 5) экспертизу на наличие в государственном реестре идентичного названия лекарственного средства с другим составом активных веществ;
- 24. Первичная экспертиза изделия медицинского назначения и медицинской техники включает в себя: 1) проверку предоставленных документов регистрационного
- 25. Заключение о безопасности, эффективности и качестве ЛС, ИМН и МТ На этапе формирования заключения по безопасности,
- 26. По результатам первичной, аналитической и специализированной экспертизы изделий медицинского назначения и медицинской техники составляет заключение о
- 27. Государственная экспертная организация направляет в электронном виде в государственный орган: заключение о безопасности, эффективности и качестве
- 28. инструкцию по медицинскому применению лекарственного средства, изделия медицинского назначения, согласованную с экспертной организацией на государственном и
- 29. Пайдаланылға әдебиеттер http://www.dari.kz/pages/1181
- 31. Скачать презентацию

























 Построение календарного плана производства монтажных работ
Построение календарного плана производства монтажных работ Технологии современного производства
Технологии современного производства Я - учитель.
Я - учитель. презентация к уроку В мире математики, 6 класс
презентация к уроку В мире математики, 6 класс Биоокисление. Метаболизм углеводов. Тема 6
Биоокисление. Метаболизм углеводов. Тема 6 Изменения в трудовом законодательстве
Изменения в трудовом законодательстве Письмо букв Диск
Письмо букв Диск Поворот и центральная симметрия
Поворот и центральная симметрия Пермская и Кунгурская епархия РПЦ Добрянское благочиние. Храм св.апостола Иоанна Богослова
Пермская и Кунгурская епархия РПЦ Добрянское благочиние. Храм св.апостола Иоанна Богослова Методология и методика диссертационного исследования
Методология и методика диссертационного исследования Звонкие парные согласные на конце и в середине слова
Звонкие парные согласные на конце и в середине слова Правила поведения в школе для первоклассников
Правила поведения в школе для первоклассников Работа в графическом редакторе PAINT. Закрепление полученных ранее знаний
Работа в графическом редакторе PAINT. Закрепление полученных ранее знаний Контрейлерные перевозки: состояние и перспективы развития
Контрейлерные перевозки: состояние и перспективы развития Техника безопасности на занятиях гимнастикой. Основные группы мышц и способы их развития
Техника безопасности на занятиях гимнастикой. Основные группы мышц и способы их развития Дизартрия дегеніміз
Дизартрия дегеніміз картотека загадок по лексической теме Домашние птицы
картотека загадок по лексической теме Домашние птицы Христианские праздники и традиции их празднования на Руси
Христианские праздники и традиции их празднования на Руси Гиперреализм. Фотореализм
Гиперреализм. Фотореализм Дидактические игры для формирования слоговой структуры слова.
Дидактические игры для формирования слоговой структуры слова. Пасха
Пасха Аллергия. Аллергены
Аллергия. Аллергены Проект строительства эксплуатационной скважины глубиной 3000 м на Мамонтовском нефтяном месторождении
Проект строительства эксплуатационной скважины глубиной 3000 м на Мамонтовском нефтяном месторождении Буквосочетания чк, чн, чт
Буквосочетания чк, чн, чт Порядок формирований спепендиального фонда на выплаты стипендий за счет средств федерального бюджета
Порядок формирований спепендиального фонда на выплаты стипендий за счет средств федерального бюджета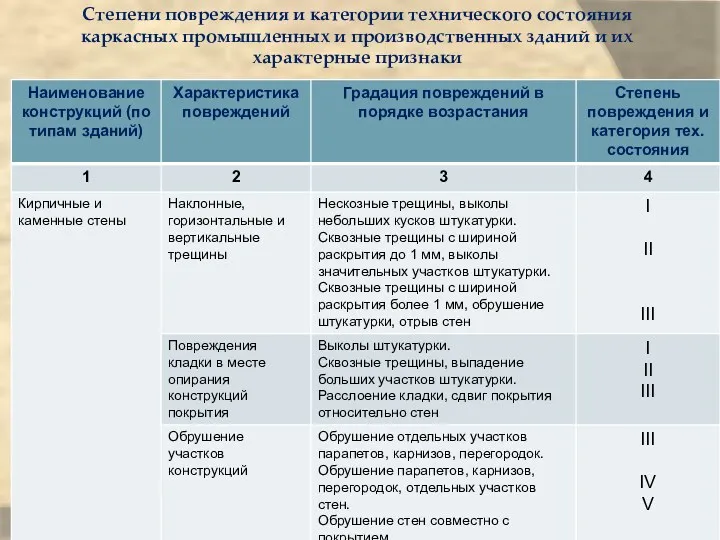 Степени повреждения и категории технического состояния промышленных и производственных зданий и их характерные признаки
Степени повреждения и категории технического состояния промышленных и производственных зданий и их характерные признаки Презентация Английский для детей
Презентация Английский для детей ООП (+ постановка задачи)
ООП (+ постановка задачи)