Содержание
- 2. Открытие электрона.
- 3. Опыты Фарадея Майкл Фарадей (22.09.1791 – 25.08.1867) – английский физик-экспериментатор и химик В 1833 - 34
- 4. Опыты Крукса Уильям Крукс (17.06.1832 – 4.04.1919) – английский химик и физик Исследовал электрическую проводимость в
- 5. Опыты Стони Джордж Джонстон Стони (15.02.1826 – 5.07.1911) – британский ирландский физик и математик. В 1874
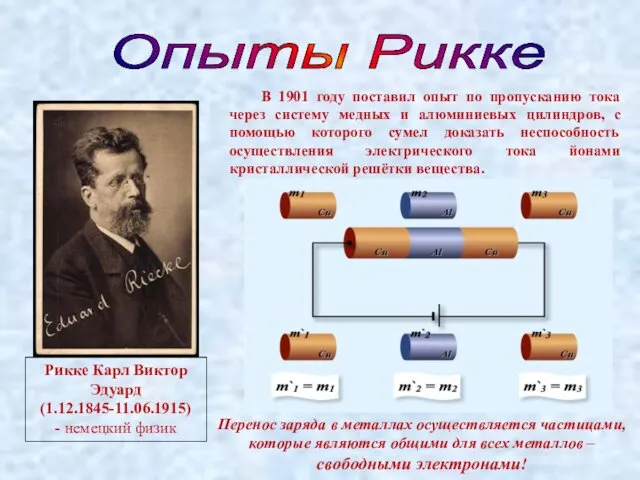
- 6. Опыты Рикке Рикке Карл Виктор Эдуард (1.12.1845-11.06.1915) - немецкий физик В 1901 году поставил опыт по
- 7. Опыты Томсона Джозеф Джон Томсон (18.12.1856-30.08.1940) - английский физик, лауреат Нобелевской премии по физике В 1897
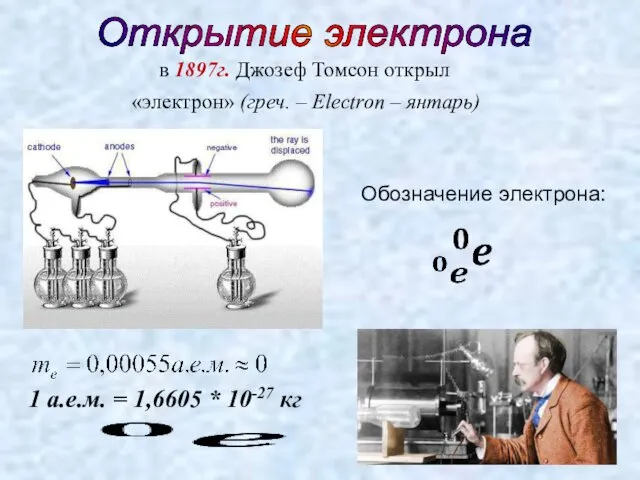
- 8. Открытие электрона в 1897г. Джозеф Томсон открыл «электрон» (греч. – Electron – янтарь) Обозначение электрона: 1
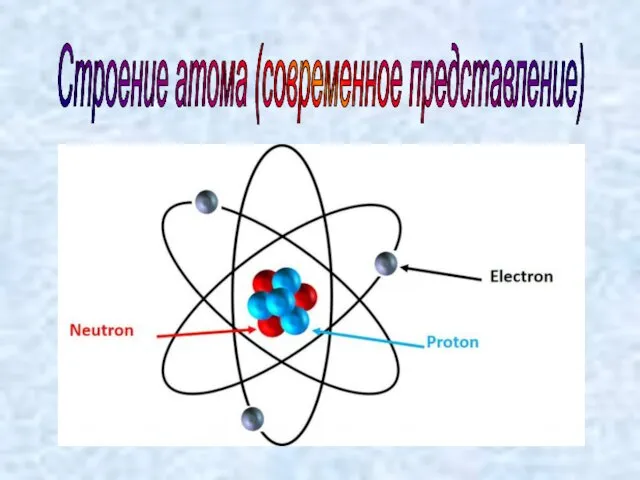
- 9. В центре атома расположено положительно заряженное ядро, в котором сконцентрирована почти вся масса атома. Вокруг ядра
- 10. Открытие протона и нейтрона.
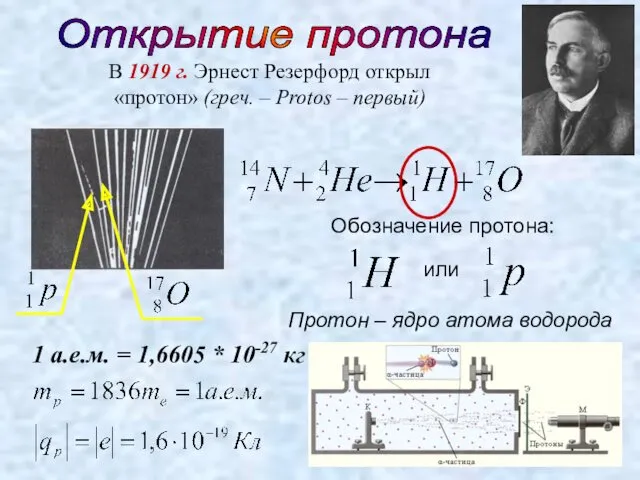
- 11. Открытие протона В 1919 г. Эрнест Резерфорд открыл «протон» (греч. – Protos – первый) Обозначение протона:
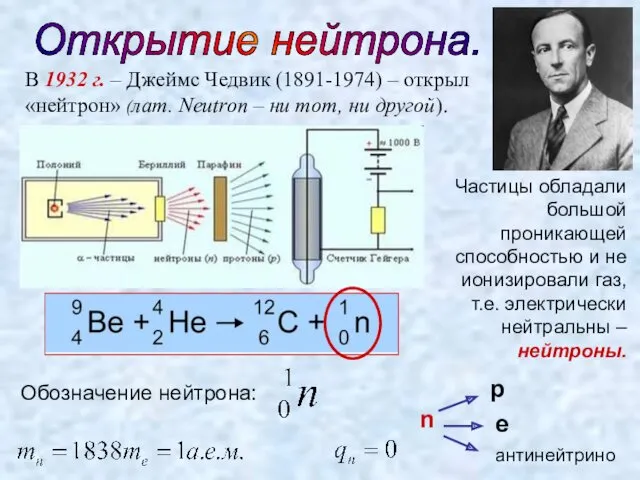
- 12. Открытие нейтрона. Частицы обладали большой проникающей способностью и не ионизировали газ, т.е. электрически нейтральны – нейтроны.
- 13. В 1932 году советский физик Д. Д. Иваненко и немецкий физик В. К. Гейзенберг предложили протонно-нейтронную
- 14. Ядро + протон нейтрон Z – число протонов в ядре (зарядовое число) N – число нейтронов
- 15. Строение атома (современное представление)
- 16. Задача №1 Сколько нуклонов содержат ядра: Задача №2 Определите нуклоновый состав ядер: Задача №3 Назовите химический
- 18. Скачать презентацию










 Позиционирование ампайров и винг-ампайров в матчевых гонках (Umpires’ Positioning)
Позиционирование ампайров и винг-ампайров в матчевых гонках (Umpires’ Positioning) Основи побудови радіоелектронної техніки. Загальні відомості про РЛС 19Ж6. (Тема 10.1)
Основи побудови радіоелектронної техніки. Загальні відомості про РЛС 19Ж6. (Тема 10.1) Транспортная безопасность
Транспортная безопасность Великая отечественная война
Великая отечественная война Кузбасс: вчера. сегодня, завтра
Кузбасс: вчера. сегодня, завтра Паркувальний радар
Паркувальний радар Презентация Права ребёнка
Презентация Права ребёнка Балканские страны перед завоеванием
Балканские страны перед завоеванием Организационная перестройка по Дж. Коттеру
Организационная перестройка по Дж. Коттеру Становление Древнерусского государства и правление первых русских князей
Становление Древнерусского государства и правление первых русских князей Случаи вычитания 17 - 18 -
Случаи вычитания 17 - 18 - Работа для участия в НПК Начальные классы (2 класс) - 1 место на школьном этапе, 2 - на районном.
Работа для участия в НПК Начальные классы (2 класс) - 1 место на школьном этапе, 2 - на районном. Призентация к интерактивному уроку:Основные классы неорганических соединений 7класс
Призентация к интерактивному уроку:Основные классы неорганических соединений 7класс Презентация В память о Беслане
Презентация В память о Беслане Конструкция бесстыкового пути
Конструкция бесстыкового пути Василий Иванович Белов
Василий Иванович Белов Подарочные наборы iPapai
Подарочные наборы iPapai Башлангыч сыйныфта татар теленнән кагыйдәләр
Башлангыч сыйныфта татар теленнән кагыйдәләр Площадь криволинейной трапеции
Площадь криволинейной трапеции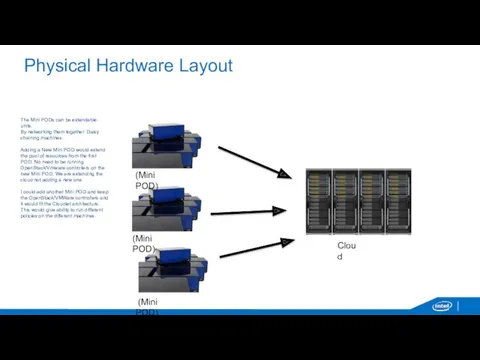 Physical Hardware Layout
Physical Hardware Layout Организация работы станции Кая (Электрификация 8 и 9 путей)
Организация работы станции Кая (Электрификация 8 и 9 путей) Природные уникумы Урала. Экологические проблемы Урала
Природные уникумы Урала. Экологические проблемы Урала Valentines day riddles
Valentines day riddles Буклет на звук Л
Буклет на звук Л История развития ГИС за рубежом и в нашей стране. Наиболее популярные современные ГИС. Их краткая характеристика
История развития ГИС за рубежом и в нашей стране. Наиболее популярные современные ГИС. Их краткая характеристика Ручной труд как средство развития мелкой моторики
Ручной труд как средство развития мелкой моторики Правовой стиль и правовые семьи по К. Цвайгерту и Х. Кётцу
Правовой стиль и правовые семьи по К. Цвайгерту и Х. Кётцу Биологическая роль липидов. Транспортные формы липидов
Биологическая роль липидов. Транспортные формы липидов