Содержание
- 2. Загадка: Есть такие металлы, которые в руки не возьмешь и ножа из них не сделаешь. О
- 3. 07.11.2020 Элементы IА-группы и их соединения
- 4. Что вам известно о щелочных металлах?
- 5. План урока Положение щелочных металлов в ПСХЭ. Физические свойства. Химические свойства. Соединения ЩМ. Применение. Биологическое значение
- 6. Положение в ПСХЭ Д.И. Менделеева Покажите, где находятся щелочные металлы в периодической системе. Составьте электронные конфигурации
- 7. Физические свойства ЩМ
- 8. Физические свойства ЩМ
- 9. Физические свойства ЩМ
- 10. Физические свойства ЩМ Твердые вещества с металлическим блеском на свежем срезе, быстро тускнеют вследствие окисления. Серебристо-белые
- 11. Хранение ЩМ Из-за высокой химической активности хранят под слоем керосина. Который защищает от контакта с воздушной
- 12. Химические свойства ЩМ I. С простыми веществами-неметаллами (ОВР): 1. C кислородом: Li + O2 → Na
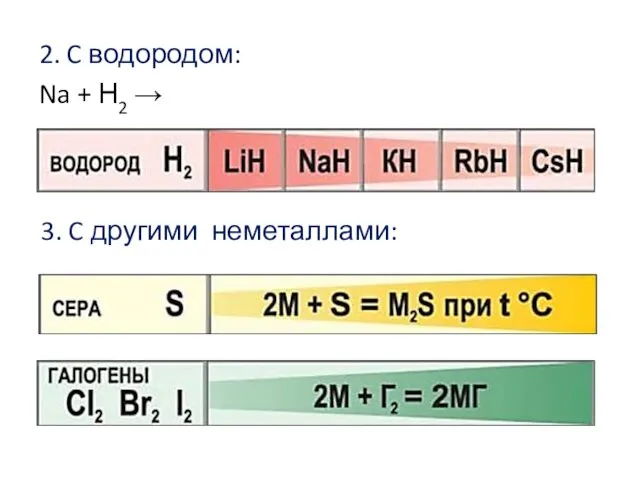
- 13. 2. C водородом: Na + Н2 → 3. C другими неметаллами:
- 14. II. Со сложными веществами (ОВР): 1. С водой: активно взаимодействуют, образуя гидроксид и водород: 2Me +
- 15. II. Со сложными веществами (ОВР): 2. С растворами кислот: Na + HCl →
- 16. Соединения ЩМ Гидроксиды ЩМ: МеОН Щелочи едкие, разъедают бумагу и ткани. Первая помощь: смыть водой, обработать
- 17. Соединения ЩМ Соли ЩМ: NaCl- хлорид натрия, поваренная соль Na2CO3 – карбонат натрия, кристаллическая сода NaHCO3
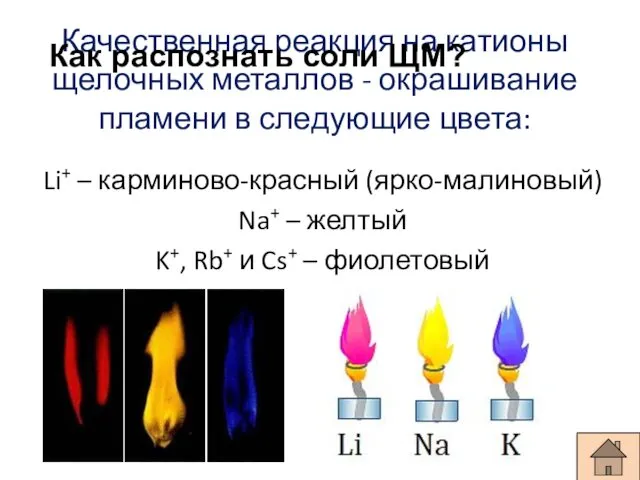
- 18. Качественная реакция на катионы щелочных металлов - окрашивание пламени в следующие цвета: Li+ – карминово-красный (ярко-малиновый)
- 19. Задание: вставьте пропущенные термины, допишите предложения 1. Щелочными металлами называются элементы I группы, … подгруппы. Это
- 20. В далекой стране Химляндии существует множество королевств: металлы, щелочи, неметаллы, кислоты и т.д. Королевством металлов правит
- 21. Щелочные металлы имеют свой собственный многоэтажный домик в таблице Менделеева. На каждом этаже живет свой металл:
- 22. Все щелочные металлы – братья, они очень похожи друг на друга: у всех есть металлический блеск,
- 23. Щелочные металлы очень нужны в королевстве людей… Закончите сказку, рассказав о применении и биологическом значении ЩМ.
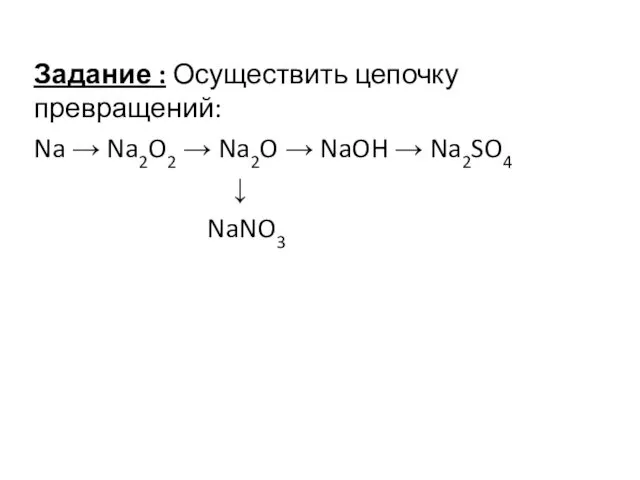
- 24. Задание : Осуществить цепочку превращений: Na → Na2O2 → Na2O → NaOH → Na2SO4 ↓ NaNO3
- 26. Скачать презентацию




















 Работа с программно-аппаратным комплексом УКЭБ производства компании Электронный вокзал
Работа с программно-аппаратным комплексом УКЭБ производства компании Электронный вокзал Питание и кормление пациентов
Питание и кормление пациентов Нелинейные электрические цепи
Нелинейные электрические цепи У Васюньки день народження
У Васюньки день народження Беспроводные локальные сети Wlan
Беспроводные локальные сети Wlan Нефть и её транспортировка
Нефть и её транспортировка Ettevõtete ühinemised ja ülevõtmised Tulemuslikkuse hindamise süsteemid
Ettevõtete ühinemised ja ülevõtmised Tulemuslikkuse hindamise süsteemid Проектная работа. Здоровье. Правильная осанка- залог здоровья
Проектная работа. Здоровье. Правильная осанка- залог здоровья Кроссворд по правилам дорожного движения
Кроссворд по правилам дорожного движения Исследовательская работа Участники ВОВ - наши земляки
Исследовательская работа Участники ВОВ - наши земляки звуковой анализ
звуковой анализ Объяснения сторон и третьих лиц
Объяснения сторон и третьих лиц Мастер - класс на тему:Развитие познавательных способностей у дошкольников через использование песочной терапии
Мастер - класс на тему:Развитие познавательных способностей у дошкольников через использование песочной терапии Лечебное питание при заболеваниях почек и мочевыводящих путей
Лечебное питание при заболеваниях почек и мочевыводящих путей Презентация к классному часу Всех на свете дороже доброта
Презентация к классному часу Всех на свете дороже доброта Достопримечательности города Дрезден
Достопримечательности города Дрезден Информационные технологии давно стали частью образовательного процесса, однако с появлением ЭОР открылась новая страница
Информационные технологии давно стали частью образовательного процесса, однако с появлением ЭОР открылась новая страница Общие сведения о металлах и сплавах
Общие сведения о металлах и сплавах История, которая вас удивит: что изучает историческая наука и как писать историю
История, которая вас удивит: что изучает историческая наука и как писать историю Презентация5
Презентация5 Воспалительные заболевания кишечника: неспецифический язвенный колит и болезнь Крона
Воспалительные заболевания кишечника: неспецифический язвенный колит и болезнь Крона Угрозы безопасности информации. Преднамеренные угрозы
Угрозы безопасности информации. Преднамеренные угрозы Дидактическая игра для детей 3-4 лет Найди две одинаковые машины
Дидактическая игра для детей 3-4 лет Найди две одинаковые машины Ликуй студент! Учись и здравствуй! Ко Дню Российского студенчества
Ликуй студент! Учись и здравствуй! Ко Дню Российского студенчества Конструирование одежды
Конструирование одежды Рынок банковских карт в России: проблемы и перспективы развития
Рынок банковских карт в России: проблемы и перспективы развития Архитектор Михаил Павлович Малахов (1781-1842)
Архитектор Михаил Павлович Малахов (1781-1842) Мероприятия по повышению эффективности деятельности компании и управлению затратами
Мероприятия по повышению эффективности деятельности компании и управлению затратами