Содержание
- 2. Общая характеристика органических соединений Органические соединения являются производными углерода; Углерод в органических соединениях образует четыре ковалентные
- 3. Для органических соединений характерна изомерия: имея одинаковый химический состав, молекулы могут обладать различным пространственным строением и
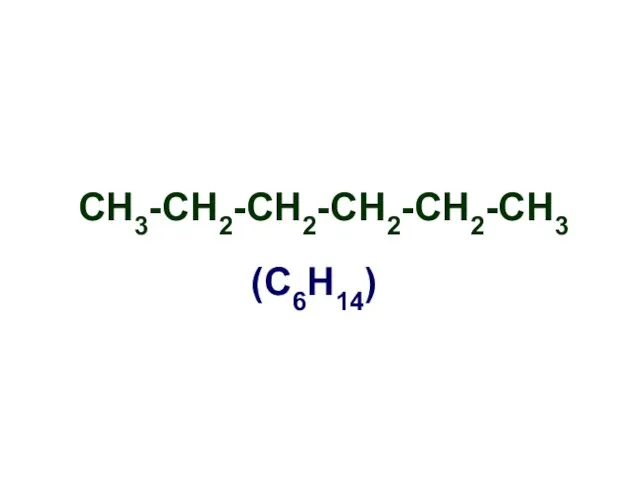
- 4. СН3-СН2-СН2-СН2-СН2-СН3 (С6Н14)
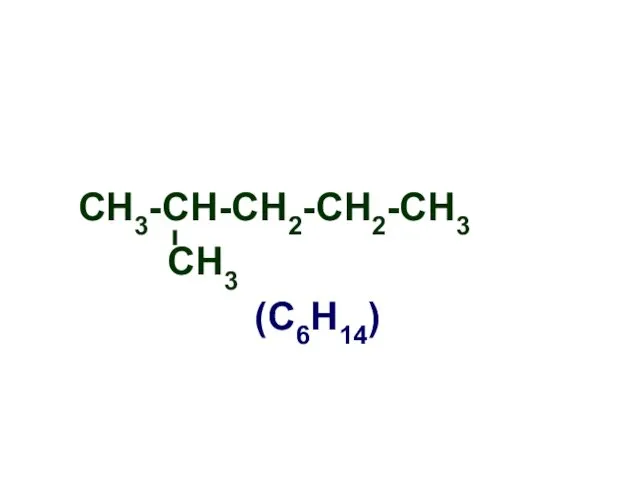
- 5. СН3-СН-СН2-СН2-СН3 СН3 (С6Н14)
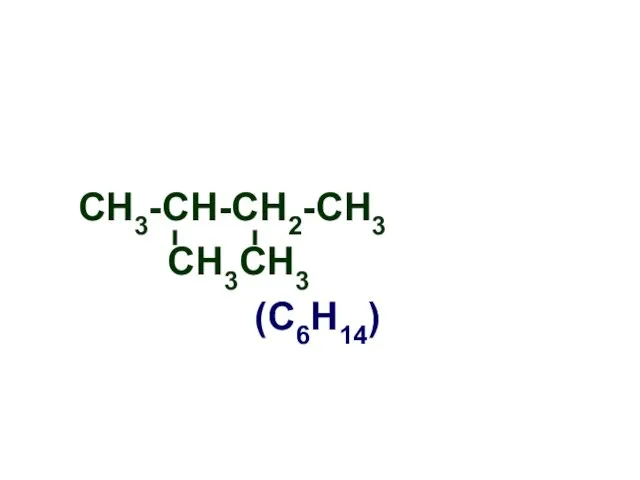
- 6. СН3-СН-СН2-СН3 СН3СН3 (С6Н14)
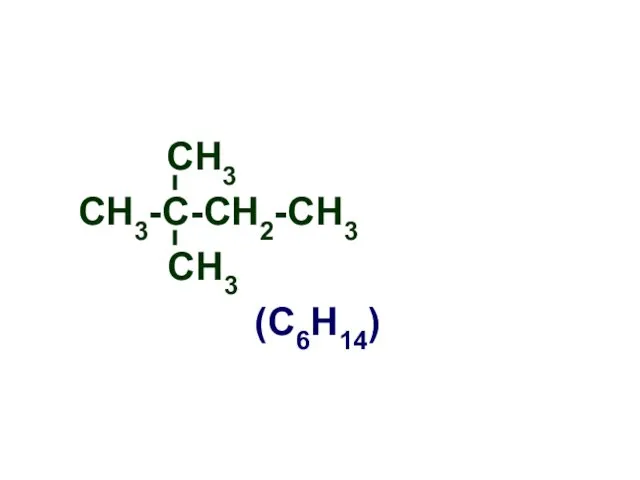
- 7. СН3-С-СН2-СН3 СН3 (С6Н14) СН3
- 8. Углеводороды В зависимости от наличия или отсутствия двойных и тройных связей углеводороды делятся на предельные или
- 9. Алканы Простейшим алканом является метан - СН4; Имея общую формулу - СnH2n+2, алканы образуют ряд соединений
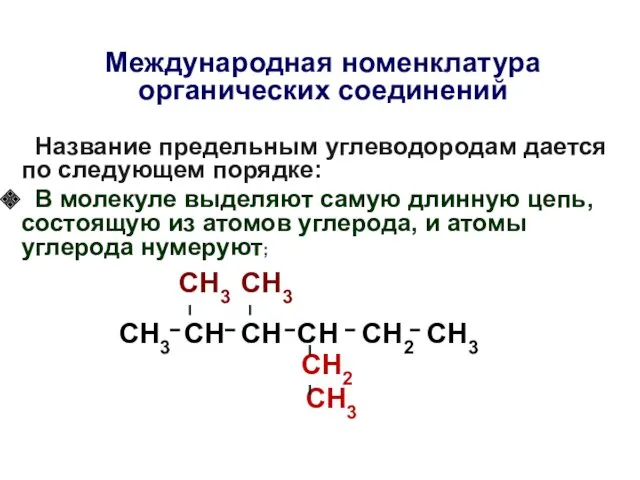
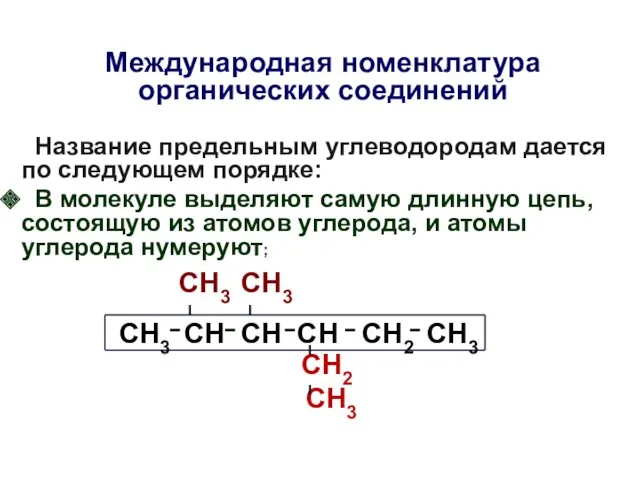
- 10. Международная номенклатура органических соединений Название предельным углеводородам дается по следующем порядке: В молекуле выделяют самую длинную
- 11. Международная номенклатура органических соединений Название предельным углеводородам дается по следующем порядке: В молекуле выделяют самую длинную
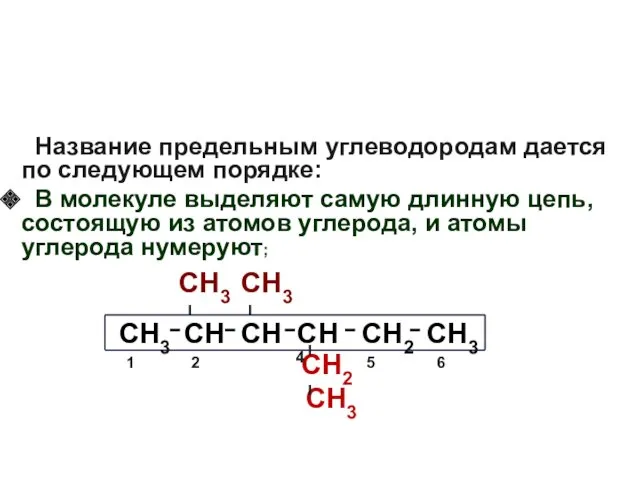
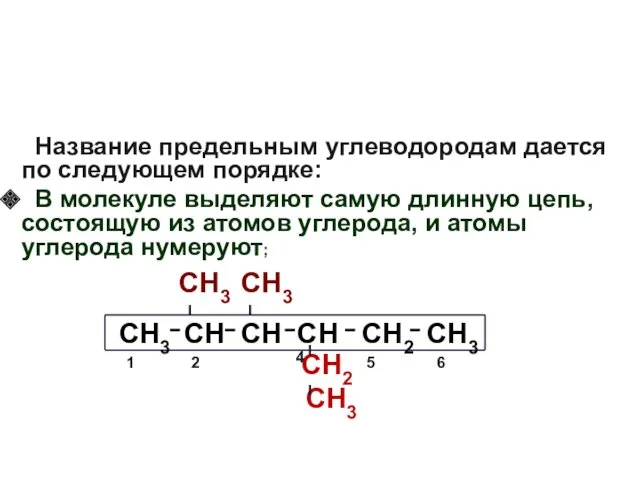
- 12. Название предельным углеводородам дается по следующем порядке: В молекуле выделяют самую длинную цепь, состоящую из атомов
- 13. Название предельным углеводородам дается по следующем порядке: В молекуле выделяют самую длинную цепь, состоящую из атомов
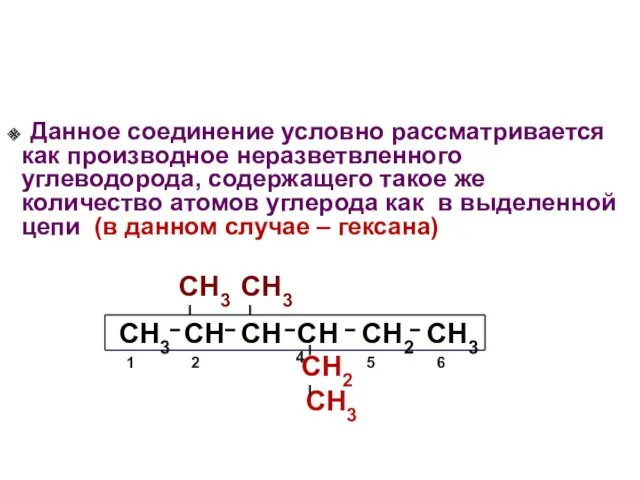
- 14. Данное соединение условно рассматривается как производное неразветвленного углеводорода, содержащего такое же количество атомов углерода как в
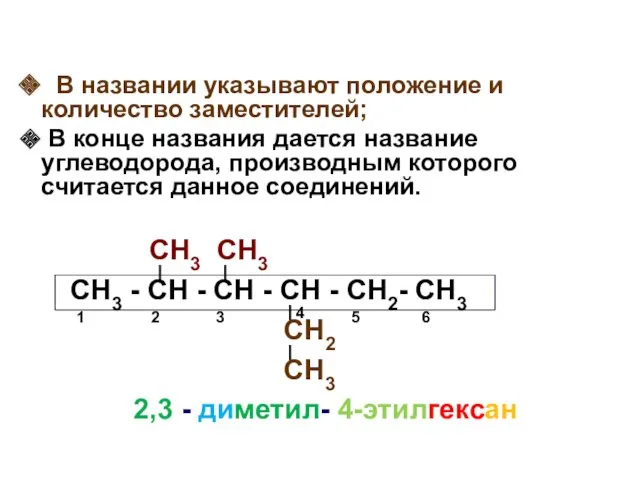
- 15. СН3 СН3 СН3 - СН - СН - СН - СН2- СН3 СН2 СН3 2,3 -
- 16. Физико-химические свойства алканов Все алканы не растворимы в воде; Алканы, содержащие не более 5 углеродных атомов,
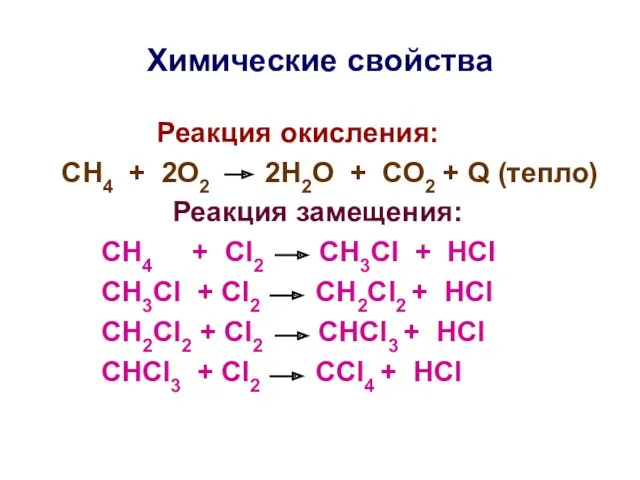
- 17. Химические свойства Реакция окисления: СН4 + 2О2 2Н2О + СО2 + Q (тепло) Реакция замещения: СН4
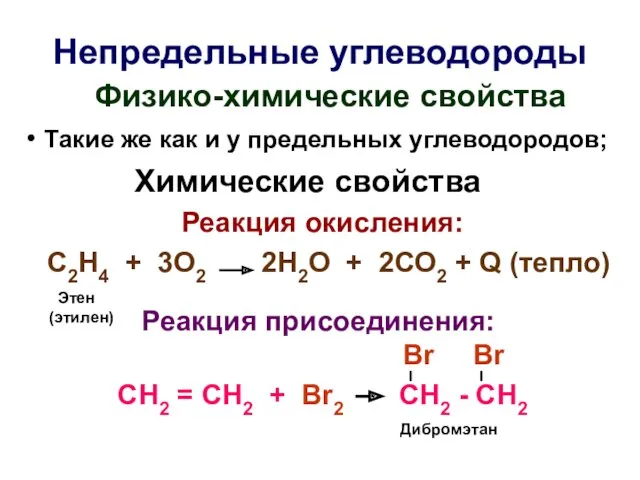
- 18. Непредельные углеводороды Физико-химические свойства Такие же как и у предельных углеводородов; Химические свойства Реакция окисления: С2Н4
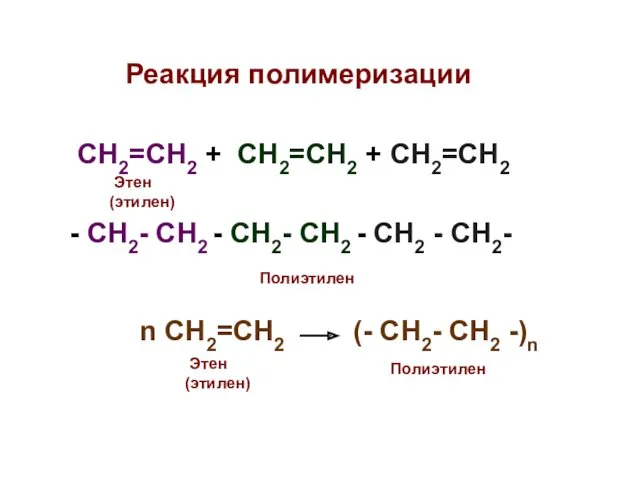
- 19. Реакция полимеризации СН2=СН2 + СН2=СН2 + СН2=СН2 - СН2- СН2 - СН2- СН2 - СН2 -
- 20. Номенклатура непредельных углеводов За основу названия берется название соответствующего предельного углеводорода, и в этом названии вместо
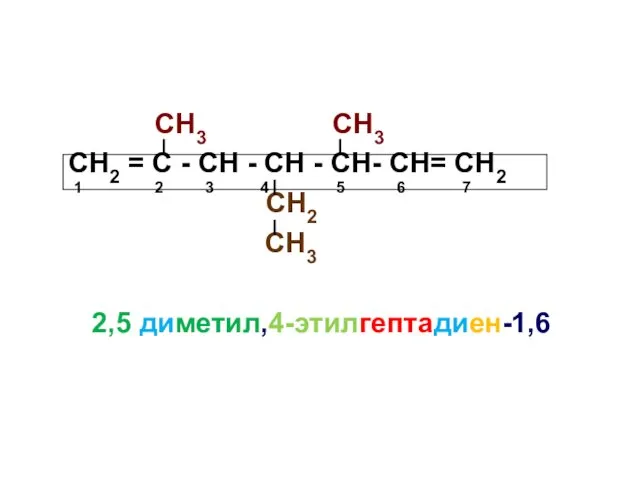
- 21. СН3 СН3 СН2 = С - СН - СН - СН- СН= СН2 СН2 СН3 2,5
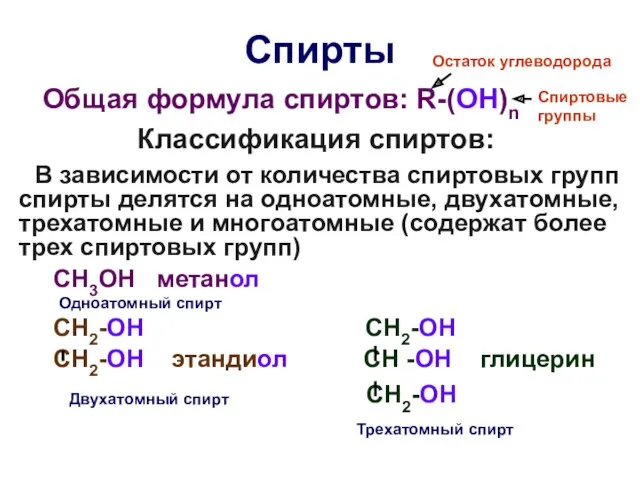
- 22. Спирты Общая формула спиртов: R-(OH)n Классификация спиртов: В зависимости от количества спиртовых групп спирты делятся на
- 23. Физико-химические свойства спиртов Низкомолекулярные спирты, содержащие не более 11-12 атомов углерода, являются жидкостями; Высокомолекулярные спирты, содержащие
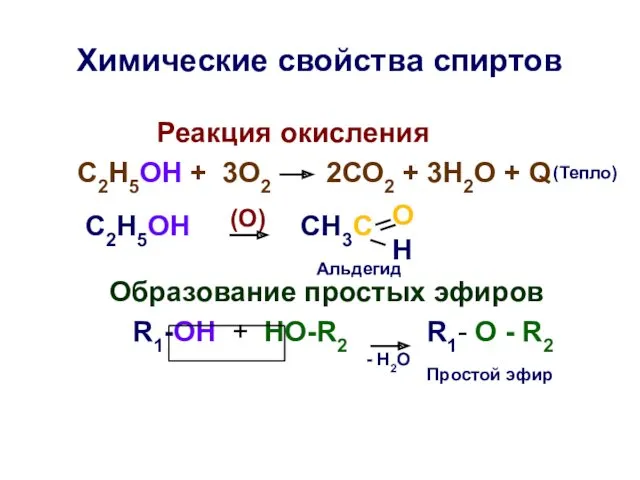
- 24. Химические свойства спиртов Реакция окисления С2Н5ОН + 3О2 2СО2 + 3Н2О + Q С2Н5ОН CH3C Образование
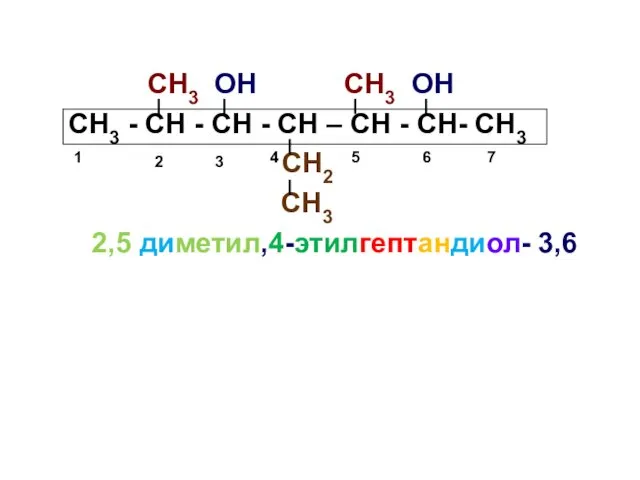
- 25. Номенклатура спиртов За основу названия берется название углеводорода, входящего в молекулу спирта, и добавляется окончание «ол»
- 26. СН3 ОН СН3 ОН СН3 - СН - СН - СН – СН - СН- СН3
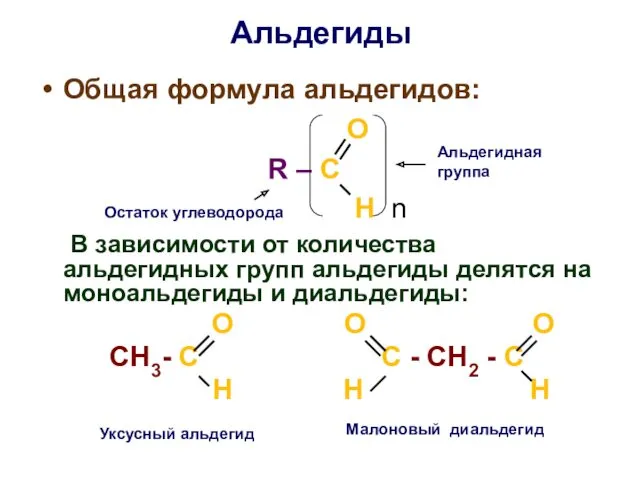
- 27. Альдегиды Общая формула альдегидов: O R – C H n В зависимости от количества альдегидных групп
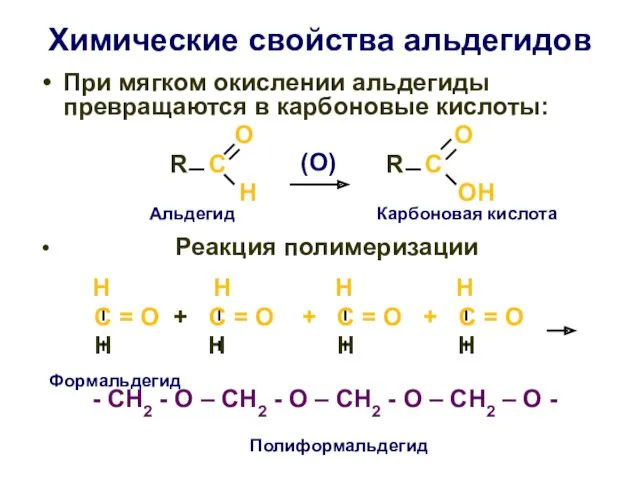
- 28. Химические свойства альдегидов При мягком окислении альдегиды превращаются в карбоновые кислоты: О О R C R
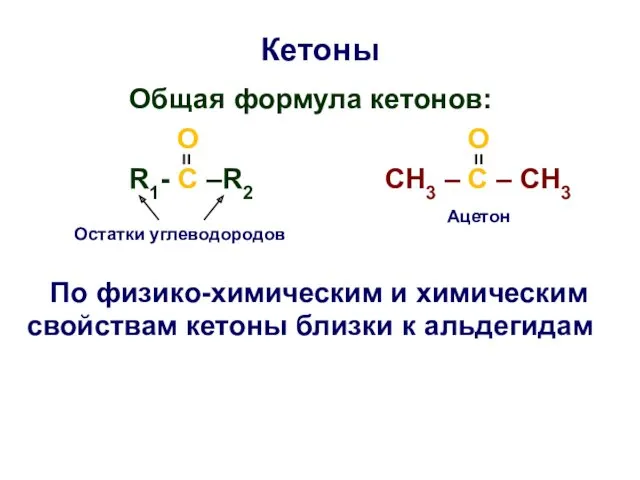
- 29. Кетоны Oбщая формула кетонов: O O R1- C –R2 CH3 – C – CH3 По физико-химическим
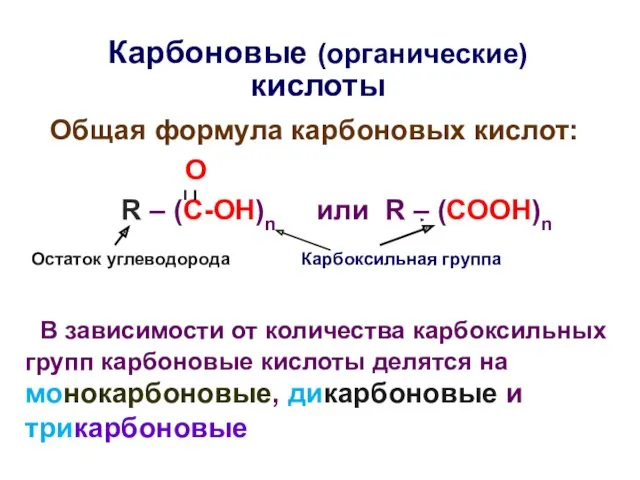
- 30. Карбоновые (органические) кислоты Общая формула карбоновых кислот: О R – (C-OH)n или R – (COOH)n В
- 31. CH3 COOH COOH COOH CH2 CH2 CH2 HO- C- COOH COOH CH2 COOH В зависимости от
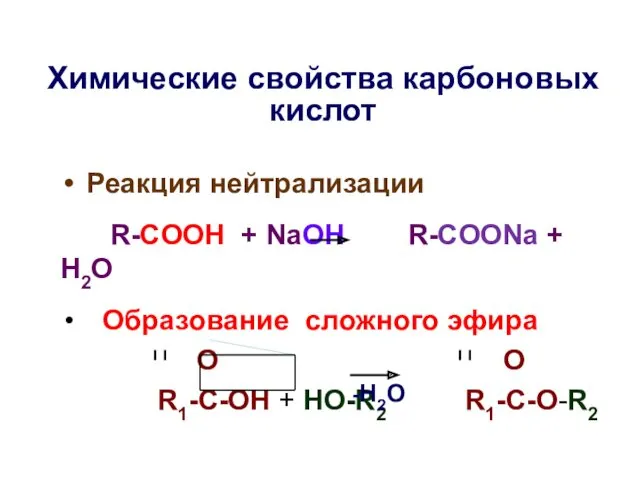
- 32. Химические свойства карбоновых киcлот Реакция нейтрализации R-COOH + NaOH R-COONa + H2O Образование сложного эфира O
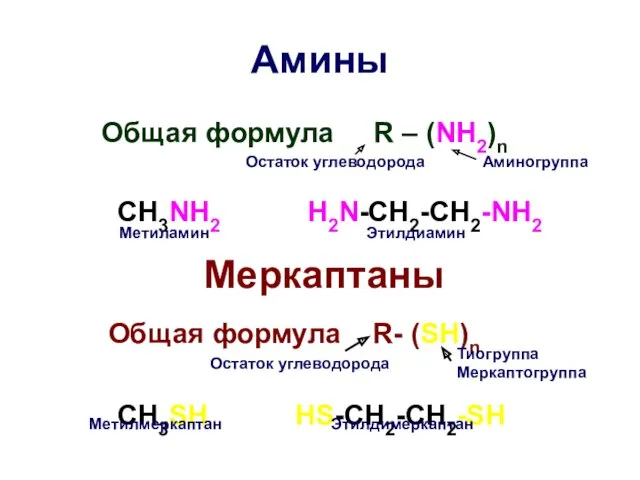
- 33. Амины Общая формула R – (NH2)n CH3NH2 H2N-CH2-CH2-NH2 Меркаптаны Общая формула R- (SH)n CH3SH HS-CH2-CH2-SH Остаток
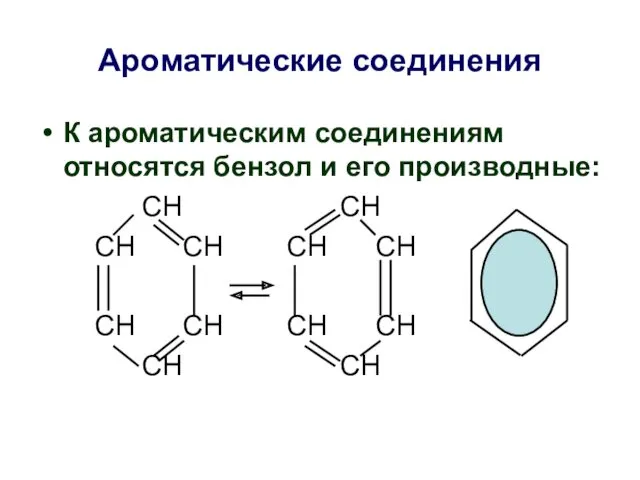
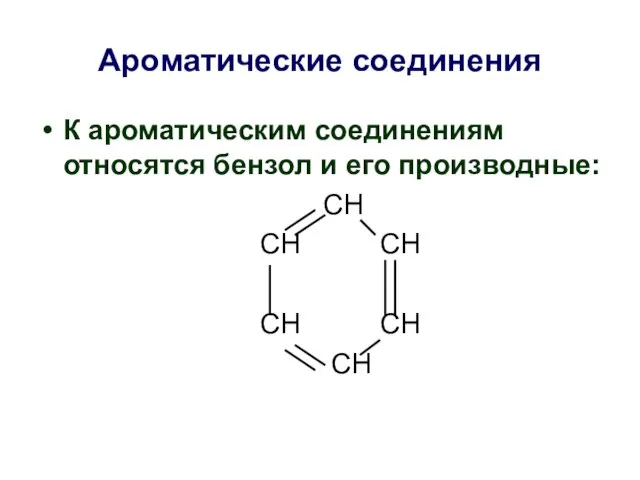
- 34. Ароматические соединения К ароматическим соединениям относятся бензол и его производные: СН СН СН СН СН СН
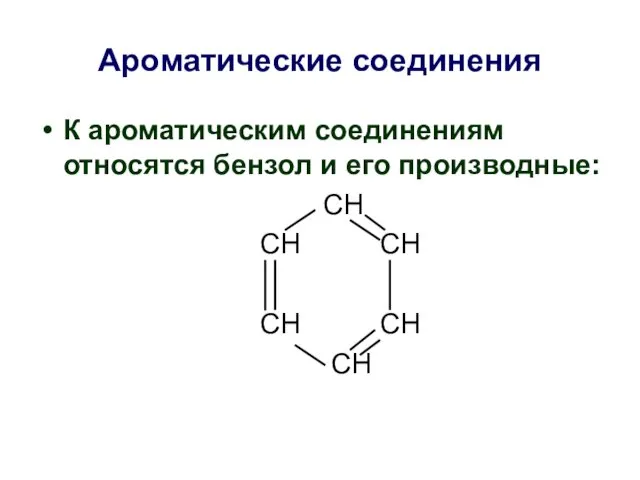
- 35. Ароматические соединения К ароматическим соединениям относятся бензол и его производные: СН СН СН СН СН СН
- 36. Ароматические соединения К ароматическим соединениям относятся бензол и его производные: СН СН СН СН СН СН
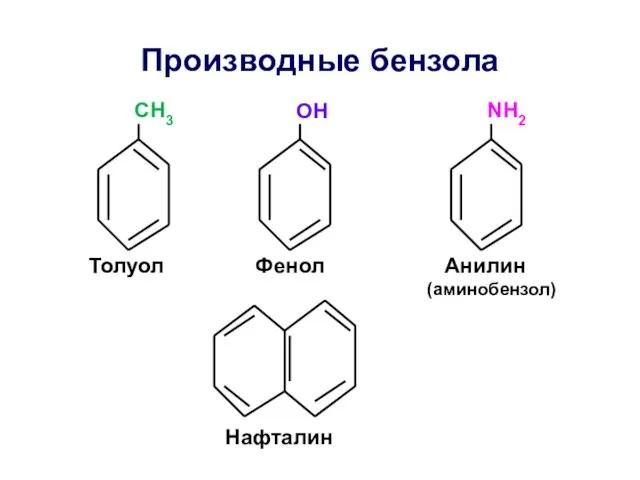
- 37. Производные бензола СН3 ОН NH2 Толуол Фенол Анилин (аминобензол) Нафталин
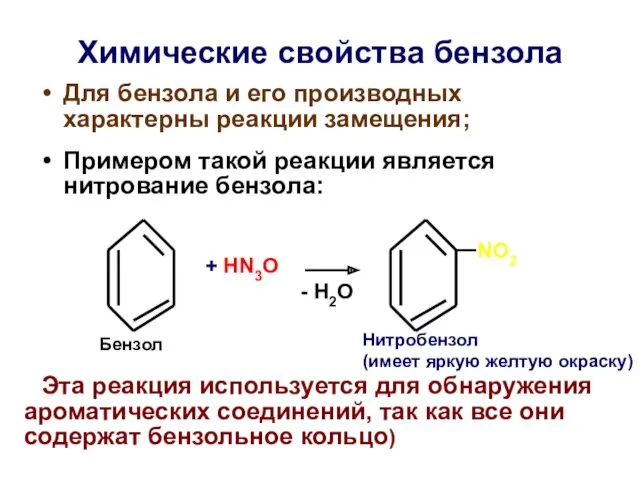
- 38. Химические свoйства бензола Для бензола и его производных характерны реакции замещения; Примером такой реакции является нитрование
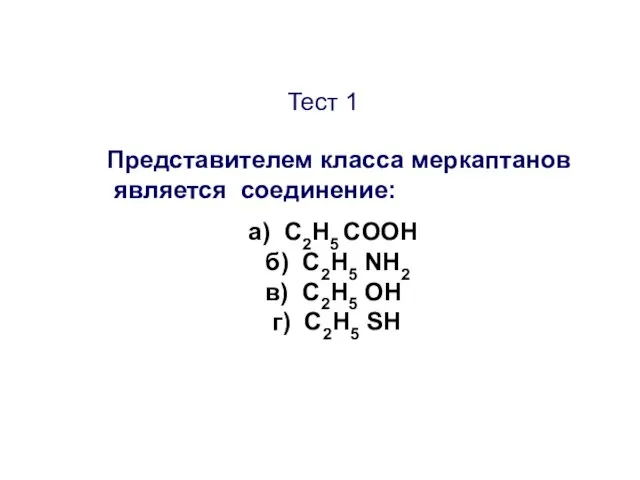
- 39. Тест 1 Представителем класса меркаптанов является соединение: а) C2H5 COOH б) C2H5 NH2 в) C2H5 ОН
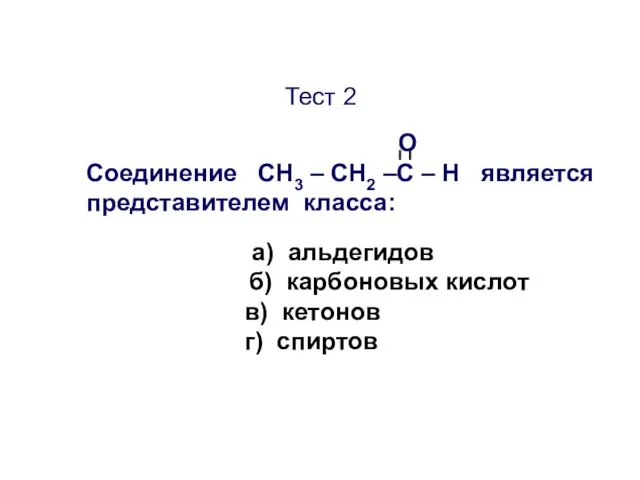
- 40. Тест 2 О Соединение CН3 – СН2 –С – Н является представителем класса: а) альдегидов б)
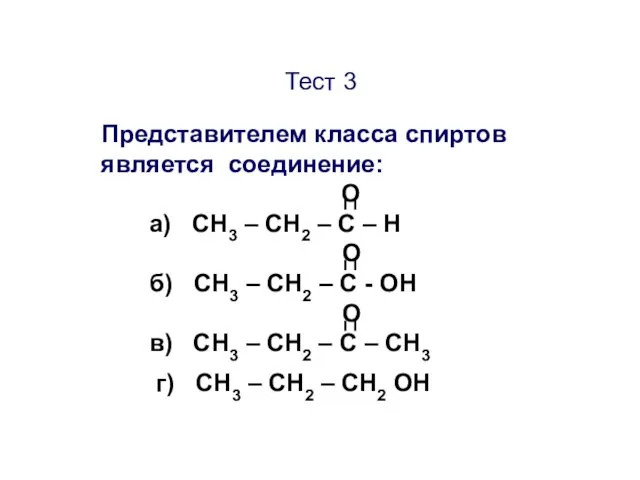
- 41. Тест 3 Представителем класса спиртов является соединение: О а) CН3 – СН2 – С – Н
- 42. Бензольное кольцо содержит: а) бутанол б) толуол в) циклопептан г) циклогексан Тест 4
- 43. Тест 5 В реакцию присоединения легко вступают: а) ароматические углеводороды б) непредельные углеводороды в) предельные углеводороды
- 44. Тест 5 Синтетическим полимером является: а) белок б) полипропилен в) крахмал г) целлюлоза
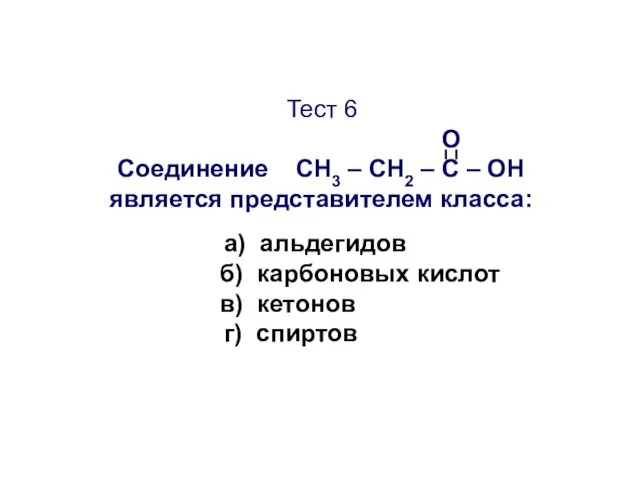
- 45. Тест 6 О Соединение CН3 – СН2 – С – ОН является представителем класса: а) альдегидов
- 46. Тест 7 Атомы углерода в органических соединениях образуют: а) одну ковалентную связь б) две ковалентные связи
- 47. Тест 8 Карбоновые кислоты легко вступают в реакцию: а) с альдегидами б) с бензолом б) с
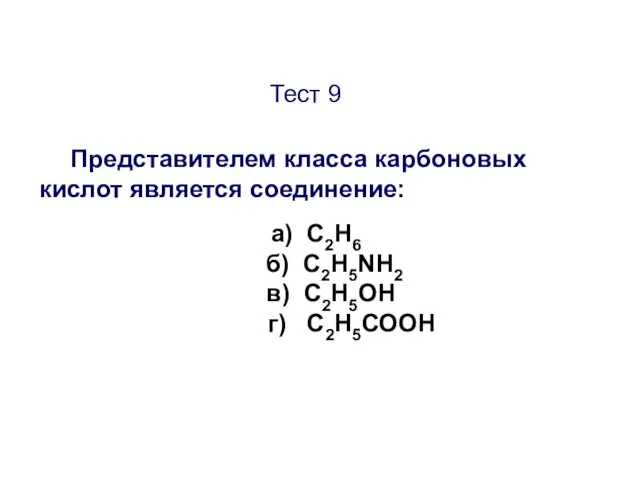
- 48. Тест 9 Представителем класса карбоновых кислот является соединение: а) C2H6 б) C2H5NH2 в) C2H5ОН г) C2H5СООН
- 49. Тест 10 Для обнаружения ароматических соединений применяется реакция: а) гидролиза б) изомеризации в) нитрования г) фосфоролиза
- 50. Тест 11 Соединение НО- CН2 – СН2 – СН2 – ОН является представителем класса: а) одноатомных
- 51. Тест 12 Атомы углерода в органических соединениях соединяются: а) водородными связями б) ионными связями в) ковалентными
- 53. Скачать презентацию

















 Основы российского трудового и уголовного права
Основы российского трудового и уголовного права Презентация Наше здоровье - в наших руках
Презентация Наше здоровье - в наших руках Международные стандарты ISO серии 10000 - технологии поддержки стандартов ISO серии 9000
Международные стандарты ISO серии 10000 - технологии поддержки стандартов ISO серии 9000 Максим Горький. Биография
Максим Горький. Биография Мастер-класс Новогодний подсвечник из солёного теста
Мастер-класс Новогодний подсвечник из солёного теста Экологические проблемы в центрально-азиатском регионе
Экологические проблемы в центрально-азиатском регионе Создание условий для развития детской одаренности у детей дошкольного возраста.
Создание условий для развития детской одаренности у детей дошкольного возраста. Презентация к уроку. Черчение - 8 класс (по А.Д.Ботвинникову). Тема урока: Общие сведения о проецировании.
Презентация к уроку. Черчение - 8 класс (по А.Д.Ботвинникову). Тема урока: Общие сведения о проецировании. 20231105_moya_funk_gramotnost1902
20231105_moya_funk_gramotnost1902 Служба психолого-педагогического сопровождения в условиях современной школы интернатного типа.
Служба психолого-педагогического сопровождения в условиях современной школы интернатного типа. презентация на тему: Особенности работы учителя-логопеда в рамках реализации ФГОС в ДО
презентация на тему: Особенности работы учителя-логопеда в рамках реализации ФГОС в ДО Презентация ЗДОРОВЬЕСБЕРЕГАЮЩИЕ ТЕХНОЛОГИИ НА УРОКАХ РУССКОГО ЯЗЫКА И ЛИТЕРАТУРЫ
Презентация ЗДОРОВЬЕСБЕРЕГАЮЩИЕ ТЕХНОЛОГИИ НА УРОКАХ РУССКОГО ЯЗЫКА И ЛИТЕРАТУРЫ Достопримечательности Бахчисарайского района, полуострова Крым
Достопримечательности Бахчисарайского района, полуострова Крым Методы оптимальных решений. Транспортная задача
Методы оптимальных решений. Транспортная задача Итоговая работа по курсу повышения квалификации. Формирование ключевых компетенций в игровой деятельности дошкольников
Итоговая работа по курсу повышения квалификации. Формирование ключевых компетенций в игровой деятельности дошкольников Основные элементы налога
Основные элементы налога Правовые основы воинской службы
Правовые основы воинской службы Политическая элита и политическое лидерство
Политическая элита и политическое лидерство проект Что нам осень подарила был создан октябрь 2013г.
проект Что нам осень подарила был создан октябрь 2013г. Травянистые биогеоценозы
Травянистые биогеоценозы Родительское собрание Учим детей мыслить
Родительское собрание Учим детей мыслить Системы уравнений. Метод подстановки
Системы уравнений. Метод подстановки 6 Путешествие в страну Грамота (звуки Х, Хь, буква Х)
6 Путешествие в страну Грамота (звуки Х, Хь, буква Х) Историческое сочинение
Историческое сочинение Функции цитоплазматической мембраны. Цитология микроорганизмов
Функции цитоплазматической мембраны. Цитология микроорганизмов День православной книги
День православной книги Организация сюжетно-ролевой игры с детьми дошкольного возраста.
Организация сюжетно-ролевой игры с детьми дошкольного возраста. Сочетание рынка и государства в смешанной экономике. Лекция 1
Сочетание рынка и государства в смешанной экономике. Лекция 1