Содержание
- 2. Химические свойства азота Химически пассивен, не реагирует с кислотами, щелочами, серой, с галогенами (кроме фтора). Незначительно
- 3. Соединения азота Соединения азота со степенью окисления азота – 3 Нитриды Как упомянуто выше, при высоких
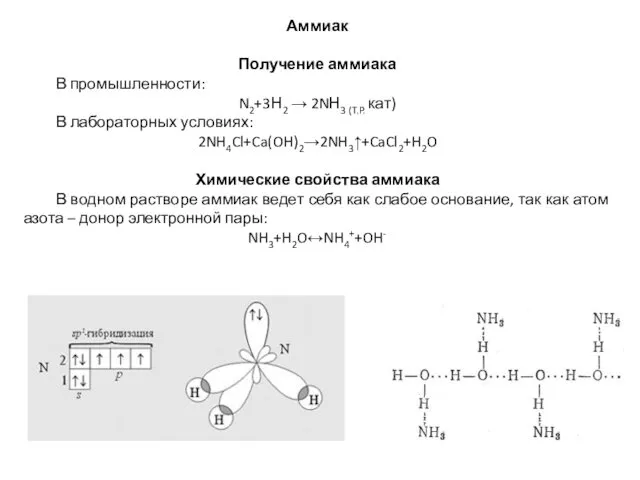
- 4. Аммиак Получение аммиака В промышленности: N2+3Н2 → 2NН3 (T.P. кат) В лабораторных условиях: 2NH4Cl+Ca(OH)2→2NH3↑+CaCl2+H2O Химические свойства
- 5. Взаимодействие с кислотами: NH3+HCl→NH4Cl Реакции комплексообразования: Сu2++4NH3→[Cu(NH3)4]2+ Восстановительные свойства аммиака: 3СuO+2NH3→3Cu+N2+3H2O
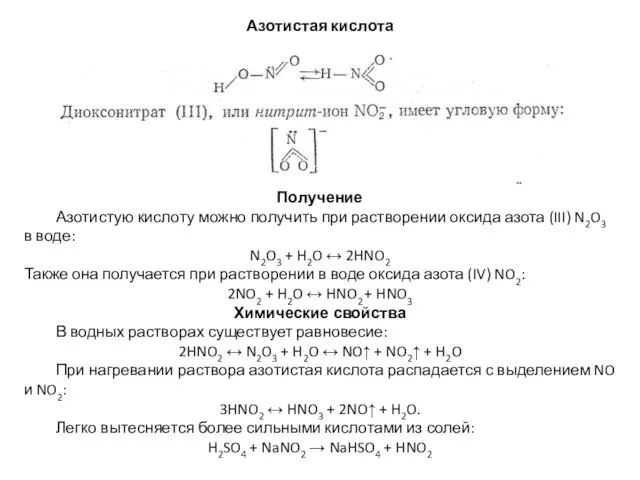
- 6. Азотистая кислота Получение Азотистую кислоту можно получить при растворении оксида азота (III) N2O3 в воде: N2O3
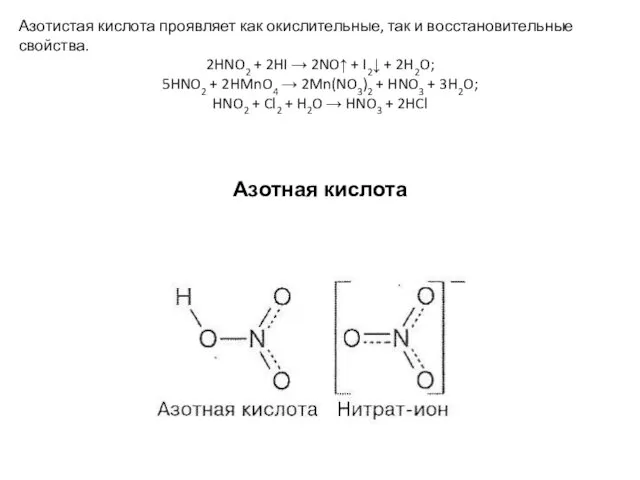
- 7. Азотистая кислота проявляет как окислительные, так и восстановительные свойства. 2HNO2 + 2HI → 2NO↑ + I2↓
- 8. Химические свойства азотной кислоты Высококонцентрированная HNO3 имеет обычно бурую окраску вследствие происходящего на свету процесса разложения:
- 9. Разбавленная HNO3 б) с металлами, стоящими в ряду напряжений левее водорода: Азотная кислота окисляет неметаллы, при
- 10. и сложные вещества, например: Нитраты Соли азотной кислоты — нитраты — при нагревании необратимо разлагаются, продукты
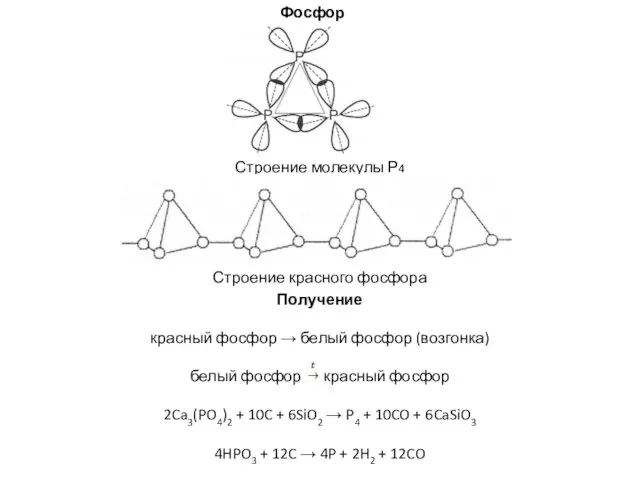
- 11. Фосфор Строение молекулы Р4 Строение красного фосфора Получение красный фосфор → белый фосфор (возгонка) белый фосфор
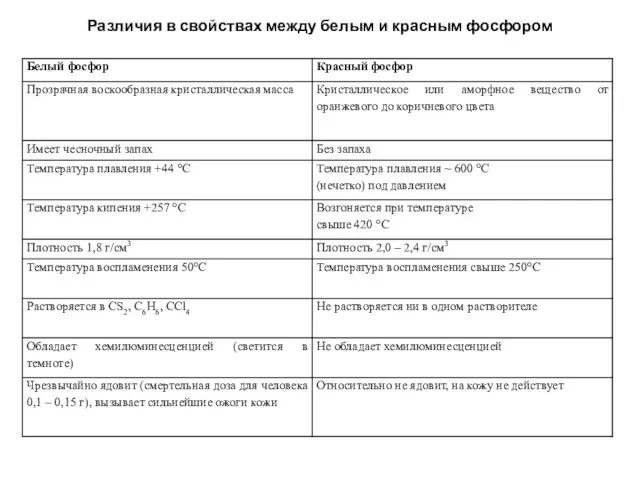
- 12. Различия в свойствах между белым и красным фосфором
- 13. Взаимодействие с водой 8Р + 12Н2О = 5РН3 + 3Н3РО4 (фосфорная кислота). Взаимодействие со щелочами 4Р
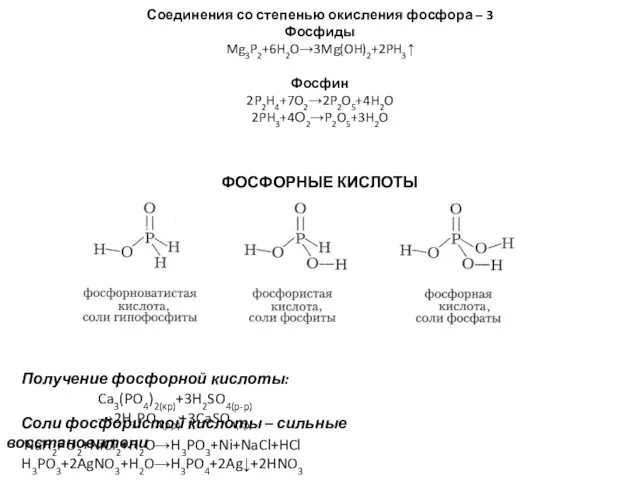
- 14. Соединения со степенью окисления фосфора – 3 Фосфиды Mg3P2+6H2O→3Mg(OH)2+2PH3↑ Фосфин 2P2H4+7O2→2P2O5+4H2O 2PH3+4О2→P2O5+3H2O ФОСФОРНЫЕ КИСЛОТЫ NaH2PO2+NiCl2+H2O→H3PO3+Ni+NaCl+HCl H3PO3+2AgNO3+H2O→H3PO4+2Ag↓+2HNO3
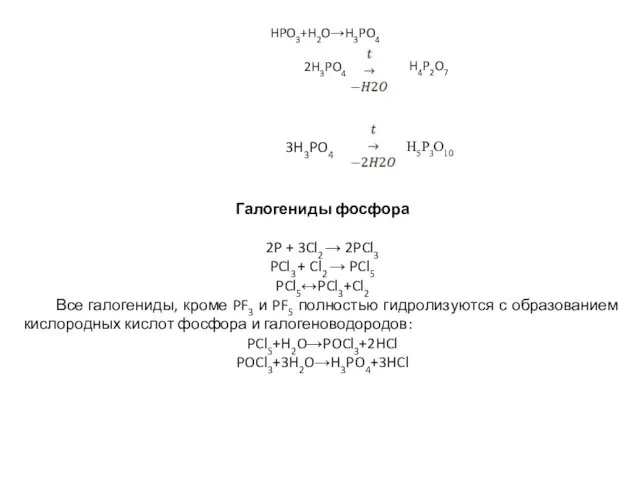
- 15. HPO3+H2O→H3PO4 2H3PO4 H4P2O7 H5P3O10 Галогениды фосфора 2P + 3Cl2 → 2PCl3 PCl3 + Cl2 → PCl5
- 16. Подгруппа мышьяка Степени окисления As, Sb и Bi равны – 3, +3, +5 Химические свойства мышьяка
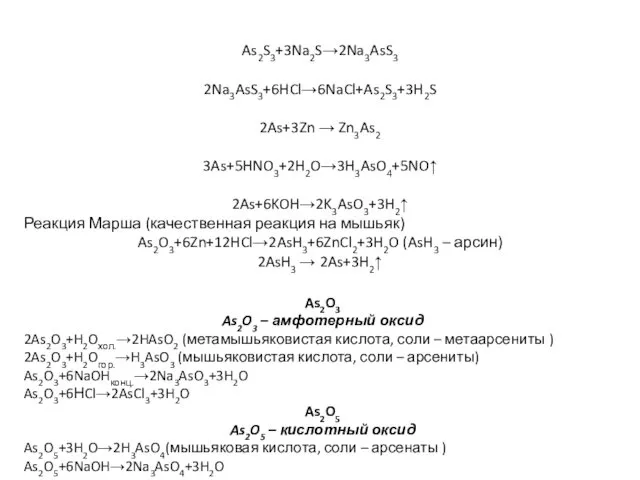
- 17. As2S3+3Na2S→2Na3AsS3 2Na3AsS3+6HCl→6NaCl+As2S3+3H2S 2As+3Zn → Zn3As2 3As+5HNO3+2H2O→3H3AsO4+5NO↑ 2As+6KOH→2K3AsO3+3H2↑ Реакция Марша (качественная реакция на мышьяк) As2O3+6Zn+12HCl→2AsH3+6ZnCl2+3H2O (AsH3 –
- 18. Сурьма и ее соединения Взаимодействие с кислородом: 2Sb+3O2→2Sb2O3 Sb2O3 – амфотерный оксид, образующий при взаимодействии со
- 19. Взаимодействует с некоторыми металлами: 2Sb+3Mg Mg3Sb2 Взаимодействует с кислотами-окислителями: 2Sb+10HNO3конц.→Sb2O5+5NO2↑+10H2O В отличии от мышьяка с кислородными
- 20. Соли сурьмы (III), в водном растворе подвергаются гидролизу с образованием основных солей (оксосолей): SbCl3 + 2H2O
- 21. Химические свойства Взаимодействие с кислородом: 2Bi+3O2 Bi2O3 Взаимодействие с галогенами: 2Bi+3Cl2 2BiCl3 Для солей висмута, как
- 23. Скачать презентацию


![Взаимодействие с кислотами: NH3+HCl→NH4Cl Реакции комплексообразования: Сu2++4NH3→[Cu(NH3)4]2+ Восстановительные свойства аммиака: 3СuO+2NH3→3Cu+N2+3H2O](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/43568/slide-4.jpg)









 Теоретическая грамматика английского языка
Теоретическая грамматика английского языка Игра Собери портфель
Игра Собери портфель Сеть фитнес клубов My Fit
Сеть фитнес клубов My Fit Общие сведения о радиоматериалах
Общие сведения о радиоматериалах Организация профессиональной деятельности повара с разработкой технологии приготовления и оформления блюда утка фаршированная
Организация профессиональной деятельности повара с разработкой технологии приготовления и оформления блюда утка фаршированная Сенім дегеніміз не? Евр 11:1-2
Сенім дегеніміз не? Евр 11:1-2 презентация проекта Большая книга сказок
презентация проекта Большая книга сказок Программа обучения стажера
Программа обучения стажера Внеклассное мероприятие В гостях у сказки
Внеклассное мероприятие В гостях у сказки Сложные эфиры. Жиры. Мыла
Сложные эфиры. Жиры. Мыла HAICTC el planeta es para nuestros hijos. BIOMASA primera fuente de energías renovables
HAICTC el planeta es para nuestros hijos. BIOMASA primera fuente de energías renovables воспитательный час счастлив тот, кто счастлив у себя дома
воспитательный час счастлив тот, кто счастлив у себя дома Проектирование участков цехов ДСтП
Проектирование участков цехов ДСтП Электр жетектердегі өтпелі процестер
Электр жетектердегі өтпелі процестер Русский народный праздник Ефремов день
Русский народный праздник Ефремов день Часть речи существительное
Часть речи существительное Безработица, её причины и последствия
Безработица, её причины и последствия Презентация НИР
Презентация НИР Презентация по теме Предельные углеводороды 10 класс УМК О.С.Габриелян
Презентация по теме Предельные углеводороды 10 класс УМК О.С.Габриелян Дидактическая игра Что лишнее?
Дидактическая игра Что лишнее? Презентация к методической разработке: Покормите птиц зимой
Презентация к методической разработке: Покормите птиц зимой Презентация к уроку Бабочка (бисер)
Презентация к уроку Бабочка (бисер) Древнегерманские племена. Классификация по Плинию
Древнегерманские племена. Классификация по Плинию Tele2 зажигает свет мобильных перемен
Tele2 зажигает свет мобильных перемен Vspomogatelnoe_oborudovanie_teplovoza
Vspomogatelnoe_oborudovanie_teplovoza Проектная деятельность, как средство реализации ФГОС
Проектная деятельность, как средство реализации ФГОС Психологические особенности подросткового возраста и роль родительских установок на формирование личности.
Психологические особенности подросткового возраста и роль родительских установок на формирование личности. La France. Французский язык
La France. Французский язык