Слайд 2

Хроматография –
физико – химический метод разделения и анализа смеси веществ,
основанный на раз-личном распределении компо-нентов между двумя несме-шивающимися фазами.
Слайд 3

Основные понятия
Сорбция – поглощение газов, паров и растворенных веществ твердыми
или жидкими поглотителями (сорбентами);
Сорбтив – вещество, молекулы которого способны сорбироваться;
Сорбат – вещество в адсорбирован-ном состоянии;
Слайд 4

Элюирование – процесс перемещения веществ вместе с подвижной фазой через слой
неподвижной фазы
Элюент – растворитель или газ, проходящий через слой неподвижной фазы – подвижная фаза;
Элюат – подвижная фаза, выходящая из колонки и содержащая разделенные компоненты
Слайд 5
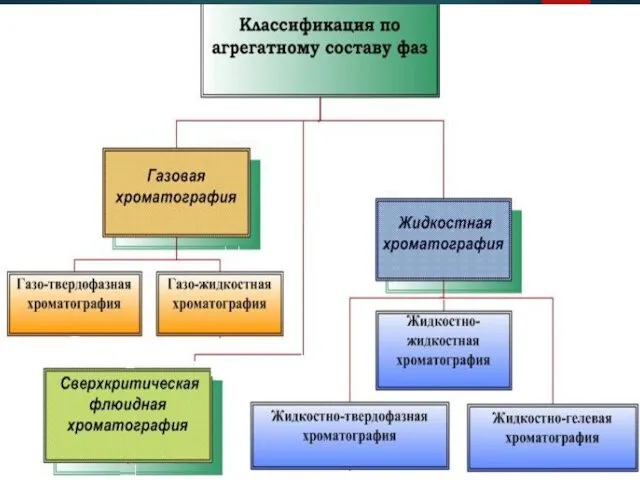
Слайд 6
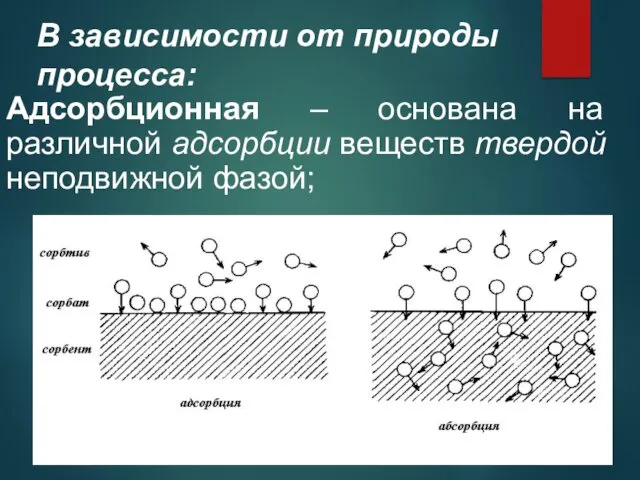
В зависимости от природы процесса:
Адсорбционная – основана на различной адсорбции
веществ твердой неподвижной фазой;
Слайд 7

Распределительная – основана на различной растворимости сорбатов в жидкой неподвижной фазе;
Ионообменная
- основана на различной способности к ионному обмену веществ с ионогенными группами неподвижной фазы;
Слайд 8

Осадочная – основана на различной растворимости осадков , получающихся после реакции
взаимодействия с осадителем, содержащимся в неподвижной фазе;
Эксклюзионная (молекулярно – ситовая или гелевая) – основана на различии в размерах и формах молекул разделяемых веществ;
Слайд 9

Аффинная – основана на специфических взаимодействиях биологических объектов (ферментов, и т.д.)
с группами на поверхности твердой фазы.
Слайд 10

В зависимости от способа оформления процесса:
Колоночная – процесс разделения проводят
в колонках, заполненных неподвижной фазой;
Плоскостная – процесс разделения проводят на хроматографической бумаге (бумажная) или тонком слое сорбента, нанесенном на подложку (тонкослойная).
Слайд 11

Теоретические основы хроматографии
Слайд 12

Основа процесса хроматографии – неравновесная адсорбция
Изотерма адсорбции Ленгмюра
В области низких давлений
(кон-центраций):
уравнение Генри
Слайд 13

Эффективность разделения компо-нентов определяется числом теоре-тических тарелок (N).
! Чем больше N
и уже их высота (H), тем эффективнее колонка
Высота, эквивалентная теоретичес-кой тарелке – ВЭТТ – (H) опре-деляется:
Слайд 14

A – вихревая диффузия:
где λ – характеристика набивки колон-ки, dp –
диаметр зерна сорбента
Слайд 15

B – продольная (осевая) диффузия – диффузия компонентов в подвижной фазе:
где
γ – эмпирический коэффициент, DM – коэффициент диффузии
Слайд 16

С – внутренняя диффузия – зависит от способности адсорбироваться на неподвижной
фазе;
u – линейная скорость потока
L – длина колонки, tM – время удер-живания несорбируемого компонента.
Слайд 17

Слайд 18

Газовая хроматография - это метод разделения летучих соединений, основанный на распределении
веществ между подвижной фазой (ПФ) - газом и неподвижной фазой (НФ) с сорбентом с большой площадью поверхности
Слайд 19

Подвижная фаза - инертный газ (азот, гелий, водород, аргон, углекислый газ),
протекающий через НФ;
! ПФ выполняет только транспорт-ную функцию
! ПФ должна обеспечивать мак-симальную чувствительность детек-тора
Слайд 20

Неподвижная фаза
В газо-адсорбционной хроматогра-фии - твердый сорбент с развитой мелкопористой поверхностью;
размер зерен 0.1-0.5 мм
силикагель
активный уголь
Слайд 21

В газо-жидкостной хроматографии - пленка жидкости, нанесенная на поверхность твердого носителя
полимерные
Слайд 22

Типы жидкой НФ:
Неполярные (насыщенные углеводо-роды);
Умеренно полярные (сложные эфиры, нитрилы);
Полярные (многоатомные спирты,
гликоли)
! Полярность НФ должна быть близка к полярности веществ анализируемой пробы
Слайд 23

Требования к жидкой НФ :
хорошо растворять компоненты смеси;
прочно удерживаться
на твердом носителе;
быть термически устойчивой;
быть нелетучей при данной температуре;
обладать высокой селективностью;
быть химически инертной.
Слайд 24

Слайд 25

Подвижная фаза в жидкостной хроматографии – чистый раствори-тель или смесь растворителей
Жидкостная
хроматография в которой используют колонки малого размера и высокое давление ПФ (до 0.5 – 70 МПа) называют высокоэффектив-ной жидкостной хроматографией (ВЭЖХ)
Слайд 26

Ионообменная хроматография
Слайд 27

Неподвижная фаза
Иониты природного или синтетического происхождения:
цеолиты, глинистые материалы (природные алюмосиликаты);
сульфированые активные угли;
синтетические ионообменные смолы
Слайд 28

Неподвижная фаза
Катиониты – иониты, обменивающиеся с раствором катионами:
Сильнокислотные - R-SO3H
Среднекислотные -
R-PO3H2
Слабокислотные - R-COOH
R-OH
Слайд 29

Уравнение катионного обмена
R-SO3H + Na+ ⮀ R-SO3Na + H+
Н- форма
Na- форма
! Форма катионита определяется его противоионом, т.е. катионом, способным к обмену
Слайд 30

Неподвижная фаза
Аниониты – иониты, обменивающиеся с раствором анионами:
Сильноосновные - R-[N(CH3)3]+OH-
Среднеосновные -
R-[NH(CH3)2]+OH-
Слабоосновные - R-[NH3] +OH-
Слайд 31
![Уравнение анионного обмена R-[NH3]+OH− + Cl−⮀ R-[NH3]+Cl − + OH−](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/45090/slide-30.jpg)
Уравнение анионного обмена
R-[NH3]+OH− + Cl−⮀ R-[NH3]+Cl − + OH−
OН- форма Cl-
форма
Амфолиты – иониты, содержащие как катионогенные, так и анионогенные группы
Слайд 32

Регенерация ионитов
!Ионный обмен обратим
Регенерация – восстановление свойств ионита
Регенерация катионита:
R-SO3Na + H+
⮀ R-SO3H + Na+
Регенерация анионита:
R-[NH3]+Cl − + OH− ⮀ R-[NH3]+OH− + Cl−
Слайд 33

Плоскостная хроматография





























![Уравнение анионного обмена R-[NH3]+OH− + Cl−⮀ R-[NH3]+Cl − + OH−](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/45090/slide-30.jpg)


 Изобразительное искусство. Семья пространственных искусств. Урок 1 6 класс
Изобразительное искусство. Семья пространственных искусств. Урок 1 6 класс РАБОТЫ УЧАЩИХСЯ 2А класса по информатике и ИКТ
РАБОТЫ УЧАЩИХСЯ 2А класса по информатике и ИКТ Формирование целевых ориентиров дошкольного образования в условиях ФГОС, требования по обеспечению надёжности и безопасности их использования.
Формирование целевых ориентиров дошкольного образования в условиях ФГОС, требования по обеспечению надёжности и безопасности их использования. Бутерброд-networking
Бутерброд-networking Принятие решений при формировании коммуникационной политики
Принятие решений при формировании коммуникационной политики День государственного флага ДНР
День государственного флага ДНР Татарские народные костюмы!!!
Татарские народные костюмы!!! Технология создания и обработки графической информации
Технология создания и обработки графической информации Причины возникновения девиаций в поведении детей и подростков.
Причины возникновения девиаций в поведении детей и подростков. Компоненты компьютерной системы
Компоненты компьютерной системы 22 июня 1941 года. Начало Великой Отечественной войны
22 июня 1941 года. Начало Великой Отечественной войны Микронасосы. Принцип действия микронасосов
Микронасосы. Принцип действия микронасосов Литейное производство
Литейное производство Обучающий семинар для участников XXIII Республиканского конкурса научных работ студентов
Обучающий семинар для участников XXIII Республиканского конкурса научных работ студентов 48 законов Грина
48 законов Грина Строительство и оснащение многопрофильного реабилитационного центра для детей-инвалидов
Строительство и оснащение многопрофильного реабилитационного центра для детей-инвалидов Суда с современным парусным вооружением
Суда с современным парусным вооружением Применение лекарственных средств
Применение лекарственных средств Классный час Первый раз в 1 - ый класс. До свидания, 1- ый класс!
Классный час Первый раз в 1 - ый класс. До свидания, 1- ый класс! Обработка информации. 5 класс
Обработка информации. 5 класс Каспий экологиясы
Каспий экологиясы Текстовый процессор Writer
Текстовый процессор Writer Введение в учебный курс Отечественная история
Введение в учебный курс Отечественная история дидактическое пособие по логопедии (презентация)
дидактическое пособие по логопедии (презентация) Занятие по внеурочной деятельности. Школа здоровья. Советы доктора ВОДЫ
Занятие по внеурочной деятельности. Школа здоровья. Советы доктора ВОДЫ Игра как активная форма развития воображения у детей дошкольного возраста
Игра как активная форма развития воображения у детей дошкольного возраста Чрезвычайные ситуации мирного и военного времени. Единая государственная система предупреждения и ликвидации ЧС (РСЧС)
Чрезвычайные ситуации мирного и военного времени. Единая государственная система предупреждения и ликвидации ЧС (РСЧС) Самостоятельная двигательная активность детей в условиях ограниченного пространства
Самостоятельная двигательная активность детей в условиях ограниченного пространства