Содержание
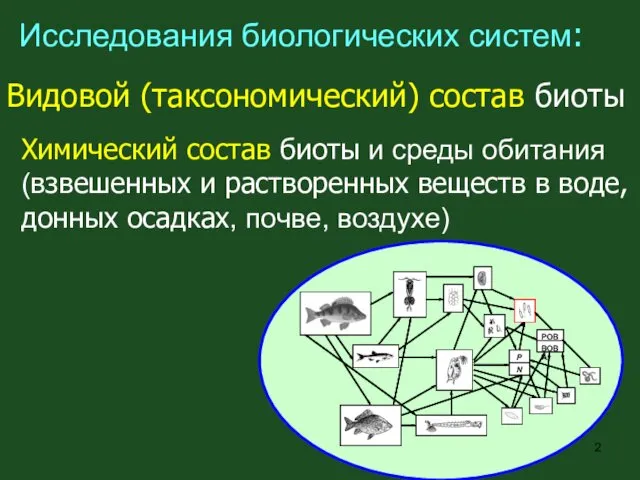
- 2. Исследования биологических систем: Видовой (таксономический) состав биоты Химический состав биоты и среды обитания (взвешенных и растворенных
- 3. Цели анализа химического состава биологических систем Выполнение задач экологического мониторинга Информация о составе биологической продукции, используемой
- 4. Анализ химического состава биоты и окружающей среды (воды, воздуха, почв) – необходимая часть экологического мониторинга: Элементный
- 5. Анализ химического состава биоты и окружающей среды – необходимая часть экологического мониторинга Элементный состав включает: Стехиометрия
- 6. После катастрофы на Саяно-Шушенской ГЭС (2009 г.) оказался востребованным анализ нефтепродуктов (смесей углеводородов) в р.Енисей Состав
- 7. Анализ биомассы как источника полезной для человека продукции Биомасса животных – источник белка, аминокислот, витаминов, незаменимых
- 8. Фотометрические, включая колориметрию, цветные реакции Флуоресцентные, включая спектральный анализ Электрохимические Спектроскопические (атомная абсорбция, эмиссия) Физико-химические методы
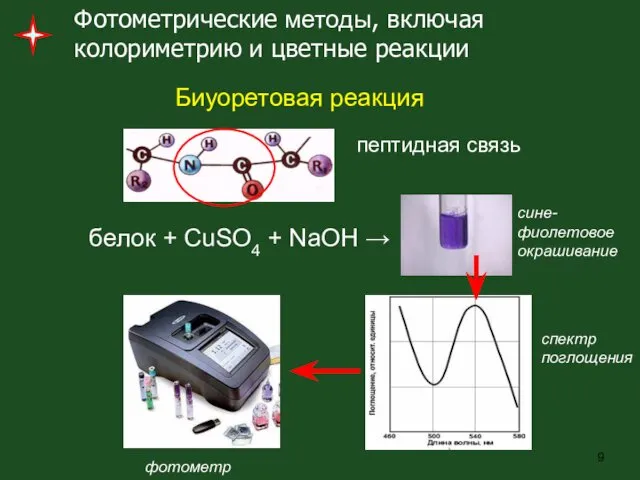
- 9. Фотометрические методы, включая колориметрию и цветные реакции пептидная связь Биуоретовая реакция белок + CuSO4 + NaOH
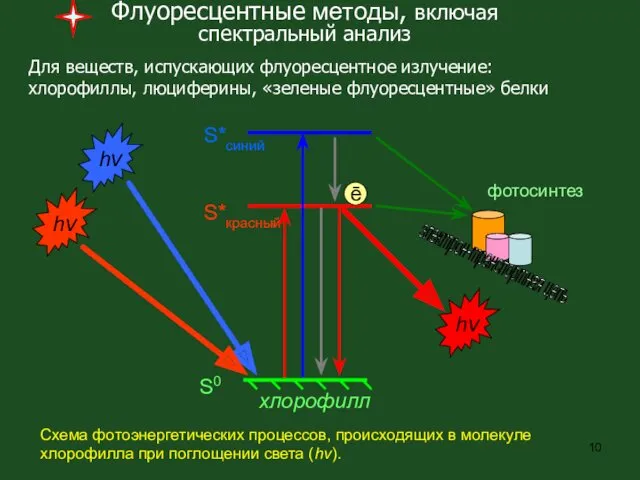
- 10. Флуоресцентные методы, включая спектральный анализ Для веществ, испускающих флуоресцентное излучение: хлорофиллы, люциферины, «зеленые флуоресцентные» белки Схема
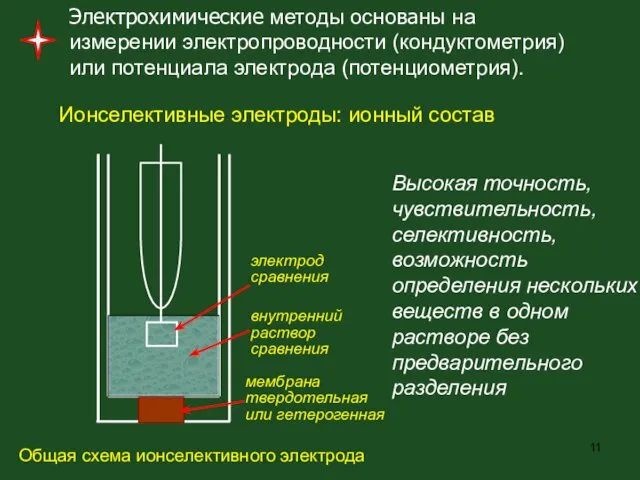
- 11. Электрохимические методы основаны на измерении электропроводности (кондуктометрия) или потенциала электрода (потенциометрия). Высокая точность, чувствительность, селективность, возможность
- 12. Спектроскопические методы (атомная абсорбция, эмиссия) Для валового содержания металлов и ряда неметаллов проба + кислота t
- 13. Спектроскопические методы (атомная абсорбция, эмиссия) Атомно-абсорбционная спектрометрия Атомизация термически и пламенем t = 3000 oC газообразное
- 14. Спектроскопические методы (атомная абсорбция, эмиссия) Атомно-эмиссионная спектрометрия с индуктивно-связанной плазмой Электрический разряд в магнитном поле аргоновая
- 15. Применяемые методы анализа Неорганические вещества и элементы Органические вещества Спектроскопические методы (атомная абсорбция, эмиссия) Спектрофотометрические методы
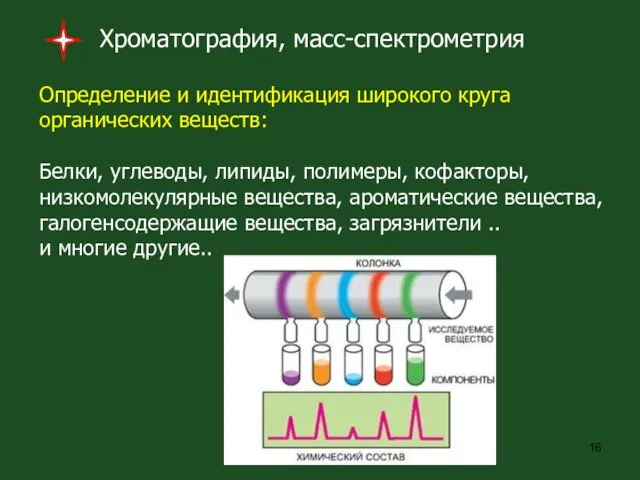
- 16. Хроматография, масс-спектрометрия Определение и идентификация широкого круга органических веществ: Белки, углеводы, липиды, полимеры, кофакторы, низкомолекулярные вещества,
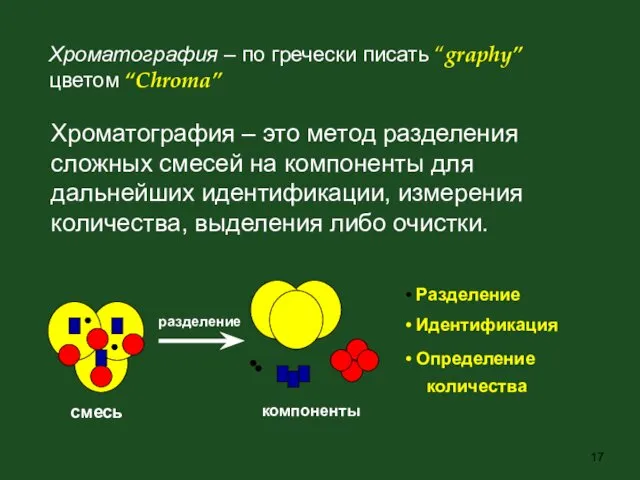
- 17. Хроматография – по гречески писать “graphy” цветом “Chroma” Хроматография – это метод разделения сложных смесей на
- 18. Михаил Семенович Цвет 1872 – 1919, Ботаник, физиолог Изобретение хроматографии - 1903 г. «…различные компоненты сложного
- 19. В 1931 г. лаборатория Р. Куна и Е.Ледерера, изучавших разновидности каротеноидов, подтвердила перспективность хроматографического метода М.С.Цвета
- 20. Все виды хроматографии имеют две фазы 1. стационарная (адсорбент) фаза Материал, на котором происходит разделение 2.
- 21. Хроматография аналитическая Цели анализа препаративная Недеструктивные методы, очищение продукта
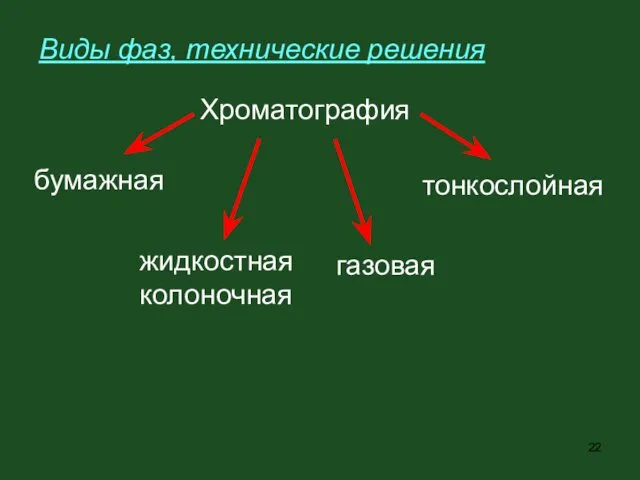
- 22. Виды фаз, технические решения Хроматография бумажная тонкослойная газовая жидкостная колоночная
- 23. Бумажная хроматография – разделяет сухие пробы с помощью жидкого растворителя на полосе бумаги (стационарная фаза) Жидкостная
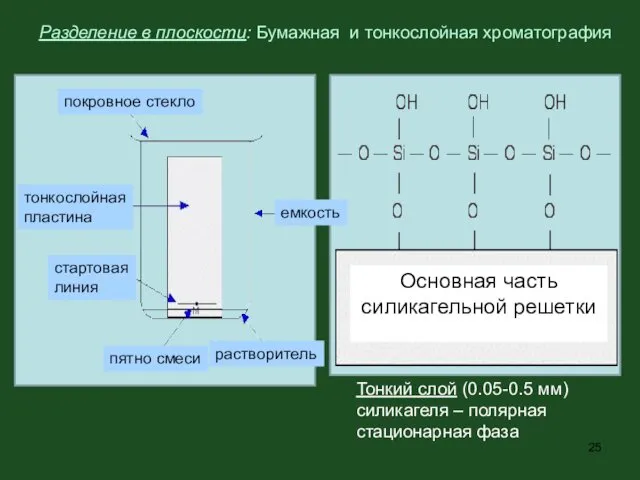
- 24. Разделение в плоскости: Бумажная и тонкослойная хроматография
- 25. Тонкий слой (0.05-0.5 мм) силикагеля – полярная стационарная фаза покровное стекло растворитель пятно смеси тонкослойная пластина
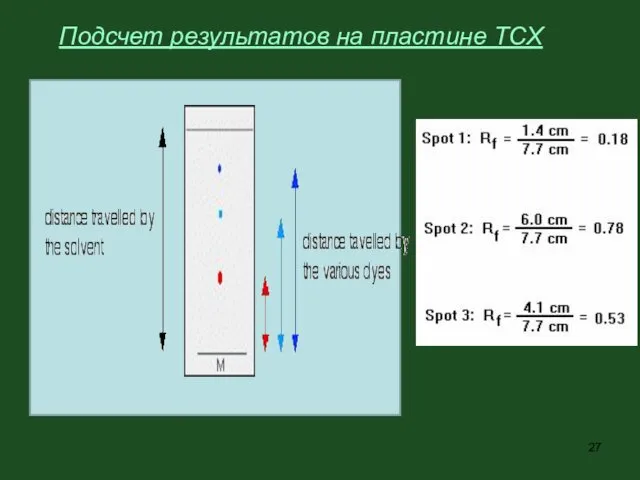
- 26. Подсчет результатов на пластине ТСХ Rf = Соотношение расстояний, пройденных веществом и растворителем линия старта линия
- 27. Подсчет результатов на пластине ТСХ
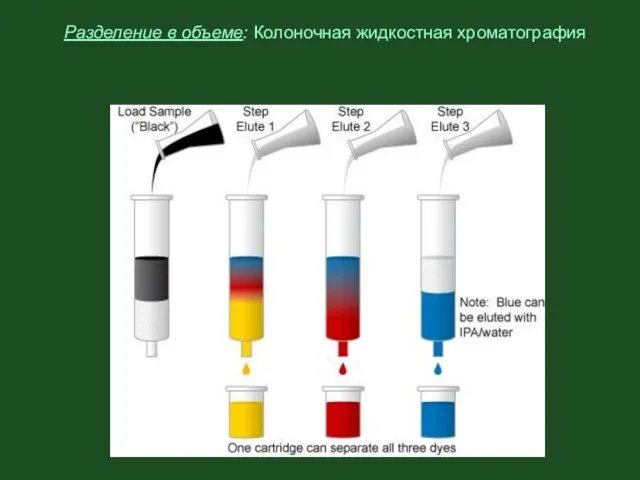
- 28. Разделение в объеме: Колоночная жидкостная хроматография
- 29. Высокоэффективная жидкостная хроматография и газовая хроматография - современные приборные варианты колоночной хроматографии. Например в ВЭЖХ, вместо
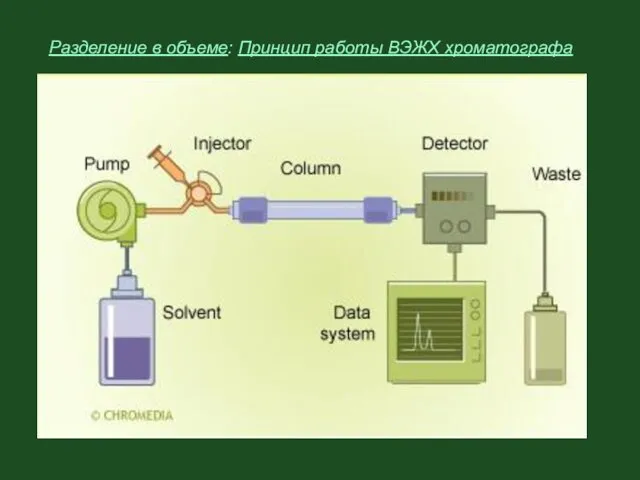
- 30. Разделение в объеме: Принцип работы ВЭЖХ хроматографа
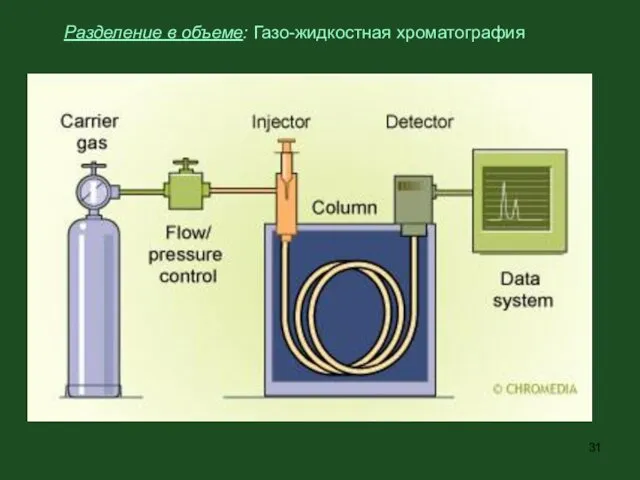
- 31. Разделение в объеме: Газо-жидкостная хроматография
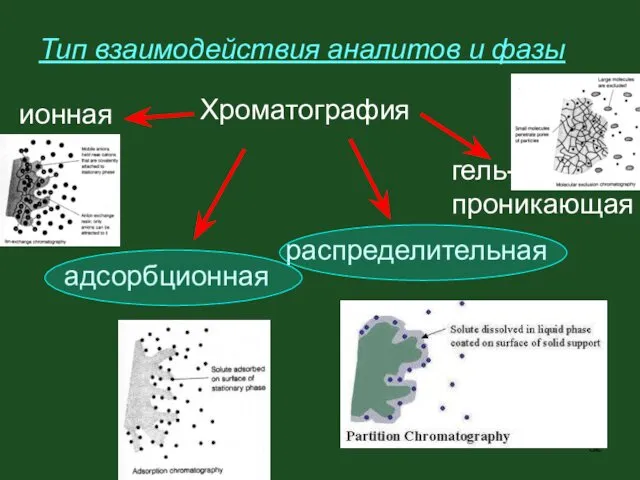
- 32. Тип взаимодействия аналитов и фазы Хроматография ионная гель- проникающая адсорбционная распределительная
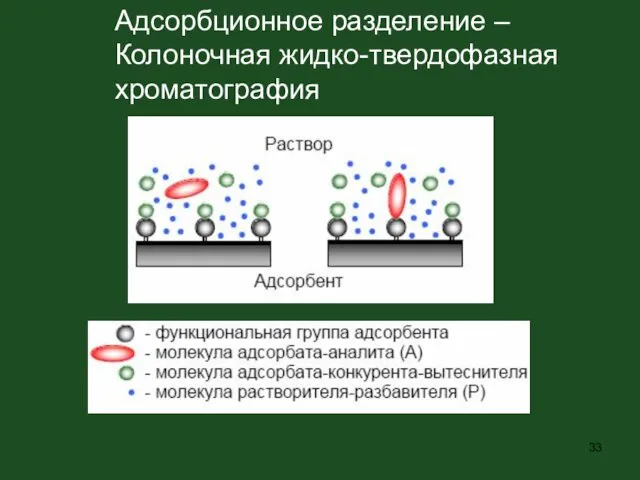
- 33. Адсорбционное разделение – Колоночная жидко-твердофазная хроматография
- 34. Формирование хроматографического пика На выходе (детекторе) записывается серия пиков. Каждый пик представляет собой одно вещество из
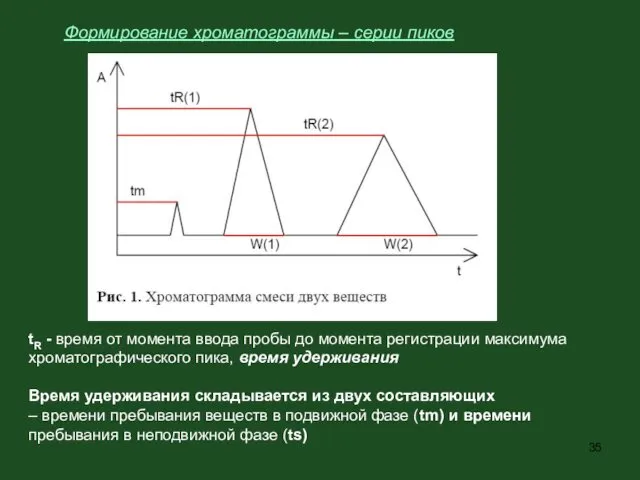
- 35. Формирование хроматограммы – серии пиков tR - время от момента ввода пробы до момента регистрации максимума
- 36. Хроматографические параметры tm – мертвое время колонки исправленное время удерживания t’ = tR – tm коэффициент
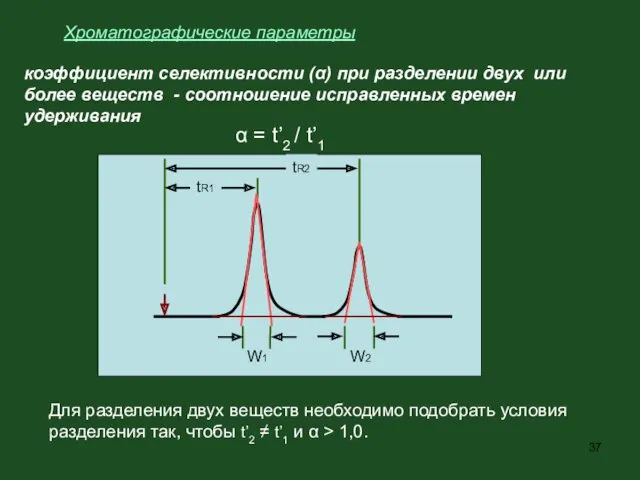
- 37. Хроматографические параметры коэффициент селективности (α) при разделении двух или более веществ - соотношение исправленных времен удерживания
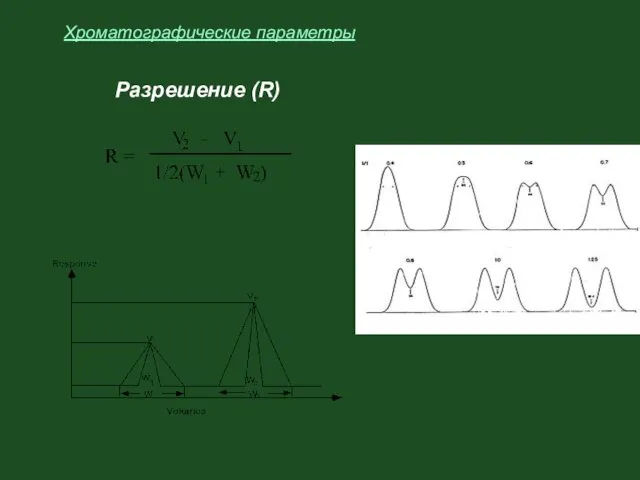
- 38. Разрешение (R) Хроматографические параметры
- 39. Хроматографические параметры Чем эффективнее колонка, тем уже пик, тем большее число компонентов можно разделить за более
- 40. Хроматографические параметры
- 42. Скачать презентацию





















 Кінетична скульптура
Кінетична скульптура NCAB Outgoing Report
NCAB Outgoing Report Игровая зависимость (лудомания)
Игровая зависимость (лудомания) Уголок природы для детей среднего возраста 4-5 лет
Уголок природы для детей среднего возраста 4-5 лет Консалтинговый центр Стратегия успеха. Аттракционы для мероприятий. Тренинги командообразования
Консалтинговый центр Стратегия успеха. Аттракционы для мероприятий. Тренинги командообразования Презентация проекта Дымковская игрушка.
Презентация проекта Дымковская игрушка. Интернет - викторина Новый год шагает по планете
Интернет - викторина Новый год шагает по планете Итоговое сочинение по литературе
Итоговое сочинение по литературе Академия Вэлнэс. Продуктовая секция. Подробный тренинг по продукции Вэлнэс
Академия Вэлнэс. Продуктовая секция. Подробный тренинг по продукции Вэлнэс Презентация Помоги лисичке найти лисят. Звук Ш.
Презентация Помоги лисичке найти лисят. Звук Ш. Презентация И песня в бой вела
Презентация И песня в бой вела Техническая эксплуатация подвижного состава железных дорог. Организация работ участка ремонта колесных пар при ТР-2
Техническая эксплуатация подвижного состава железных дорог. Организация работ участка ремонта колесных пар при ТР-2 Общество, как саморазвивающаяся система
Общество, как саморазвивающаяся система Основы семьи и брака
Основы семьи и брака Зимняя сказка. Игра - тренажёр. (1 - 2 класс)
Зимняя сказка. Игра - тренажёр. (1 - 2 класс) Правка тонколистового металла и проволоки
Правка тонколистового металла и проволоки Проект тепличного комплекса Славный вегетарий на общественных землях
Проект тепличного комплекса Славный вегетарий на общественных землях Этапы развития реакции горя при утрате близких. Правила проведения психотерапии
Этапы развития реакции горя при утрате близких. Правила проведения психотерапии Моя семья - моё богатство. Важность и роль семьи в жизни человека
Моя семья - моё богатство. Важность и роль семьи в жизни человека Виртуальный музей ЧОУ СФМЛ при МИФИ
Виртуальный музей ЧОУ СФМЛ при МИФИ ВКР: Технология поверки и технического обслуживания микропроцессорного многоканального прибора Термодат12К5
ВКР: Технология поверки и технического обслуживания микропроцессорного многоканального прибора Термодат12К5 Состояние местной неспецифической резистентности организма при дисбактериозе у беременных женщин
Состояние местной неспецифической резистентности организма при дисбактериозе у беременных женщин Франция Бурбонов и Орлеанов: от революции 1830 года к новому политическому кризису
Франция Бурбонов и Орлеанов: от революции 1830 года к новому политическому кризису Проектирование котлованов. (Лекция 11)
Проектирование котлованов. (Лекция 11) Презентация Сравнение на уроках химии
Презентация Сравнение на уроках химии Умформер. Схема включения люминесцентных ламп
Умформер. Схема включения люминесцентных ламп Панч Зет
Панч Зет Производство халвы
Производство халвы