Содержание
- 2. Цель урока: Изучить строение, свойства, нахождение в природе, области применения карбоновых кислот Карбоновые кислоты- производные углеводородов,
- 3. 1 1 2 3 4 5 6 ☺ ☺ ☺
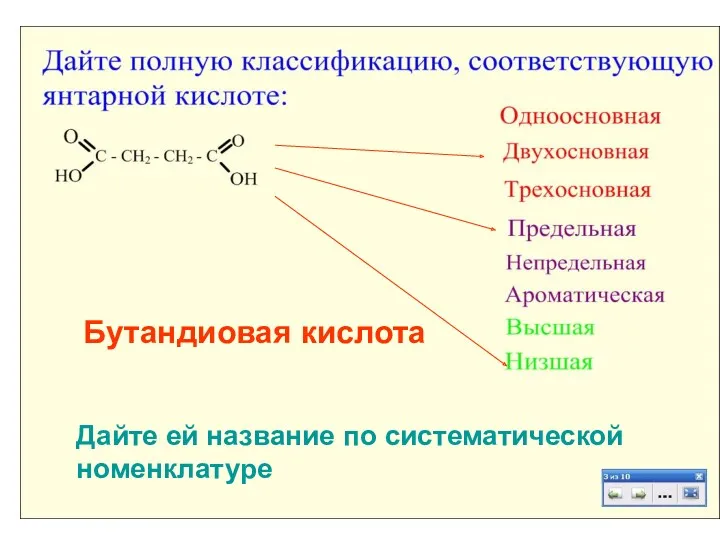
- 4. Бутандиовая кислота Бутандиовая кислота Дайте ей название по систематической номенклатуре
- 5. тест 1Карбоновые кислоты содержат функциональную группу 1)-он 2)-с=о 3)-сно 4)-соон 2 Она называется 1)Гидроксильная 2)карбонильная 3)Карбоксильная
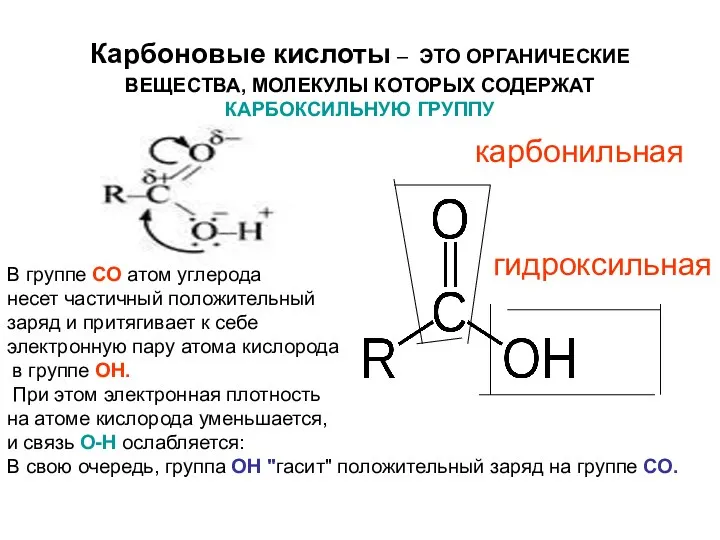
- 6. Карбоновые кислоты – ЭТО ОРГАНИЧЕСКИЕ ВЕЩЕСТВА, МОЛЕКУЛЫ КОТОРЫХ СОДЕРЖАТ КАРБОКСИЛЬНУЮ ГРУППУ гидроксильная карбонильная В группе СО
- 7. КИСЛОТЫ-сложные в-ва . Состоящие из катионов водорода и кислотного остатка НЕОРГАНИЧЕСКИЕ КИСЛОТЫ HnA сложные вещества, в
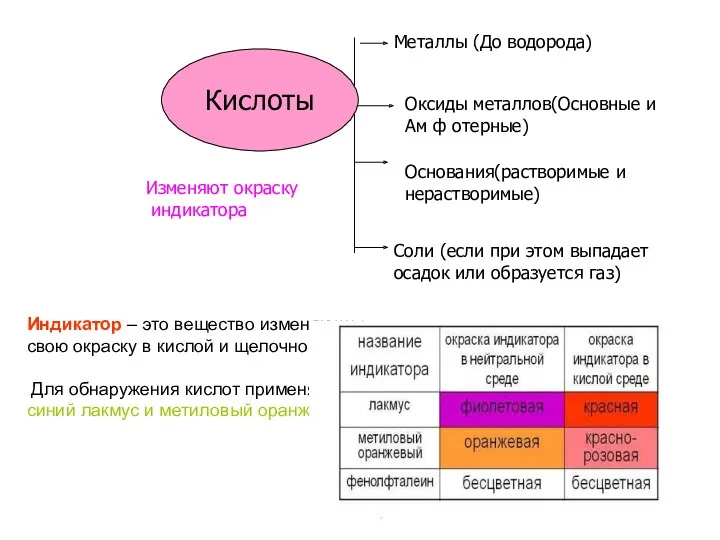
- 8. Металлы (До водорода) Оксиды металлов(Основные и Ам ф отерные) Основания(растворимые и нерастворимые) Соли (если при этом
- 9. Работа иследовательских групп Гипотеза : Возьмите инструкционные карты и проверьте наши предположения на примере уксусной кислоты
- 11. Взаимодействуя со спиртами, карбоновые кислоты образуют сложные эфиры (РЕАКЦИЯ ЭТЕРИФИКАЦИИ) CH3COOH + HOC2H5 CH3-CO-O-C2H5 + H2O
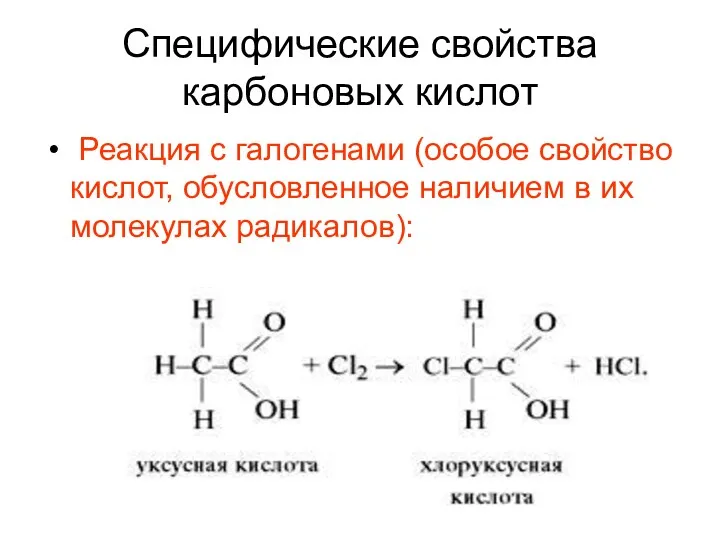
- 12. Специфические свойства карбоновых кислот Реакция с галогенами (особое свойство кислот, обусловленное наличием в их молекулах радикалов):
- 13. Особенности муравьиной кислоты (альдегидная группа) Н +Ag2O→ 2Ag +H2O+CO2 НСООН+2[Ag(NH3)2]OH→NH4HCO3+2Ag↓+3NH3↑ C* t t Реакция серебряного зеркала
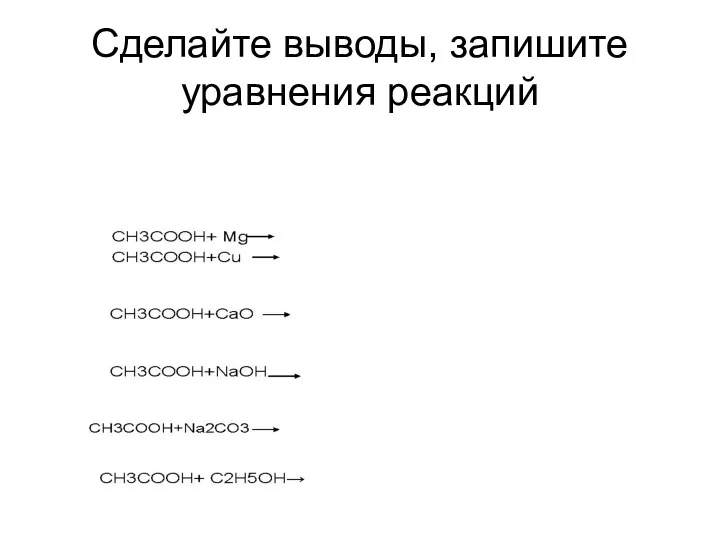
- 14. Сделайте выводы, запишите уравнения реакций
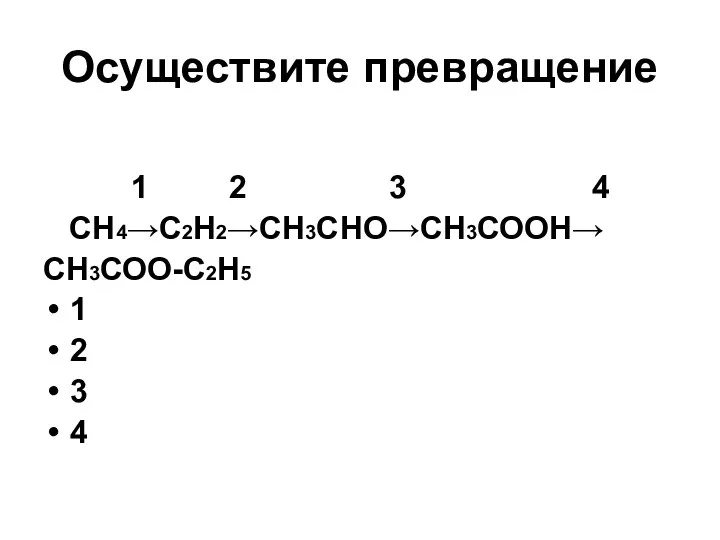
- 15. Осуществите превращение 1 2 3 4 СН4→С2Н2→СН3СНО→СН3СООН→ СН3СОО-С2Н5 1 2 3 4
- 16. Задача Мама печёт пирог для теста ей необходимо погасить чайную ложку пищевой соды (NaHCO3) столовым уксусом
- 18. Скачать презентацию







![Особенности муравьиной кислоты (альдегидная группа) Н +Ag2O→ 2Ag +H2O+CO2 НСООН+2[Ag(NH3)2]OH→NH4HCO3+2Ag↓+3NH3↑ C* t t Реакция серебряного зеркала](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/547459/slide-12.jpg)

 Электроснабжение коттеджа Мечта в Невском районе г. Санкт-Петербург
Электроснабжение коттеджа Мечта в Невском районе г. Санкт-Петербург Выпускной 2020 в КЗ Останкино
Выпускной 2020 в КЗ Останкино Формы в HTML-документе. Элементы форм
Формы в HTML-документе. Элементы форм Городской конкурс Учитель года 2014. 2 день. Методический семинар.
Городской конкурс Учитель года 2014. 2 день. Методический семинар. Трудом ковалась победа. 1941-1945
Трудом ковалась победа. 1941-1945 Биологическое действие искусственных электромагнитных излучений
Биологическое действие искусственных электромагнитных излучений презентация казахстан
презентация казахстан Хронический вирусный гепатит С с трансформацией в цирроз. Клинический случай
Хронический вирусный гепатит С с трансформацией в цирроз. Клинический случай Мышцы плечевого пояса и свободной верхней конечности
Мышцы плечевого пояса и свободной верхней конечности Разработка урока географии в 6 классе Мировой океан и его части
Разработка урока географии в 6 классе Мировой океан и его части Творчество С.Е.Есенина. 9 класс
Творчество С.Е.Есенина. 9 класс Профессиональные 4K ЖК мониторы c Медиа-плеером
Профессиональные 4K ЖК мониторы c Медиа-плеером Қазіргі дәстүрлі емес діни қозғалыстар мен бірлестіктер
Қазіргі дәстүрлі емес діни қозғалыстар мен бірлестіктер Дополнительные общеобразовательные общеразвивающие программы
Дополнительные общеобразовательные общеразвивающие программы Формирование предмета и метода экономической науки. Лекция 1
Формирование предмета и метода экономической науки. Лекция 1 Гражданская война в России 1917-1922 гг
Гражданская война в России 1917-1922 гг Методы экологического образования детей дошкольного возраста
Методы экологического образования детей дошкольного возраста Звуки [Ф] и [Ф’]. Буква Ф
Звуки [Ф] и [Ф’]. Буква Ф Творчество Хариной В.Т
Творчество Хариной В.Т Подготовка к сочинению-описанию по картине П.П. Кончаловского Сирень в корзине
Подготовка к сочинению-описанию по картине П.П. Кончаловского Сирень в корзине Бихевиоризм
Бихевиоризм Интеллектуальная игра По страницам книги по повести Ю. Я. Яковлева Зимородок
Интеллектуальная игра По страницам книги по повести Ю. Я. Яковлева Зимородок Конституция России
Конституция России Интеллектуальный марафон - 22 (2 класс)
Интеллектуальный марафон - 22 (2 класс) Исследовательский проект: Мобильный телефон - друг или враг?
Исследовательский проект: Мобильный телефон - друг или враг? Короткие и длинные волны на воде
Короткие и длинные волны на воде Конструктивно-технологичские особенности средств связи (LTE)
Конструктивно-технологичские особенности средств связи (LTE) Практические вопросы построения МП систем
Практические вопросы построения МП систем