Содержание
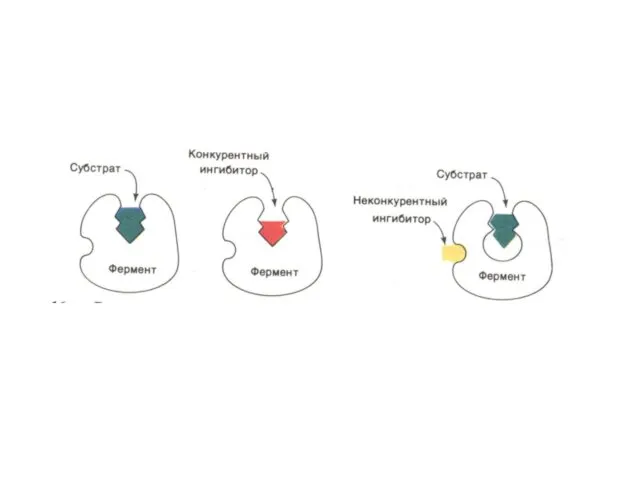
- 2. Кинетика ферментативных реакций Кинетическая схема Михаэлиса-Ментен
- 3. Квазистационарное приближение Скорость образования ES = Скорость расходования ES
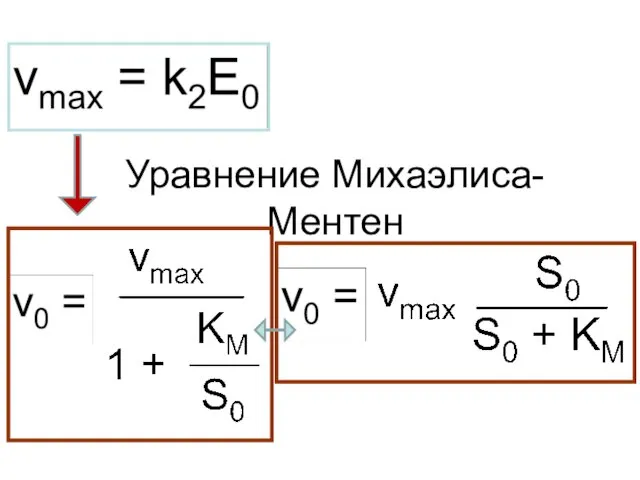
- 5. Уравнение Михаэлиса-Ментен
- 7. [S] Vmax V = Vmax ────── V = ────── [S] + КМ 1 + КМ/[S] Vmax
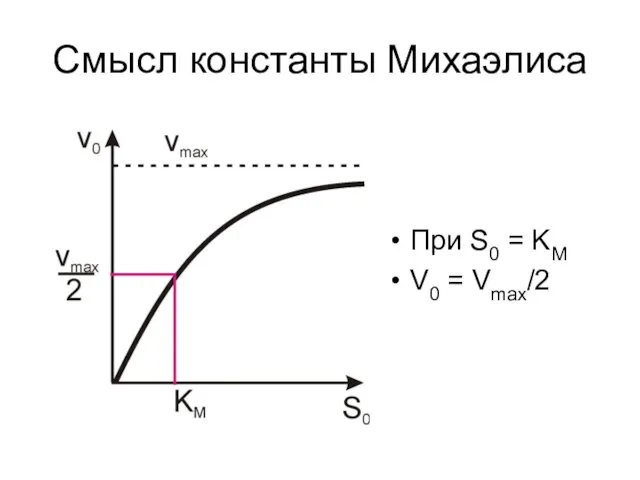
- 8. Смысл константы Михаэлиса При S0 = KM V0 = Vmax/2
- 9. [S] Vmax V = Vmax ────── V = ────── [S] + КМ 1 + КМ/[S] Vmax
- 10. Величины КМ для различных ферментов -6 -7 -4
- 11. Величины k2 для различных ферментов Фермент Vmax = k2[E]o
- 12. График Лайнуивера – Берка , График Иди-Хофсти [S] Vmax V = Vmax ────── V = ──────
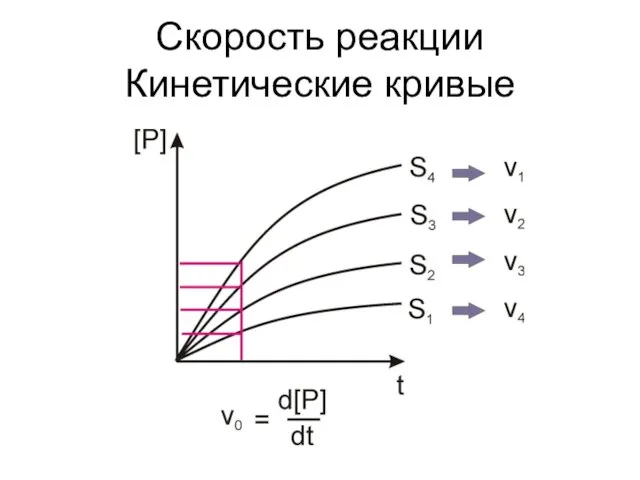
- 13. Скорость реакции Кинетические кривые
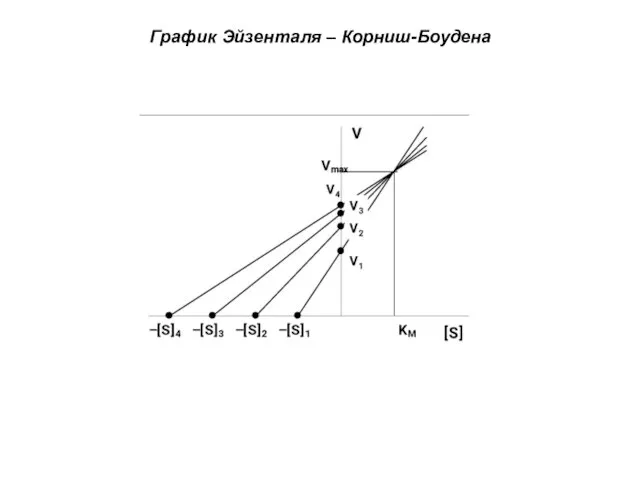
- 14. График Эйзенталя – Корниш-Боудена
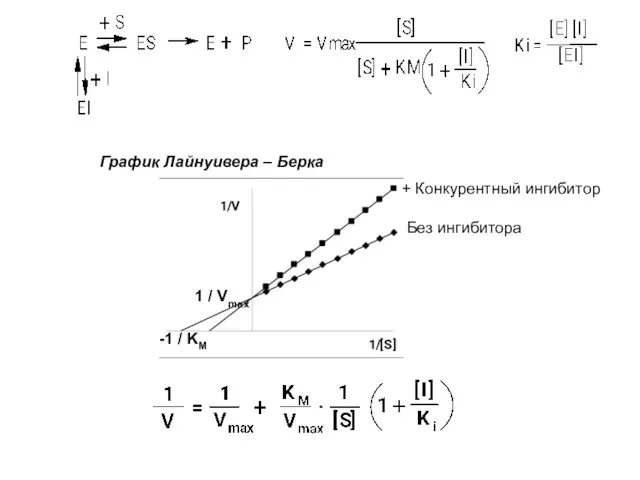
- 16. + Конкурентный ингибитор Без ингибитора График Лайнуивера – Берка -1 / KM 1 / Vmax
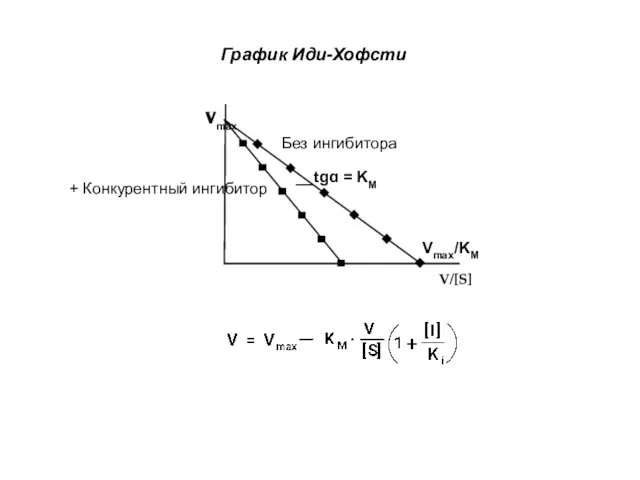
- 17. График Иди-Хофсти Без ингибитора + Конкурентный ингибитор Vmax __tgɑ = KM Vmax/KM
- 18. График Лайнуивера – Берка + Неконкурентный ингибитор Без ингибитора -1 / KM 1 / Vmax
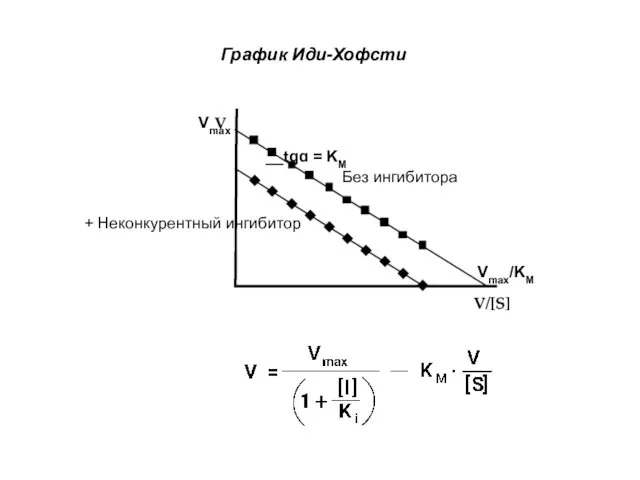
- 19. График Иди-Хофсти Без ингибитора + Неконкурентный ингибитор Vmax __tgɑ = KM Vmax/KM
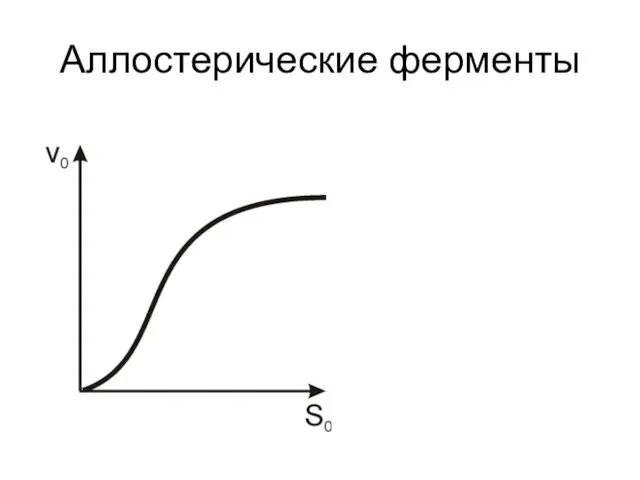
- 20. Аллостерические ферменты
- 21. КЛАССЫ ФЕРМЕНТОВ Оксидоредуктазы Трансферазы Гидролазы Лиазы Изомеразы Синтетазы (лигазы) Транслоказы
- 22. Классификация ферментативных реакций IUBMB, International Union of Biochemistry and Molecular Biology EC – Enzyme Classification КФ
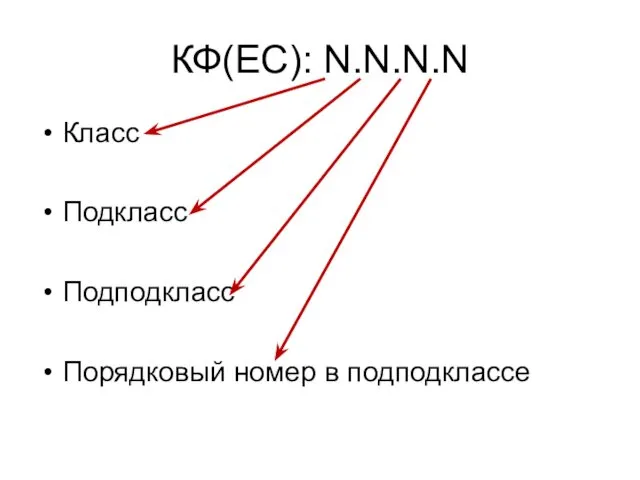
- 23. КФ(EC): N.N.N.N Класс Подкласс Подподкласс Порядковый номер в подподклассе
- 24. КЛАССЫ ФЕРМЕНТОВ Оксидоредуктазы Трансферазы Гидролазы Лиазы Изомеразы Синтетазы (лигазы) Транслоказы
- 25. 1. Оксидоредуктазы Ферменты, катализирующие окислительно-восстановительные реакции Подклассы – донор электронов Подподклассы – акцептор электронов
- 26. Подклассы оксидоредуктаз, действующие на доноры: 1. CH-OH группу 2. альдегидную или оксогруппу 3. CH-CH группу 4.
- 27. 1. Оксидоредуктазы (25 подклассов) Подкласс 1: Действующие на CH-OH группу донора (8 подподклассов) Подподкласс 1: NAD+
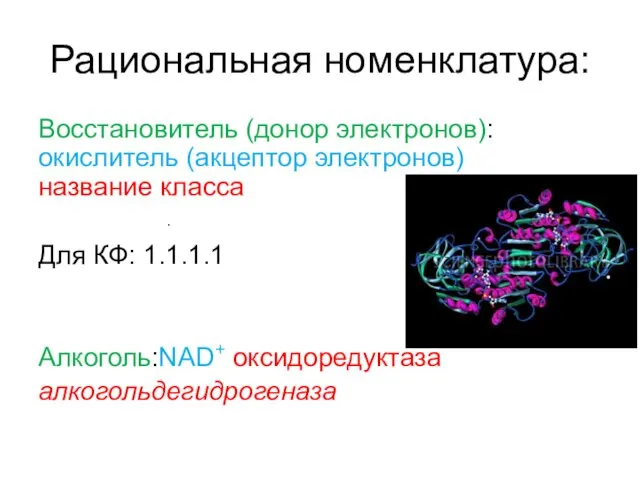
- 28. Рациональная номенклатура: Восстановитель (донор электронов): окислитель (акцептор электронов) название класса Для КФ: 1.1.1.1 Алкоголь:NAD+ оксидоредуктаза алкогольдегидрогеназа
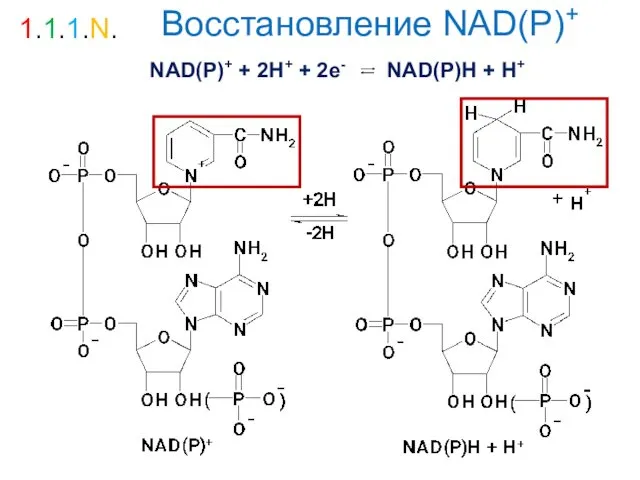
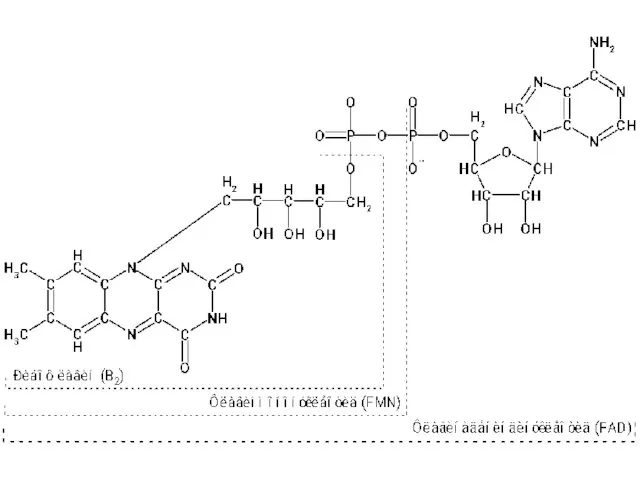
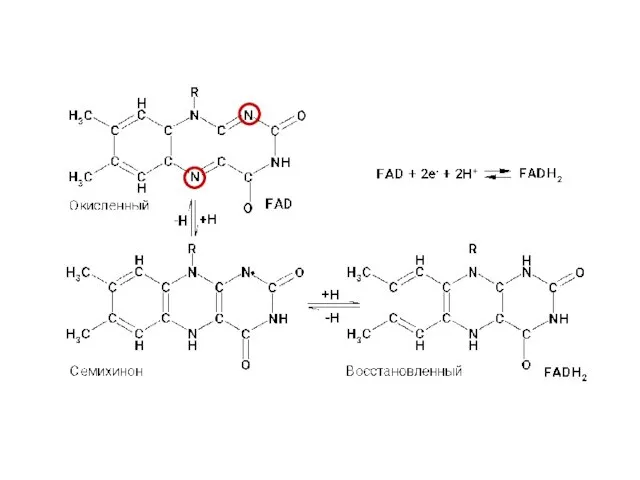
- 29. Восстановление NAD(P)+ 1.1.1.N. NAD(Р)+ + 2Н+ + 2е- NAD(Р)Н + Н+
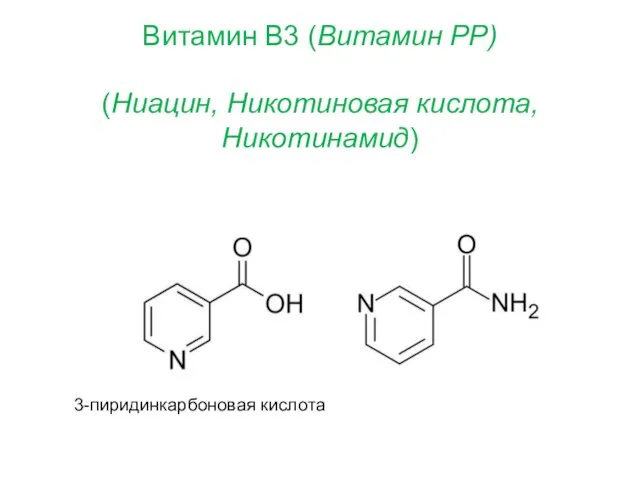
- 30. Витамин B3 (Витамин PP) (Ниацин, Никотиновая кислота, Никотинамид) 3-пиридинкарбоновая кислота
- 31. 1.1.3.4. Глюкозооксидаза Подкласс 1: Действующие на CH-OH группу донора Подподкласс 3: O2 в качестве акцептора Флавопротеин
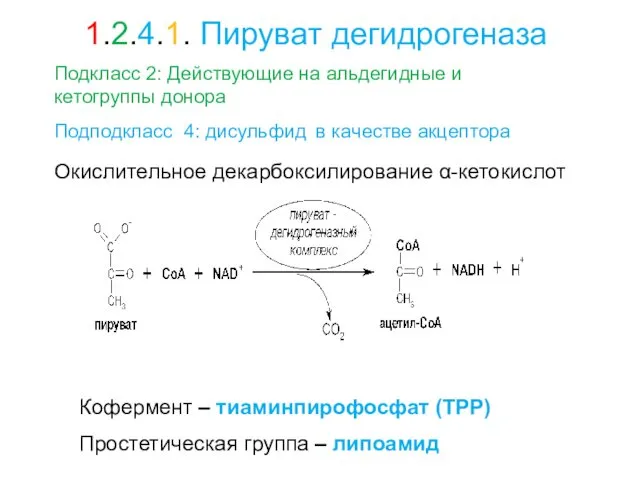
- 34. Окислительное декарбоксилирование α-кетокислот Кофермент – тиаминпирофосфат (ТРР) Простетическая группа – липоамид Подкласс 2: Действующие на альдегидные
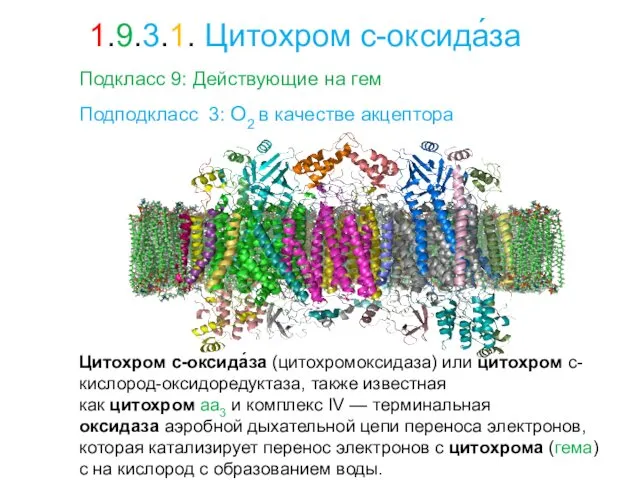
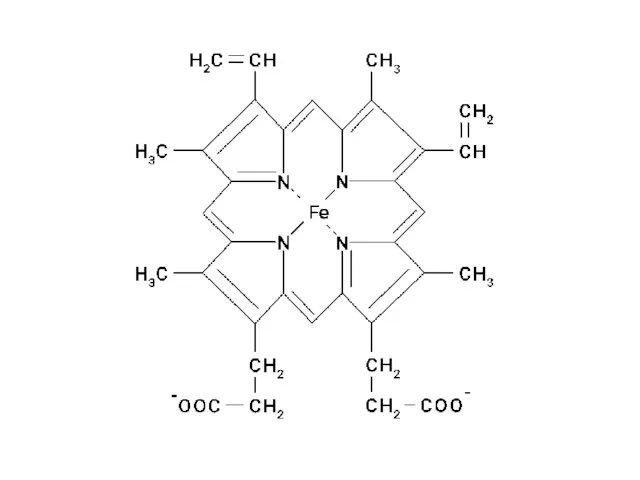
- 35. Цитохром с-оксида́за (цитохромоксидаза) или цитохром с-кислород-оксидоредуктаза, также известная как цитохром aa3 и комплекс IV — терминальная
- 36. 1.11.1.6. Каталаза Гем-содержащий фермент 2 H2O2 = O2 + 2 H2O Рациональное название пероксид водорода:пероксид водорода
- 39. Скачать презентацию




![[S] Vmax V = Vmax ────── V = ────── [S]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/78618/slide-6.jpg)
![[S] Vmax V = Vmax ────── V = ────── [S]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/78618/slide-8.jpg)

![Величины k2 для различных ферментов Фермент Vmax = k2[E]o](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/78618/slide-10.jpg)
![График Лайнуивера – Берка , График Иди-Хофсти [S] Vmax V](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/78618/slide-11.jpg)









 Конспект урока и презентация Почитай родителей
Конспект урока и презентация Почитай родителей Заболевания печени
Заболевания печени Тревожные дети тревожных родителей
Тревожные дети тревожных родителей Ароматерапія – медицина майбутнього
Ароматерапія – медицина майбутнього Становление христианства и развитие больничного дела
Становление христианства и развитие больничного дела Логопедическая работа с учащимися 1 классов.
Логопедическая работа с учащимися 1 классов. Работа ученицы Первая железная дорога
Работа ученицы Первая железная дорога Элементы дизайна
Элементы дизайна Методы обеспечения финансовой безопасности предприятий отрасли дорожного строительства
Методы обеспечения финансовой безопасности предприятий отрасли дорожного строительства заявка на семинар
заявка на семинар Будь осторожен с огнём!
Будь осторожен с огнём! Culture and International Public Relations
Culture and International Public Relations Комплексные методы управления качеством
Комплексные методы управления качеством Бюджет МО Южно-Приморский на 2019 год и плановый период 2020 и 2021 годов
Бюджет МО Южно-Приморский на 2019 год и плановый период 2020 и 2021 годов Ряд Фурье и интеграл Фурье
Ряд Фурье и интеграл Фурье Шаблон. Руководство по использованию фирменного стиля администрации города Ноябрьска
Шаблон. Руководство по использованию фирменного стиля администрации города Ноябрьска Телефон доверия для детей и подростков, и их родителей
Телефон доверия для детей и подростков, и их родителей Робототехника в нашей жизни
Робототехника в нашей жизни sohrani_moyu_i_svoyu_zhizn
sohrani_moyu_i_svoyu_zhizn Выводы логики высказываний (2)
Выводы логики высказываний (2) Составляющие и функции операционной системы Linux
Составляющие и функции операционной системы Linux золотая хохлома
золотая хохлома Перекрытия и полы малоэтажных зданий
Перекрытия и полы малоэтажных зданий Поздравление с Днем рождения
Поздравление с Днем рождения Единицы времени 2. Календарь. 2 класс
Единицы времени 2. Календарь. 2 класс Круглый стол на тему Наркомания и СПИД: сущность и проблема (методика проведения вебинара)
Круглый стол на тему Наркомания и СПИД: сущность и проблема (методика проведения вебинара) Термообработка деревянного реквизита
Термообработка деревянного реквизита Характеристики позиционных систем счисления
Характеристики позиционных систем счисления