Слайд 2

Слайд 3
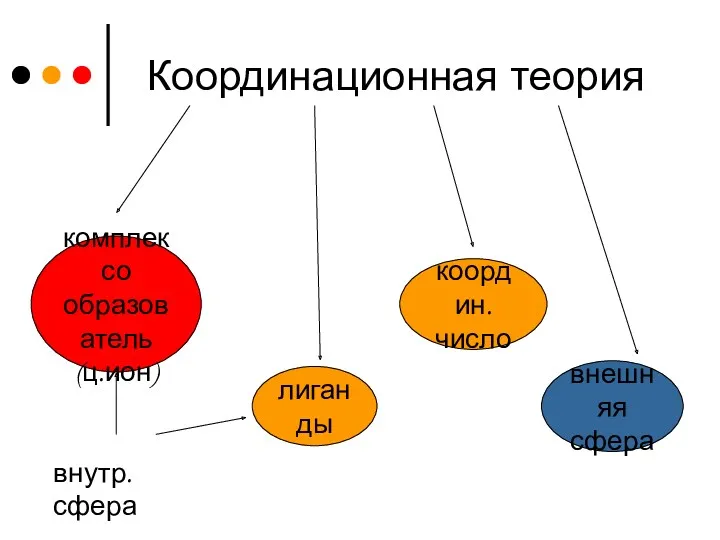
Координационная теория
комплексо
образователь
(ц.ион)
лиганды
координ.
число
внешняя
сфера
внутр.сфера
Слайд 4
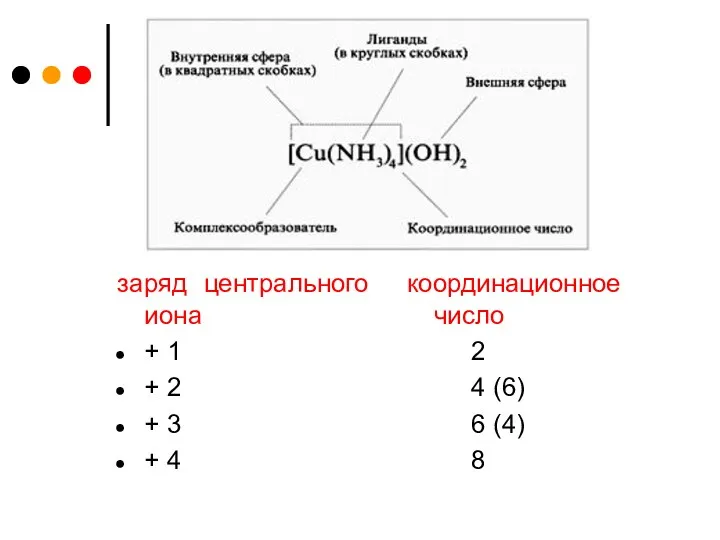
заряд центрального иона
+ 1
+ 2
+ 3
+ 4
координационное число
2
4
(6)
6 (4)
8
Слайд 5
![Типы комплексных соединений CuSO4·5H2O [Cu(NH3)4]SO4 K2[Zn(OH)4] AlCl3·6H2O [Co(NH3)6]Cl3 K4[Fe(CN)6] аквакомплексы](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/483401/slide-4.jpg)
Типы комплексных соединений
CuSO4·5H2O [Cu(NH3)4]SO4 K2[Zn(OH)4]
AlCl3·6H2O [Co(NH3)6]Cl3 K4[Fe(CN)6]
аквакомплексы
аммиакаты
ацидокомплексы
лиганды – Н2О
лиганды – NH3
лиганды
- анионы
Слайд 6
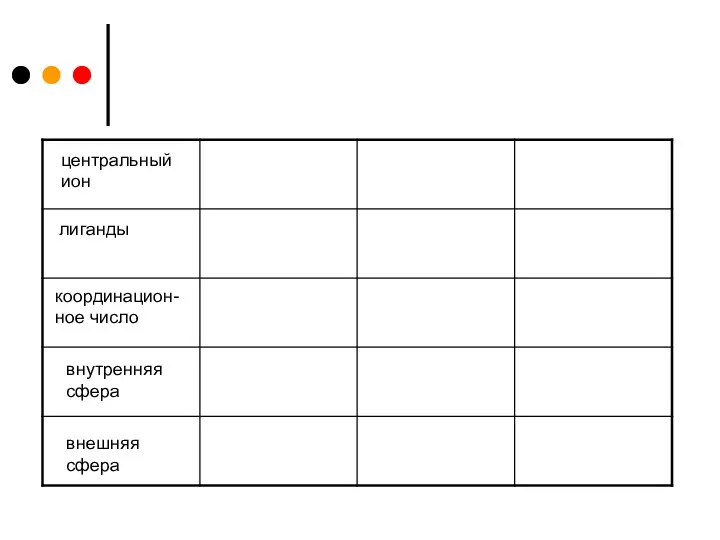
центральный
ион
лиганды
координацион-
ное число
внутренняя
сфера
внешняя
сфера
Слайд 7

номенклатура
внутренняя сфера – катион (+)
хлорид гексаакважелеза (3+)
сульфат тетраамминмеди (2+)
внутренняя сфера –
анион (-)
гексацианофер-рат (2+) калия
тетрагидроксо-алюминат калия
Слайд 8
![Назвать и объяснить с точки зрения координационной теории K2[Co(CNS)4] Тетрароданокобальтат](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/483401/slide-7.jpg)
Назвать и объяснить с точки зрения координационной теории K2[Co(CNS)4]
Тетрароданокобальтат (2+) калия
Комплексообразователь
Лиганды
Координационное
число
Внутренняя сфера
Внешняя сфера
Co2+
CNS-
4
[Co(CNS)4]2-
K+
Слайд 9
![[Ag(NH3)2]OH, K3[Fe(CN)6] Реакция «серебряного зеркала» R – CH = O](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/483401/slide-8.jpg)
[Ag(NH3)2]OH, K3[Fe(CN)6]
Реакция «серебряного зеркала»
R – CH = O + 2[Ag(NH3)2]OH
R – COOH + 2Ag + H2O + 4NH3
Доказательство амфотерности гидроксида
KOH + Al(OH)3 K[Al(OH)4]
Качественный анализ
4FeCl3 + 3K4[Fe(CN)6]
12KCl + Fe4[Fe(CN)6]3



![Типы комплексных соединений CuSO4·5H2O [Cu(NH3)4]SO4 K2[Zn(OH)4] AlCl3·6H2O [Co(NH3)6]Cl3 K4[Fe(CN)6] аквакомплексы](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/483401/slide-4.jpg)


![Назвать и объяснить с точки зрения координационной теории K2[Co(CNS)4] Тетрароданокобальтат](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/483401/slide-7.jpg)
![[Ag(NH3)2]OH, K3[Fe(CN)6] Реакция «серебряного зеркала» R – CH = O](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/483401/slide-8.jpg)
 Международный день борьбы с наркоманией
Международный день борьбы с наркоманией Презентация к статье Трудности формирования чтения у младших школьников
Презентация к статье Трудности формирования чтения у младших школьников Типы крыш
Типы крыш Тез үдемелі гломерулонефрит
Тез үдемелі гломерулонефрит 2_Пед.процес. Средства и методы (1)
2_Пед.процес. Средства и методы (1) Вопросы государственного и военного строительства РФ. Вооруженные Силы России в Структуре государственных институтов
Вопросы государственного и военного строительства РФ. Вооруженные Силы России в Структуре государственных институтов Социальная стратификация в современной России
Социальная стратификация в современной России Новый шаблон для процедуры аттестации
Новый шаблон для процедуры аттестации Владимир Владимирович Маяковский (1893-1930)
Владимир Владимирович Маяковский (1893-1930) Угловые характеристики синхронного генератора
Угловые характеристики синхронного генератора Manual QA course. Виды тестирования
Manual QA course. Виды тестирования Памятка Подвижные игры
Памятка Подвижные игры Вяжущие вещества. Порошкообразные вещества
Вяжущие вещества. Порошкообразные вещества Система канализации
Система канализации Презентация по теме Природа в опасности
Презентация по теме Природа в опасности Управление электроприводами выключателей и разъединителей
Управление электроприводами выключателей и разъединителей Площадь поверхности цилиндра
Площадь поверхности цилиндра Degrees of comparison
Degrees of comparison Мастер-класс Подкова на счастье
Мастер-класс Подкова на счастье Презентация Герои Курской дуги
Презентация Герои Курской дуги Гормоны гипофиза
Гормоны гипофиза Устройства ввода информации в ПК. Сканеры. Виды. Характеристика
Устройства ввода информации в ПК. Сканеры. Виды. Характеристика Shoppingsherlock
Shoppingsherlock Среда обитания живых организмов. 5 класс. Диск
Среда обитания живых организмов. 5 класс. Диск Проект Путешествие капельки
Проект Путешествие капельки Современная мировая экономика
Современная мировая экономика Основные технологические особенности ПГП
Основные технологические особенности ПГП Строитель своей души
Строитель своей души