Содержание
- 2. Общие свойства металлов обусловлены: - Строением атома - Наличием кристаллической решетки - Наличием металлической связи
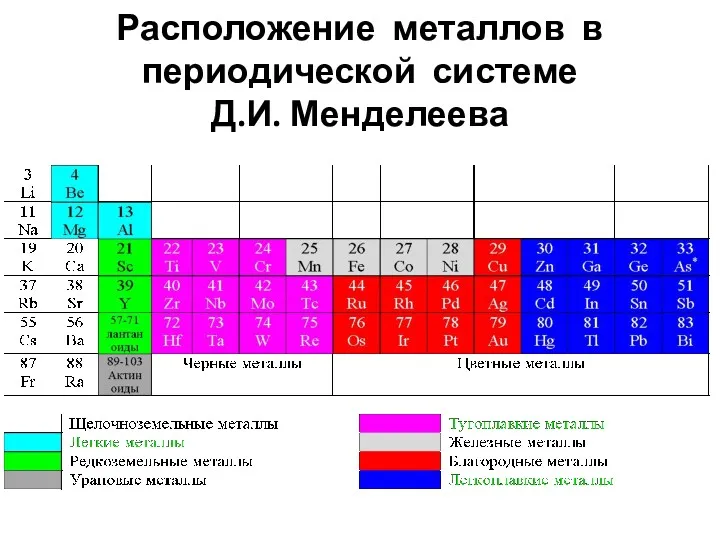
- 3. Расположение металлов в периодической системе Д.И. Менделеева
- 4. s-металлы: элементы IA и IIA групп. Свойства s-металлов: – постоянные валентности или степени окисления (+1 и
- 5. p-металлы: элементы IIIA (кроме бора B), IVA (германий Ge, олово Sn, свинец Pb) и VA (сурьма
- 6. d-металлы: 30 элементов, расположенных в серединах периодов (IV, V, VI, VII) и достраивающих d-подуровень предпоследнего слоя
- 7. f-металлы: лантаноиды и актиноиды. У этих элементов достраиваются энергетические подуровни 4f и 5f при заполненном внешнем
- 8. Черные металлы Черные металлы характеризуются темно-серым цветом, большой плотностью (кроме щелочноземельных Ме), высокой температурой плавления, относительно
- 9. Черные подразделяются: Железные металлы - Fe, Co, Ni (ферромагнетики) и Mn. Тугоплавкие металлы - температура плавления
- 10. Цветные металлы Цветные металлы характеризуются: характерной окраской (красная, желтая, белая), большой пластичностью, низкой температурой плавления, отсутствием
- 11. Цветные подразделяются: Легкие металлы - Be, Mg, Al - малая плотность. Благородные металлы - Ag, Au,
- 12. Нахождение металлов в природе В самородном состоянии: Cu, Ag, Hg, Pt, Au В виде соединений: оксидные
- 13. Кристаллические структуры металлов 1. Объемноцентрированная кубическая решетка (ОЦК) (Na, K, α-Fe, δ-Fe, V, Cr, Mo, W)
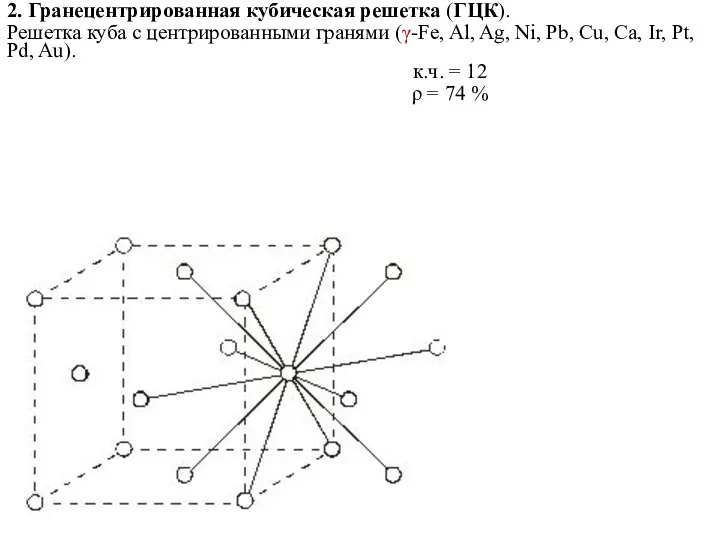
- 14. 2. Гранецентрированная кубическая решетка (ГЦК). Решетка куба с центрированными гранями (γ-Fe, Al, Ag, Ni, Pb, Cu,
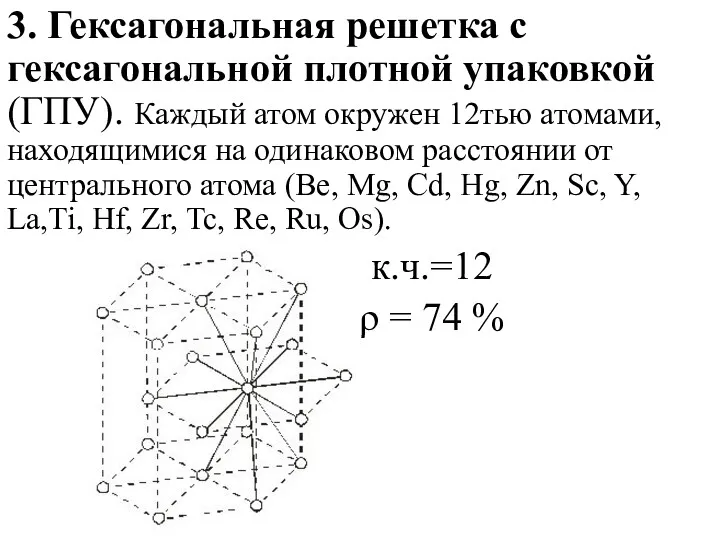
- 15. 3. Гексагональная решетка с гексагональной плотной упаковкой (ГПУ). Каждый атом окружен 12тью атомами, находящимися на одинаковом
- 16. Полиморфизм α – модификация устойчива при сравнительно низких температурах, β – устойчива при более высоких температурах.
- 17. Физические свойства металлов 1. Твердость (кроме Hg) Самый твердый Cr. Самые мягкие – щелочные. 3. Температура
- 18. 4. Плотность От 0,53 Li до 22,5 г/см3 Os ρ ρ > 5 г/см3 – тяжелые
- 19. 6. Магнитные свойства a) Диамагнитные (в основном амфотерные Ме: Be,Zn,Ga,Ge) б) Парамагнитные в) Ферромагнитные (Fe, Co,
- 20. Получение металлов Пирометаллургия Восстановители: уголь, оксида углерода (II) или водород. — С или СО ZnО +
- 21. — Сульфидные руды 2ZnS + 3О2 = 2ZnО + 2SО2 ZnО + С = СО +
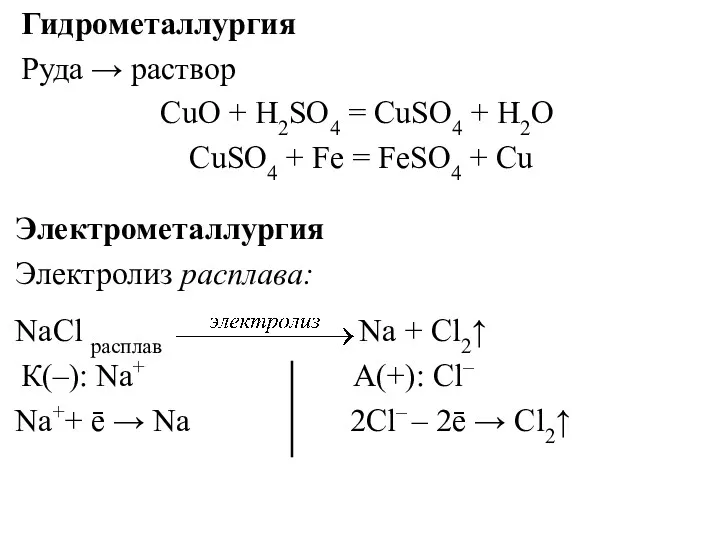
- 22. Гидрометаллургия Руда → раствор CuO + Н2SО4 = CuSО4 + Н2О CuSО4 + Fe = FeSO4
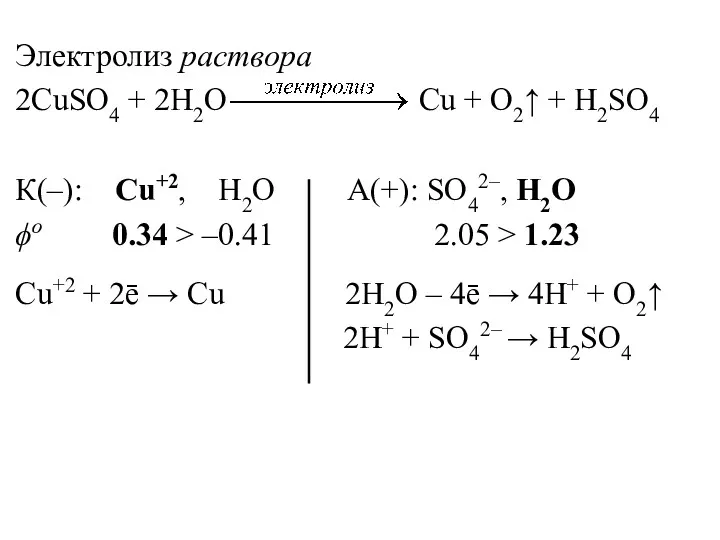
- 23. Электролиз раствора 2CuSO4 + 2H2O Cu + O2↑ + H2SO4 К(–): Cu+2, H2O А(+): SO42–, H2O
- 24. ПОЛУЧЕНИЕ МЕТАЛЛОВ ВЫСОКОЙ ЧАСТОТЫ 1. Электролитическое рафинирование (Ag, Cu, Fe, Ni, Pb) 2. Перегонка и переплавка
- 25. 3. Химические транспортные реакции Карбонильный способ (Ni, Fe) Ni + 4CO Ni(CO)4 (t = 42°C) тетракарбонил
- 26. 4. Зонная плавка (Ge, W, Mo) до чистоты 10-8 %
- 27. ХИМИЧЕСКИЕ СВОЙСТВА Me ВЗАИМОДЕЙСТВИЕ С ПРОСТЫМИ ВЕЩЕСТВАМИ С кислородом. Все, кроме Pt, Pd, Au. 4Li +
- 28. С водородом. Взаимодействуют щел. и щел.-зем. металлы: Ca (Sr, Ba) + H2 = CaH2 (SrH2, BaH2)
- 29. С серой. 2Ag + S = Ag2S2- сульфид серебра С галогенами. Mg + Cl2 = MgCl21-
- 30. С другими неметаллами. Из металлов I группы с азотом, углеродом, кремнием непосредственно взаимодействует только литий: 6Li
- 31. 2. ВЗАИМОДЕЙСТВИЕ СО СЛОЖНЫМИ ВЕЩЕСТВАМИ С водой. Металлы I группы: Na + H2O = NaOH +
- 32. 2) C кислотами. Все металлы, расположенные в ряду напряжений до водорода вытесняют его из разбавленных кислот,
- 33. 3) Со щелочами. Взаимодействуют амфотерные металлы (Zn, Al, Pb, Sn, Be, Cr(III)). Zn + 2NaOH +
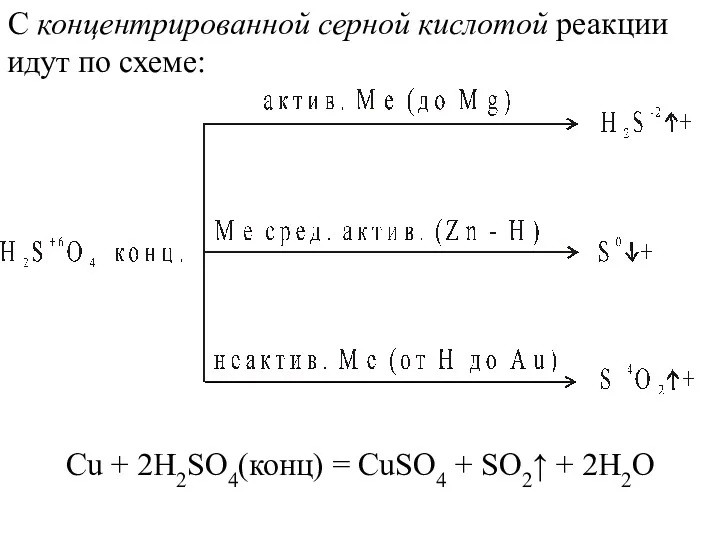
- 34. С концентрированной серной кислотой реакции идут по схеме: Сu + 2Н2SO4(конц) = СuSO4 + SO2↑ +
- 36. Скачать презентацию



























 Игра-презентация по Карточкам Ханса
Игра-презентация по Карточкам Ханса Презентация Углеводороды.
Презентация Углеводороды. Введение в IDE Unity
Введение в IDE Unity Пилотный проект. Город Пермь
Пилотный проект. Город Пермь Условия и срок в гражданско-правовой сделке
Условия и срок в гражданско-правовой сделке Среда обитания живых организмов. 5 класс. Диск
Среда обитания живых организмов. 5 класс. Диск Традиционные и нетрадиционные направления в искусстве в конце 19 - начале 20 в
Традиционные и нетрадиционные направления в искусстве в конце 19 - начале 20 в Многопроцессорные вычислительные системы
Многопроцессорные вычислительные системы Стандарт КП пример- восстановлен
Стандарт КП пример- восстановлен Устройства компьютера
Устройства компьютера Личностно-ориентированные технологии
Личностно-ориентированные технологии Афинские школы
Афинские школы Структура исследовательской работы обучающихся
Структура исследовательской работы обучающихся Портфолио, как способ представления мастера п/о, педагога Камышловского ПУ
Портфолио, как способ представления мастера п/о, педагога Камышловского ПУ Линейный список. Двусвязный список
Линейный список. Двусвязный список Герман Гессе 1877-1962
Герман Гессе 1877-1962 Классификация систем разработки. Разработка месторождений на естественном режиме и с ППД. (Лекция 4)
Классификация систем разработки. Разработка месторождений на естественном режиме и с ППД. (Лекция 4) Вредные привычки. Курение. Алкоголизм. Наркомания
Вредные привычки. Курение. Алкоголизм. Наркомания Изменения в гражданский кодекс Российской Федерации. Законопроект № 47538-6
Изменения в гражданский кодекс Российской Федерации. Законопроект № 47538-6 Особенности сестринского ухода в психиатрии и наркологии. Организация психиатрической помощи в РФ
Особенности сестринского ухода в психиатрии и наркологии. Организация психиатрической помощи в РФ Обязанности водителя
Обязанности водителя Тема:Ознакомление детей с окружающей действительностью – как средство воспитания патриотизма у детей дошкольного возраста
Тема:Ознакомление детей с окружающей действительностью – как средство воспитания патриотизма у детей дошкольного возраста Система научной литературы. Типы и виды научных документов
Система научной литературы. Типы и виды научных документов 20231022_prezentatsiya1_0
20231022_prezentatsiya1_0 Презентация Как полюбить чтение?
Презентация Как полюбить чтение? Сотовая связь
Сотовая связь Конспект урока по теме: Кислород
Конспект урока по теме: Кислород Безопасное поведение летом.
Безопасное поведение летом.