Методическая разработка урока химии для 9 класса в соответствии с требованиями ФГОС второго поколения.Тема:Предельные углеводороды(мультимедийное сопровождение) презентация
Содержание
- 2. ЦЕЛЬ УРОКА ФОРМИРОВАНИЕ НОВЫХ ЗНАНИЙ И УМЕНИЙ
- 3. Сегодня на уроке Вы закрепите знания о sp 3 - гибридном состоянии углерода. Вы познакомитесь с
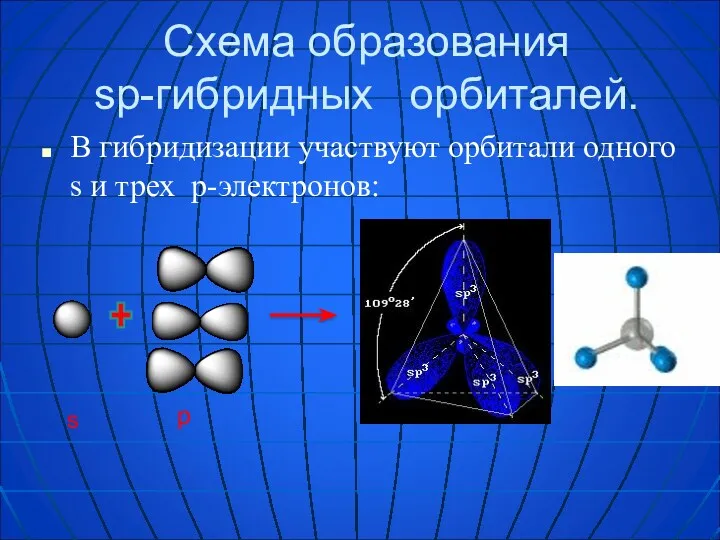
- 4. Схема образования sp-гибридных орбиталей. В гибридизации участвуют орбитали одного s и трех p-электронов: s p
- 5. Гомологический ряд алканов Метан Этан Пропан Бутан Пентан Гексан Гептан Октан Нонан Декан CH4 C2H6 C3H8
- 6. Радикалы - заместители Правила номенклатуры ИЮПАК по принципу замещения, где заместители – радикалы. Их названия формируются
- 7. Понятие об алканах. Алканы – углеводороды, содержащие в молекуле одинарные связи между атомами углерода, а качественный
- 8. Характеристика одинарной связи (С ─ С) в н – алканах. Вид гибридизации атома С – Валентный
- 9. Изомерия алканов Для алканов возможна изомерия: Структурная изомерия (углеродного скелета).
- 10. Правила формирования названия.( на примерах) 1) Выбор главной цепи 2) Нумерация атомов главной цепи, учитывая: а)
- 11. Примеры изомеров. 1 2 3 4 3 4 5 6 А) CH3 - CH- CH2- CH3
- 12. Физические свойства алканов. Алканы плохо растворимы в воде. С – С4 газы С5 – С15 жидкости
- 13. Химические свойства алканов. Предельные углеводороды (алканы) – химически неактивные вещества. Они не реагируют с кислотами, основаниями,
- 14. Типы химических реакций, которые характерны для алканов. 1) Реакции замещения. 2) Реакции изомеризации. 3) Реакции разложения.
- 15. Реакции замещения. Реагируют с хлором (реакция галогенирования) по цепному механизму при УФ – облучении или при
- 16. Алканы могут вступать в реакции изомеризации. СH3 (СH2 )6СH3 → СH3 СH(СH2 )4СH3 + СH3СHСH2СH2СH СH3
- 17. Реакции разложения. При нагревании алканов до 450-5500 С происходит расщепление сложных молекул на более простые (
- 18. Реакция разложения При повышении температуры до 550-6500 С происходит более глубокое расщепление – пиролиз. В результате
- 19. Получение синтез-газа. а) взаимодействием СH4 с водой; СH4 +H2O → СO+3H2 синтез-газ б) взаимодействием СH4 с
- 20. Горение алканов. СH4 + 2О 2 = СО 2 + 2H 2О + 880 кДж Алканы
- 21. Свойства метана. Задание: Определить плюсы и минусы указанных свойств метана при использовании его человеком. Метан –
- 22. Внимание! Пришло сообщение! Нефтяной танкер потерпел крушение, пятно нефти расползается по воде. Нефть подступает к берегу,
- 23. Инструкция по проведению эксперимента. Цель: смоделировать аварию нефтяного танкера и найти решение проблемы; обсудить нравственные стороны
- 24. Определите положительные и отрицательные последствия этого. Результаты обсуждения указать в виде плюса и минуса напротив каждого
- 25. Способ очистки воды от нефти С использованием данных объектов, объяснить действия и последствия (работа в группах):
- 26. Назовите следующие алканы. 1 2 3 4 5 6 а) СН3──СН2 ─ СН2─ СН2─СН2─СН3 СН3 1
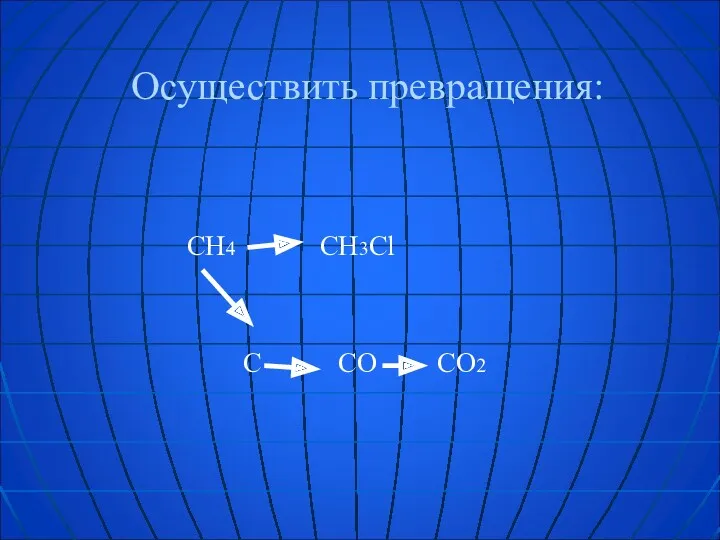
- 27. Осуществить превращения: CH4 CH3Cl C CО CО2
- 28. Решите задачу. Найдите формулу алкана, если его плотность по водороду равна 22. Постройте его структурную формулу,
- 30. Скачать презентацию

























 ОРКСЭ Урок по теме: Душа
ОРКСЭ Урок по теме: Душа Знаменитые иконописцы
Знаменитые иконописцы HLA жүйесі, құрылысы, қызметтері. Трансплантациялық иммунитет
HLA жүйесі, құрылысы, қызметтері. Трансплантациялық иммунитет Самоуправление в Латвии. Краткая программа
Самоуправление в Латвии. Краткая программа Формование металлов
Формование металлов Юридические лица как субъекты МЧП
Юридические лица как субъекты МЧП Внеклассное мероприятие по математике
Внеклассное мероприятие по математике О чём говорит музыка? Немецкий композитор Людвиг Бетховен
О чём говорит музыка? Немецкий композитор Людвиг Бетховен Полупроводниковые диоды: классификация, свойства, применение
Полупроводниковые диоды: классификация, свойства, применение Управление кредитным риском в коммерческом банке
Управление кредитным риском в коммерческом банке Дорожные знаки
Дорожные знаки Технология виртуальной реальности для создания программы реабилитации пациентов с хроническим нарушением сознания
Технология виртуальной реальности для создания программы реабилитации пациентов с хроническим нарушением сознания Зарядка. Вытягивания
Зарядка. Вытягивания Презентация Объем для 11АБ на 1.03
Презентация Объем для 11АБ на 1.03 Розрахунок економічної ефективності автоматизації процесу безперервного зволоження зерна
Розрахунок економічної ефективності автоматизації процесу безперервного зволоження зерна Презентация Знаменитые деятели науки и культуры Тамбовского края
Презентация Знаменитые деятели науки и культуры Тамбовского края Здоровьесберегающие технологии на уроках в начальной школе
Здоровьесберегающие технологии на уроках в начальной школе Биография Максима Горького
Биография Максима Горького Идейное предложение. Brand New Group
Идейное предложение. Brand New Group Анализ аудитории
Анализ аудитории Самостійна робота студента
Самостійна робота студента Зимний олимпийский вид спорта – лыжный спорт
Зимний олимпийский вид спорта – лыжный спорт Instagram. Как создать и продвинуть бренд с нуля
Instagram. Как создать и продвинуть бренд с нуля Строение, свойства и методы испытаний металлов и сплавов
Строение, свойства и методы испытаний металлов и сплавов Шепталка Правописание Н – НН в суффиксах прилагательных
Шепталка Правописание Н – НН в суффиксах прилагательных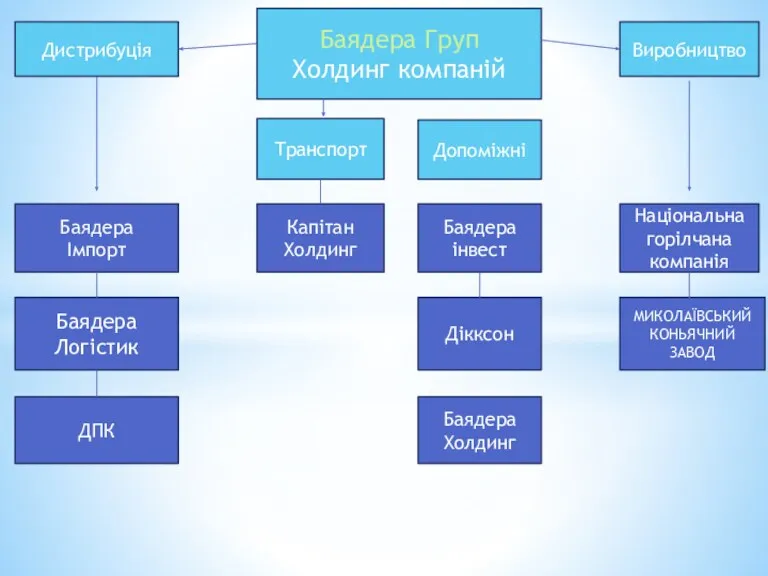 Дистрибуція Баядера Груп Холдинг компаній
Дистрибуція Баядера Груп Холдинг компаній Профессии
Профессии Unconventional hydrocarbons
Unconventional hydrocarbons