Слайд 2

Основные термины занятия (часть 2)
Качественный и количественный состав молекулы - Qualitative
and quantitative composition of the molecule
относительная молекулярная масса - relative molecular mass
Массовая доля элемента - Mass fraction of element
Молекулярное строение - molecular structure
Фтор - fluorine, хлор - chlorine, азот - nitrogen, кислород — oxygen
Железо- iron, медь - copper , натрий — sodium
Благородные газы - Noble gas
Ксенон, неон, аргон - Xenon, neon, argon
Аллотропия - allotropy
Аллотропные модификации - Allotropic modifications
Слайд 3

Основные термины занятия (часть 3)
Явление - effect
Образование нескольких веществ - The
formation of several substances
Разные — different
Свойства — properties
Способность атома присоединять определенное число атомов - The ability of an atom to add a certain number of atoms
Химическая связь - chemical bond
Постоянная валентность - Constant valence
Переменная валентность - Variable valency
Щелочные металлы - Alkali metal
Наименьшее общее кратное - lowest common multiple
Бинарные соединения - Binary compounds
Углерод - carbon
Слайд 4

Основные термины занятия (часть 4)
Число частиц - The number of particles
Количество вещества - Amount of substance
Глюкоза - glucose
Формула для расчета числа молекул - The formula to calculate the number of molecules
Слайд 5

План занятия:
Часть I
Молекулы. Химические формулы. Молекулярные массы.
Простые и сложные вещества.
Валентность
элементов.
Моль. Молярная масса.
Слайд 6
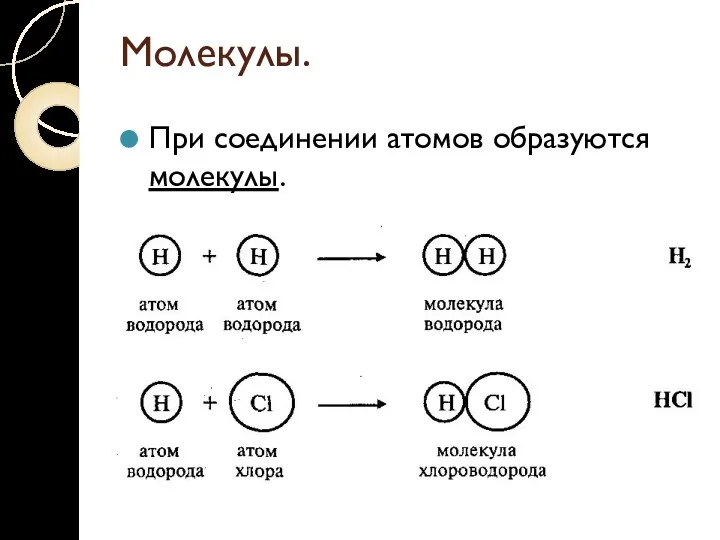
Молекулы.
При соединении атомов образуются молекулы.
Слайд 7

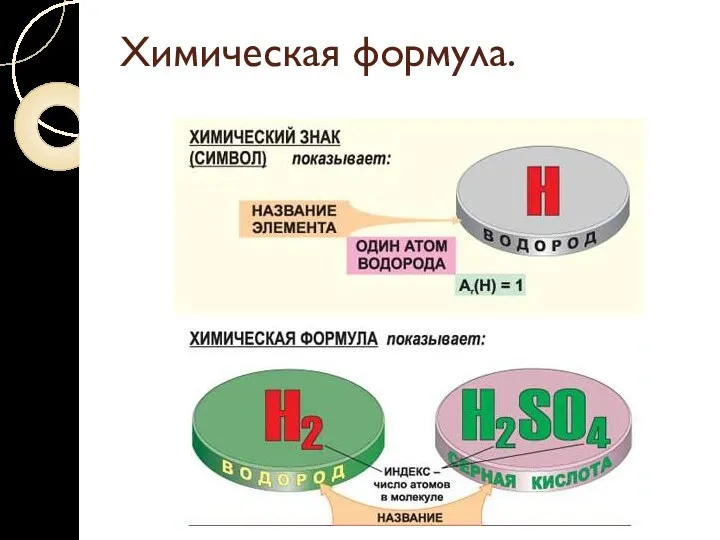
Химическая формула.
Химическая формула - условное обозначение химического состава и структурыи структуры соединенийи структуры соединений с помощью символов
химических элементови структуры соединений с помощью символов химических элементов, числовых и вспомогательных знаков.
Слайд 8

Слайд 9
Слайд 10

Молекулярные массы.
Масса любой молекулы равна сумме образующих ее атомов.
Mr – относительная
молекулярная масса.
Рассчитайте Mr: азотной кислоты, серной кислоты, гидроксида натрия, оксида кальцияоксида фосфора (V), судьфида алюминия.
Слайд 11

Молекулярные массы.
Mr величина безразмерная!
По формуле вещества можно рассчитать массовую долю каждого
химического элемента, который входит в состав вещества.
Слайд 12

Массовая доля химического элемента в веществе.
Слайд 13

Простые и сложные вещества.
Все вещества делятся на простые и сложные.
Простые
Сложные
Слайд 14

Простые и сложные вещества.
Простые вещества имеют:
Молекулярное строение: (фтор, хлор, азот, кислород)
Атомное
строение (железо, медь, натрий)
Или являются благородными газами (ксенон, неон, аргон)
Название простых веществ совпадают с названием элементов!
Слайд 15

Простые и сложные вещества.
Аллотропия – явление образования нескольких простых веществ одним
элементом.
Разные простые вещества, которые образуются одним и тем же химическим элементом, называются аллотропными видоизменениями (модификациями).
Слайд 16
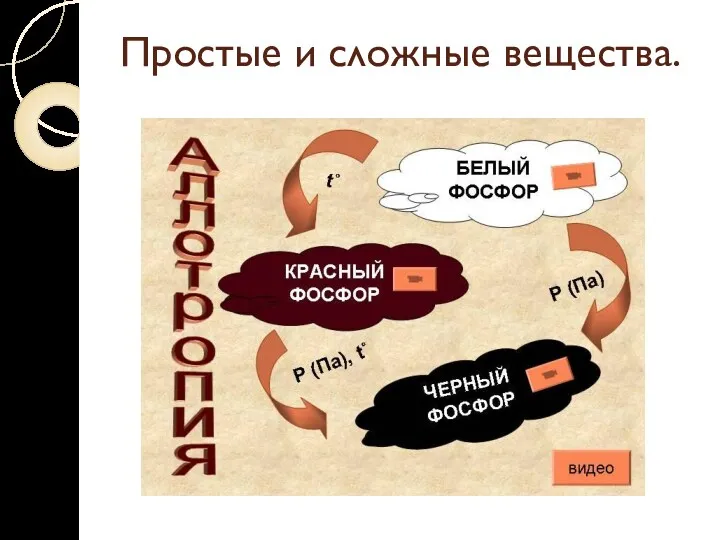
Простые и сложные вещества.
Слайд 17
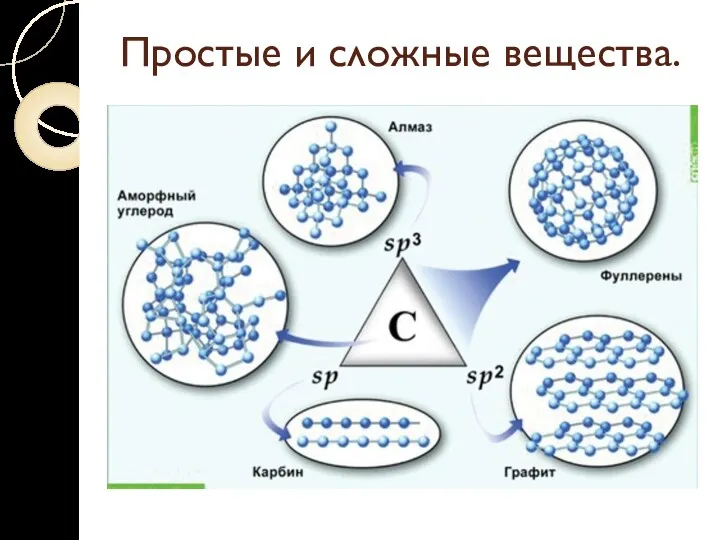
Простые и сложные вещества.
Слайд 18
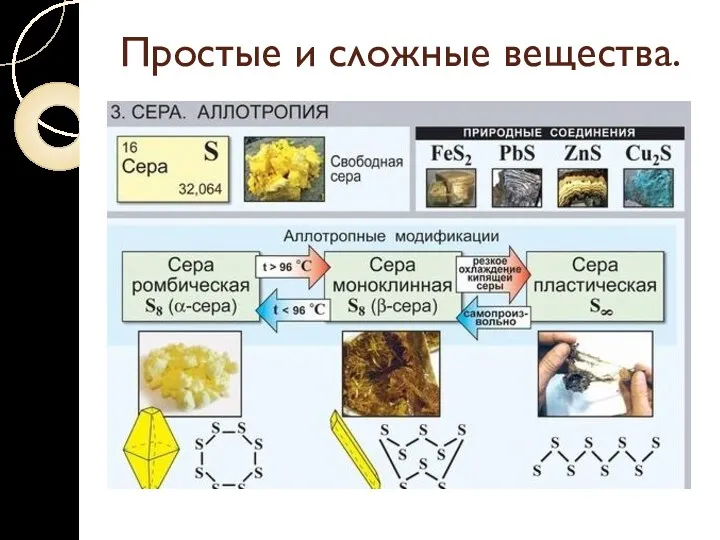
Простые и сложные вещества.
Слайд 19

Простые и сложные вещества.
Сложные вещества.
Слайд 20

Валентность элементов.
Валентность обозначается римскими цифрами:
I, II, III, IV, V, VI,
VII, VIII
Слайд 21

Валентность элементов.
Элементы с постоянной валентностью I:
H, F, щелочные металлы: Li, Na,
K – образуют только одну химическую связь.
Элементы с постоянной валентностью II:
O, Mg, Ca, Sr, Ba, Zn
Элемент с постоянной валентностью III:
Al
Слайд 22

Валентность элементов.
Атомы этих элементов в разных соединениях могут образовывать разное число
химических связей.
Слайд 23

Слайд 24
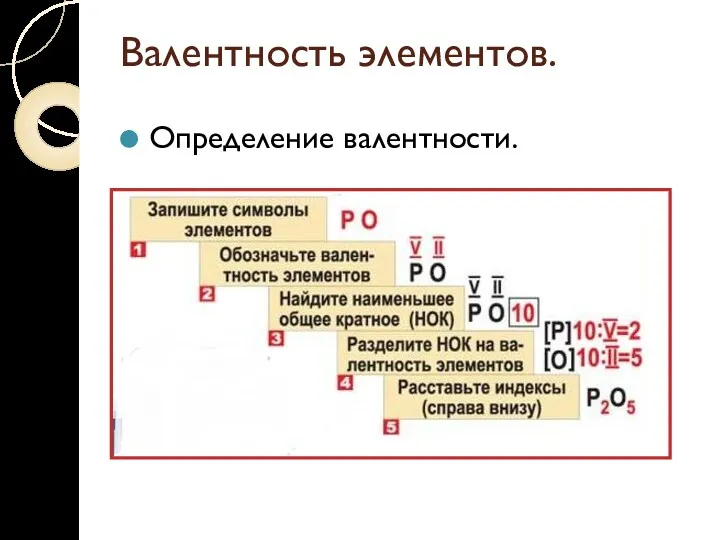
Валентность элементов.
Определение валентности.
Слайд 25

Наименьшее общее кратное (НОК)
Наименьшее общее кратное двух целых чисел m
и n есть наименьшее натуральное число, которое делится на m и n без остатка
Слайд 26

Валентность элементов.
Правило валентности:
Определить валентность элементов в соединениях: PH3, P2O5 ,H2S, SiH4
Слайд 27

Моль. Молярная масса.
Единицей количества вещества является моль.
Аа
Рассчитаем сколько атомов С
содержится в 12г углерода.
Слайд 28
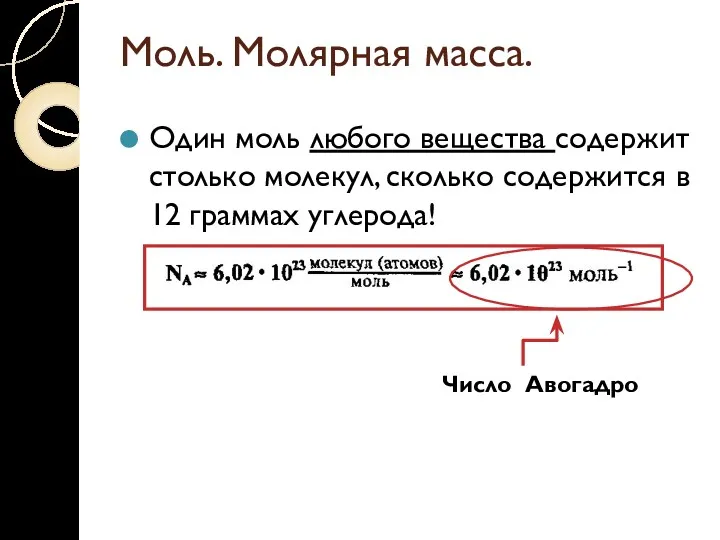
Моль. Молярная масса.
Один моль любого вещества содержит столько молекул, сколько содержится
в 12 граммах углерода!
Число Авогадро
Слайд 29

Моль. Молярная масса.
Если вещество состоит из молекул, то 1 моль это
молекул этого вещества.
Если вещество состоит из атомов, 1 моль это атомов этого вещества.
Следовательно:
Слайд 30

Слайд 31

Моль. Молярная масса.
Задача:
Решение:
Слайд 32

Моль. Молярная масса.
Масса одного моля вещества называется молярной массой.
Молярная масса выражается
в г/моль.
Слайд 33

Моль. Молярная масса.
Определим молярные массы:
Водорода
Глюкозы
Железа
Зная молярную массу вещества М, можно рассчитать
количества вещества (число молей) в любой данной массе вещества:
































 Влияние режимов термообработки на свойства сталей
Влияние режимов термообработки на свойства сталей Технология круговой тренировки
Технология круговой тренировки Компания Subaru
Компания Subaru Основные сословия российского общества в XVI веке: служилые и тяглые
Основные сословия российского общества в XVI веке: служилые и тяглые Система автоматизированного ведения пассажирского тепловоза ТЭП-70 (УСАВП-Т)
Система автоматизированного ведения пассажирского тепловоза ТЭП-70 (УСАВП-Т) Презентация День Победы!
Презентация День Победы! Политические режимы. Недемократические и гибридные режимы. Демократия. Демократизация
Политические режимы. Недемократические и гибридные режимы. Демократия. Демократизация Электронагревательные приборы
Электронагревательные приборы Положение об участии в школьной научно-практической конференции
Положение об участии в школьной научно-практической конференции Система наставничества
Система наставничества Форма и размеры Земли
Форма и размеры Земли Технология термической обработки зубчатого колеса
Технология термической обработки зубчатого колеса Рынок нерудных материалов. Строительные нерудные материалы
Рынок нерудных материалов. Строительные нерудные материалы Среда обитания организмов
Среда обитания организмов Бактерии. Грибы
Бактерии. Грибы Модуль урока Решение задач на вывод молекулярной формулы вещества
Модуль урока Решение задач на вывод молекулярной формулы вещества Религия как одна из форм культуры
Религия как одна из форм культуры Очищувальна зволожувальна емульсія
Очищувальна зволожувальна емульсія строение ат
строение ат Зимняя сказка. Тематическая интерьерная композиция, посвященная Новому году
Зимняя сказка. Тематическая интерьерная композиция, посвященная Новому году Мы выбираем здоровье
Мы выбираем здоровье Беседа с учащимися Какой он, мир, где мне тепло?
Беседа с учащимися Какой он, мир, где мне тепло? Определение места судна с помощью РЛС
Определение места судна с помощью РЛС Республика Чили
Республика Чили Електрифіковані залізниці. Електропостачання залізниць
Електрифіковані залізниці. Електропостачання залізниць презентация Музыкотерапия в коррекционной работе с детьми раннего возраста
презентация Музыкотерапия в коррекционной работе с детьми раннего возраста Лучшим мамам посвящается…
Лучшим мамам посвящается… Презентация к классному часу Памятные места Старого Оскола
Презентация к классному часу Памятные места Старого Оскола