Содержание
- 2. Степень окисления Степень окисления - это условный заряд атома в молекуле, вычисленный в предположении, что молекула
- 3. Расчет степени окисления Для вычисления степени окисления элемента следует учитывать следующие положения: 1. Степени окисления атомов
- 4. Примеры: V2+5O5-2; Na2+1B4+3O7-2; K+1Cl+7O4-2; N-3H3+1; K2+1H+1P+5O4-2; Na2+1Cr2+6O7-2 Степень окисления 3. Алгебраическая сумма степеней окисления всех атомов,
- 5. Реакции без и с изменением степени окисления Существует два типа химических реакций: A Реакции, в которых
- 6. B Реакции, в которых происходит изменение степеней окисления атомов элементов, входящих в состав реагирующих соединений: 2Mg0
- 7. Окисление, восстановление В окислительно-восстановительных реакциях электроны от одних атомов, молекул или ионов переходят к другим. Процесс
- 8. Процесс присоединения электронов – восстановление. При восстановлении степень окисления понижается. Mn+4 + 2ē = Mn+2 S0
- 9. Окислительно-восстановительные свойства вещества и степени окисления входящих в него атомов Соединения, содержащие атомы элементов с максимальной
- 10. Важнейшие восстановители и окислители
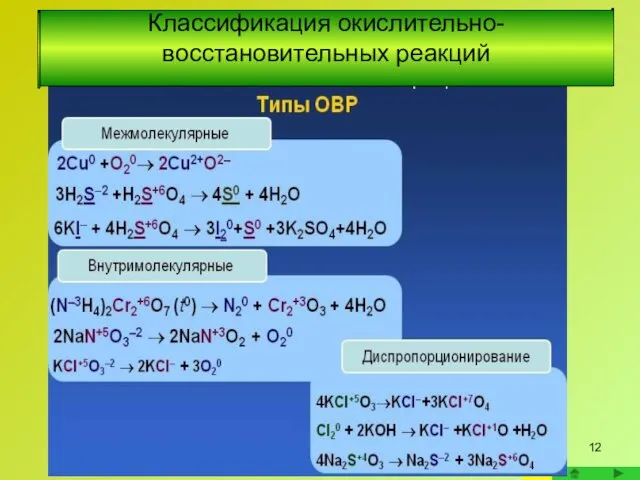
- 12. Классификация окислительно-восстановительных реакций
- 13. Межмолекулярные окислительно-восстановительные реакции Окислитель и восстановитель находятся в разных веществах; обмен электронами в этих реакциях происходит
- 14. Внутримолекулярные окислительно- восстановительные реакции Во внутримолекулярных реакциях окислитель и восстановитель находятся в одной и той же
- 15. Диспропорционирование - окислительно-восстановительная реакция, в которой один элемент одновременно повышает и понижает степень окисления
- 16. Электронный баланс - метод нахождения коэффициентов в уравнениях окислительно-восстановительных реакций, в котором рассматривается обмен электронами между
- 17. Составление уравнений ОВР методом электронного баланса Метод основан на сравнении степеней окисления атомов в исходных веществах
- 18. Составить схему реакции. Определить степени окисления элементов в реагентах и продуктах реакции. Определить, является реакция окислительно-восстановительной
- 19. Составление уравнений окислительно-восстановительных реакций
- 20. B Электронно-ионный баланс (метод полуреакций) - метод нахождения коэффициентов, в котором рассматривается обмен электронами между ионами
- 21. Составление уравнений ОВР методом полуреакций или ионно-электронным методом Метод основан на составлении ионно-электронных уравнений для процессов
- 22. 1.Записываем ионную схему процесса, которая включает только восстановитель и продукт его окисления и окислитель и продукт
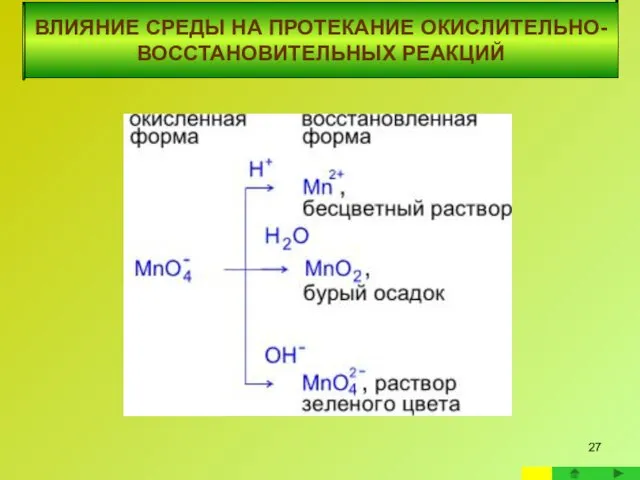
- 23. ВЛИЯНИЕ СРЕДЫ НА ПРОТЕКАНИЕ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ ВЛИЯНИЕ СРЕДЫ НА ПРОТЕКАНИЕ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ
- 24. Реакции с участием перманганата калия в качестве окислителя ВЛИЯНИЕ СРЕДЫ НА ПРОТЕКАНИЕ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ Реакции в
- 25. Реакции в нейтральной среде ВЛИЯНИЕ СРЕДЫ НА ПРОТЕКАНИЕ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ Фиолетовый раствор KMnO4 после окончания реакции
- 26. ВЛИЯНИЕ СРЕДЫ НА ПРОТЕКАНИЕ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ Реакции в щелочной среде В щелочной среде кислород предоставляют ионы
- 27. ВЛИЯНИЕ СРЕДЫ НА ПРОТЕКАНИЕ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ
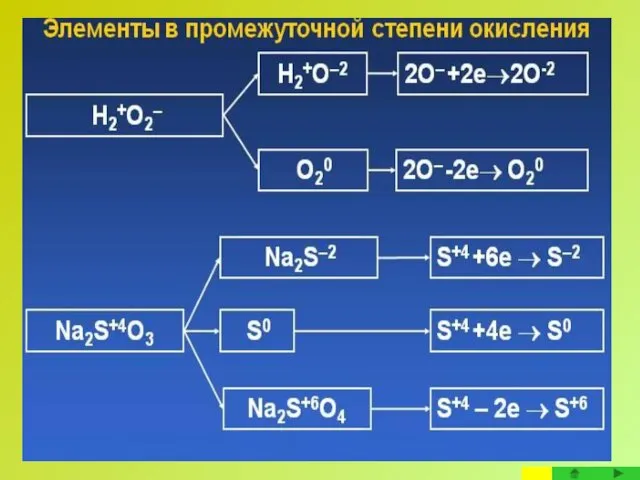
- 28. При взаимодействии веществ, содержащих в своем составе элементы в промежуточных степенях окисления о направлении реакции судят
- 29. Алгоритм действия: По таблице потенциалов определяют потенциалы окислителя и восстановителя Находят их алгебраическую сумму Если Σ
- 30. Возможен ли процесс: Cu + FeCl3 →? + ? Выписывают из справочника все варианты: Cu –
- 32. Скачать презентацию


























 Системы впрыска бензина
Системы впрыска бензина Внеклассное мероприятие Расскажу тебе
Внеклассное мероприятие Расскажу тебе КапиталСтроиПроект. Жилом комплекс по ул. Карпова в Зареченском районе г. Тулы
КапиталСтроиПроект. Жилом комплекс по ул. Карпова в Зареченском районе г. Тулы Тайна имени Илья
Тайна имени Илья Економічне управління підприємством
Економічне управління підприємством Бурильная колонна
Бурильная колонна Литературный глобус С книгой вокруг света
Литературный глобус С книгой вокруг света Всероссийский конкурс для педагогов и учащихся Недаром помнит вся Россия, посвященный 200-летнему юбилею Отечественной войны
Всероссийский конкурс для педагогов и учащихся Недаром помнит вся Россия, посвященный 200-летнему юбилею Отечественной войны Измерение отрезков
Измерение отрезков Роторные Управляемые Системы Power Drive
Роторные Управляемые Системы Power Drive Врожденный нефротический синдром
Врожденный нефротический синдром Конспект и презентация для 1 класса День знаний
Конспект и презентация для 1 класса День знаний презентация Города-герои
презентация Города-герои Философия Новейшего времени и современности
Философия Новейшего времени и современности Центр безопасности Городок Светофорик
Центр безопасности Городок Светофорик Исчезающие виды птиц
Исчезающие виды птиц основы метода ассоциаций
основы метода ассоциаций Управление оборотным капиталом
Управление оборотным капиталом Агропромышленный комплекс. Лёгкая и пищевая промышленность
Агропромышленный комплекс. Лёгкая и пищевая промышленность Портфолио воспитателя детского сада Кирилловых Н. А.
Портфолио воспитателя детского сада Кирилловых Н. А. Презентация социального проекта к 65-летию Победы Следы войны под нашими крышами
Презентация социального проекта к 65-летию Победы Следы войны под нашими крышами Презентация к уроку краеведения Что такое краеведение.Я родился в Заполярье
Презентация к уроку краеведения Что такое краеведение.Я родился в Заполярье Выпускной - 2014
Выпускной - 2014 Организация сюжетно-ролевой игр в старшей группеБольница
Организация сюжетно-ролевой игр в старшей группеБольница Каскад колокольчиков
Каскад колокольчиков Пасхальная открытка
Пасхальная открытка Производные протопласта растительной клетки
Производные протопласта растительной клетки Омыртқа жотасының зақымдануы
Омыртқа жотасының зақымдануы