Слайд 2

Этапы урока
I. Проверка домашнего задания. Фронтальный опрос.
II.Дидактическая игра «Классификация и номенклатура
веществ».
III.Самостоятельная работа.
IV.Подведение итогов.
Слайд 3

Домашнее задание
1. С какими из перечисленных веществ:
KOH,HNO3,MgO,Cu,SiO2,Ca (OH)2- будет
реагировать
серная кислота?
2. Составьте уравнения реакций по схеме:
Fe2(SO4)3 Fe(ОН)3 Fe2О3 Fe2(SO4)3.
3. Решите задачу. К раствору, содержащему избыток хлорида железа(III), прилили раствор, содержащий 240 г гидроксида натрия. Определите массу и количество образовавшегося гидроксида железа(III).
Слайд 4

Критерии оценки за Домашнее задание
1. Если задание выполнено самостоятельно и без
ошибок, поставьте -5 баллов.
2. Если допустили одну ошибку, поставьте
- 4 балла.
3. Если сделали две ошибки, поставьте
- 3 балла.
4. Если сделали три ошибки и более или не выполнили его, поставьте - прочерк.
Слайд 5

Дидактическая игра
«Найдите родственников и дайте им имена»
AI(OH)3, CO2, Mn2O7, HNO3, H2SiO3,
Na2HPO4, Mg(OH)2, CaCO3, RbOH, CuO, HBr, PbO2, KOH, Ca OHCI, H2SO3, NaHCO3, K3PO4 ,SO2, HgO, H2S, Zn(OH)2.
__________________________________________________________
1группа. Найти оксиды основные, кислотные, амфотерные (дать им названия)
2 группа. Найти основания растворимые и нерастворимые (дать им названия)
3 группа. Найти кислоты кислородсодержащие, бескислородные (дать им названия)
4 группа. Найти соли средние, основные, кислые (дать им названия)
Слайд 6

Ответ группы №1
Основные оксиды
CuO – оксид меди (II)
HgO –
оксид ртути (II)
Кислотные оксиды
CO2- оксид углерода (IV)
Mn2O7- оксид марганца (VII)
SO2 – оксид серы (IV)
Амфотерные оксиды
PbO2- оксид свинца (IV)
Слайд 7

Ответ группы №2
Растворимые основания
RbOH- гидроксид рубидия
KOH – гидроксид калия
Нерастворимые основания
AI(OH)3 –
гидроксид алюминия
Mg(OH)2- гидроксид магния
Zn(OH)2- гидроксид цинка
Слайд 8

Ответ группы №3
Кислородсодержашие кислоты
HNO3- азотная кислота
H2SiO3- кремневая кислота
H2SO3 – сернистая кислота
Бескислородные
кислоты
HBr- бромоводородная кислота
H2S- сероводородная кислота
Слайд 9

Ответ группы № 4
Средние соли
CaCO3 – карбонат кальция
K3PO4 – фосфат калия
Основные
соли
Ca OHCI – гидроксохлорид кальция
Кислые соли
Na2HPO4 – гидрофосфат натрия
NaHCO3 – гидрокарбонат натрия
Слайд 10
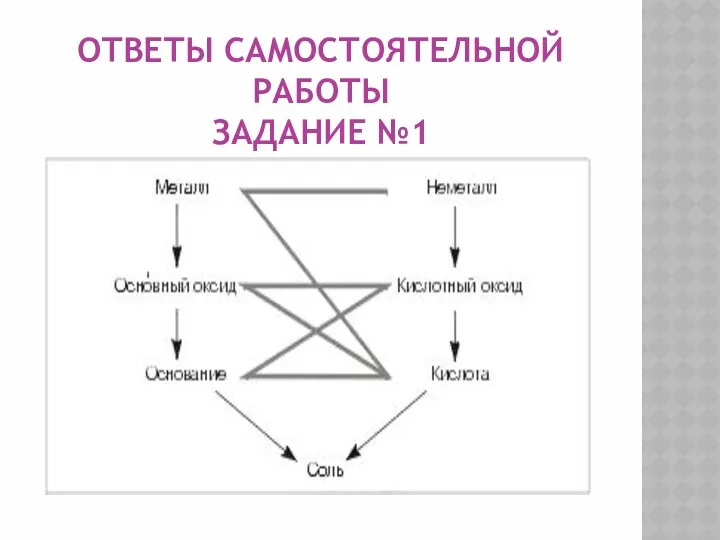
Ответы самостоятельной работы
задание №1
Слайд 11
Задание №2
Zn + 2HCI = ZnCI2 + H2
2KOH + H2SO4 =
K2SO4 + 2H2O
AI(OH)3 = AI2O3 + H2O
BaCI2 + H2SO4 = BaSO4 + 2HCI
AI(OH)3 + 3HNO3 = AI(NO3)3 + 3H2O
SO3 + Na2O = Na2SO3
AgNO3 + NaCI = AgCI + NaNO3
2KOH + H2S = K2S + H2O
Слайд 12

Задание № 3
1) Ba -> BaO -> Ba(OH)2 ->BaCI2
(или
другая соль)
2) P -> P2O5 -> H3PO4 -> Na3PO4
Слайд 13

Критерии оценки за задания № 1,2,3
1. Если задание сделано без ошибок
и самостоятельно, поставьте- 5 баллов.
2. Если задание сделано без ошибок, но вы обращались за помощью к товарищу, поставьте -4 балла.
3. Если вы сделали одну или две ошибки, поставьте -3 балла.
4. Если сделали более двух ошибок или не справились с заданием, поставьте -прочерк.
Слайд 14

Задание № 4
1) Лакмус + щелочь = синий окрас
2) FeCI3 +
3KOH = 3KCI + Fe(OH)3
Слайд 15

Критерии оценки за задание №4
1. Если вы правильно определили раствор щелочи,
самостоятельно записали уравнения химической реакции получения гидроксида железа(III) в молекулярном и ионном видах, поставьте -5 баллов.
2. Если допустили одну ошибку в уравнении химической реакций, но лабораторный опыт провели правильно, поставьте -4 балла.
3. Если сделали две ошибки в уравнениях химических реакций и экспериментальная часть задания выполнена не совсем правильно, поставьте -3 балла.
4. Если не записаны уравнения химических реакций и не проделана экспериментальная часть задания, поставьте прочерк.
Слайд 16

Критерии выставления итоговой оценки
1. Если все задания выполнены и большая часть
с оценкой «5», поставьте 5 баллов.
2. Если все задания выполнены, но преобладает оценка «4», поставьте 4 балла.
3. Если задания сделаны на оценку «3» или есть один прочерк, поставьте 3 балла.
4. Если вы не справились с двумя и более заданиями, поставьте прочерк.















 Презентация по выполнению куклы в средневековом костюме в технике бумагопластика Диск
Презентация по выполнению куклы в средневековом костюме в технике бумагопластика Диск Строительная компания Риэлт Строй 36-86-00 rsdoma.ru
Строительная компания Риэлт Строй 36-86-00 rsdoma.ru Внеклассное мероприятие для младших школьников. День Петра и Февронии
Внеклассное мероприятие для младших школьников. День Петра и Февронии Необычные животные
Необычные животные Земледельцы Аттики теряют землю и свободу
Земледельцы Аттики теряют землю и свободу Кровеносные сосуды. Круги кровообращения
Кровеносные сосуды. Круги кровообращения Селекция растений
Селекция растений Қабыршақтылар
Қабыршақтылар Планування та благоустрій котеджного селища
Планування та благоустрій котеджного селища Лексическая тема- Транспорт
Лексическая тема- Транспорт Сельскохозяйственный снабженческо-сбытовой потребительский кооператив Альянс фермервест. История создания и опыт работы
Сельскохозяйственный снабженческо-сбытовой потребительский кооператив Альянс фермервест. История создания и опыт работы Стратегия развития туризма в Мурманской области
Стратегия развития туризма в Мурманской области Доклад Формирование умения работать с учебником в начальной школе — залог успешного обучения в дальнейшем
Доклад Формирование умения работать с учебником в начальной школе — залог успешного обучения в дальнейшем Первичная профсоюзная организация студентов АлтГПУ
Первичная профсоюзная организация студентов АлтГПУ Результаты анализа применения эмульсионных взрывчатых веществ в горно-обогатительных комбинатах компании
Результаты анализа применения эмульсионных взрывчатых веществ в горно-обогатительных комбинатах компании Педагогические аспекты профессиональной деятельности. Тема 5
Педагогические аспекты профессиональной деятельности. Тема 5 Сохранность библиотечных фондов
Сохранность библиотечных фондов Мости
Мости Актуальность курса основы безопасности жизнедеятельности
Актуальность курса основы безопасности жизнедеятельности Зеленоград. Спортивная школа дошколят. Дзюдо
Зеленоград. Спортивная школа дошколят. Дзюдо Опухоли щитовидной железы
Опухоли щитовидной железы Бренд Lumene. Новинки
Бренд Lumene. Новинки культура профессионального общения педагога
культура профессионального общения педагога Кристаллические и аморфные тела
Кристаллические и аморфные тела презентация к классному часу в 4 классе Как воспитать характер по программе Все цвета, кроме черного
презентация к классному часу в 4 классе Как воспитать характер по программе Все цвета, кроме черного JavaScript Основы WEB-программирования
JavaScript Основы WEB-программирования Основные функции и принципы психолого-педагогической диагностики
Основные функции и принципы психолого-педагогической диагностики Родители – не гости, а полноправные участники коррекционно-педагогического процесса в ДОУ.
Родители – не гости, а полноправные участники коррекционно-педагогического процесса в ДОУ.