Содержание
- 2. Использование нуклеиновых кислот для изменения экспрессии генов в эукариотических клетках
- 3. Сферы применения синтетических олигонуклеотидов
- 4. Механизмы подавления трансляции антисмысловыми олигодезоксирибонуклеотидами (ODN) Трансляция в норме Разрушение РНК РНКазой H Блок инициации Блок
- 5. Гидролитическое дезаминирование аденозина с образованием инозина аденозиндезаминазой ADAR (Adenosine Deaminase that Acts on RNA) Инозин в
- 6. Метаболизм dsРНК с участием аденозиндезаминазы ADAR Редактирование dsРНК Специфическое Неспецифическое Перенос в цитоплазму 25-30 Оптимум: >100
- 7. Биогенез микроРНК в клетках животных - ядро Около 1000 генов miRNA у человека Pol II –
- 8. Биогенез микроРНК и подавление трансляции в клетках животных - цитоплазма Dicer – вторая РНКаза III RISC
- 9. Короткие интерферирующие РНК (siRNA)
- 10. Микро-РНК (miRNA) и короткие интерферирующие РНК (siRNA) могут использовать один и тот же механизм для осуществления
- 11. Некоторые свойства антисмысловых олигодезоксирибонуклеотидов (ODN) Механизм проникновения в клетку напоминает эндоцитоз, опосредованный рецепторами Высокие действующие концентрации
- 12. ODN первого поколения ISIS 2302 20-звенная молекула, завершены клинические испытания при язвенных колитах, мишень - ICAM-1
- 13. Модификации на основе бициклических сахаров ENA - ethylene-bridged nucleic acid Oxetane-modified ribose LNA - locked nucleic
- 14. Антисмысловые мофолино- (morpholino) ODN 6-звенное морфолиновое кольцо вместо рибозы Фосфородиамидитная связь вместо фосфодиэфирной связи Электронейтральная молекула
- 15. Пептидо-нуклеиновые кислоты (ПНК) Peptide nucleic acids (PNAs) ПНК ДНК Ахиральный электронейтральный псевдопептидный (полиамидный) остов ПНК Сахаро-фосфатный
- 16. Комплементарные взаимодействия между ПНК и ДНК
- 17. Применение пептидо-нуклеиновых кислот Антисмысловые и анти-генные стратегии мишени – мРНК (AUG-кодоны) и dsДНК (триплексы), антимикробные агенты
- 18. Механизм образования тройных спиралей ДНК триплекс-формирующими олигонуклеотидами (TFO) Хугстиновские связи
- 19. Трехмерная модель трехцепочечного участка ДНК, образованного триплекс-формирующим олигонуклеотидом (TFO) Молекула псоралена Цепь, обогащенная пуринами Цепь, обогащенная
- 20. Условия образования и свойства TFO Взаимодействуют с гомопуриновой цепью ДНК по большой бороздке Могут содержать в
- 21. Использование триплекс-образующих нуклеотидов в молекулярной биологии и генетике Ковалентное взаимодействие c T Псорален – природный фурокумарин
- 22. ДНК-аптамер ARC1172 в комплексе с доменом A1 фактора фон Виллебранда
- 23. Глобальный рынок аптамеров медицинского назначения (млн $)
- 24. Лиганды аптамеров
- 25. Сравнение размеров молекул антитела и нуклеотидного аптамера 17 nt
- 26. Области современного применения аптамеров
- 27. Схема отбора олигонуклеотидных аптамеров из комбинаторной библиотеки Хроматография Капиллярный электрофорез
- 28. Автоматизированная система отбора аптамеров RNA-SELEX
- 29. РНК-аптамер, взаимодействующий с AMP 36 nt Контакты преимущественно с кольцом аденина, но не рибозой. Может связывать
- 30. РНК-аптамер, взаимодействующий с GTP 41 nt Лиганд погружен в связывающий карман КD ~75 nM Обнаруживает много
- 31. РНК-аптамер, взаимодействующий с витамином B12 35 nt Лиганд взаимодействует с периферией аптамера
- 32. РНК-аптамер, взаимодействующий с FMN 35 nt FMN погружен в ДНК и образует водородные связи по границе
- 33. Зеркальные аптамеры- шпигельмеры (Spiegelmer) L-Рибоза или L-2’-дезоксирибоза в сахаро-фосфатном остове Получение: Обычный отбор среди обычных нуклеиновых
- 34. Технология получения шпигельмеров
- 35. Биосенсоры на основе олигонуклеотидных аптамеров Биосенсоры – молекулярные устройства, количественно преобразующие сигнал от внешних воздействий в
- 36. Модификации аптамеров
- 37. Рибозимы и дезоксирибозимы
- 38. Thomas Cech – первооткрыватель рибозимов 1982 г. Аутосплайсинг интрона рибосомной 35S-РНК жгутикового простейшего Tetrahymena Нобелевская премия
- 40. Сидни Олтман (Sidney Altman) получает Нобелевскую премию за РНКазу P
- 41. Каталитический цикл рибозима Рибозим (E) РНК-субстрат (S) Фермент-субстратный комплекс (E-S) Комплекс (в переходном состоянии Комплекс фермент-продукт
- 42. Фолдинг оцДНК Гидролиз субстрата rA – AMP (рибонукдеозид-монофосфат) B - биотин Схема отбора in vitro дезоксирибозима,
- 43. ДНКзимы, обладающие РНКазной активностью Субстрат РНК
- 44. Подтипы рибозимов, сконструированных на основе рибозима типа «головки молотка» РНК (субстрат) Максизим Рибозим типа «головки молотка»
- 45. Сборка активного максизима
- 46. Подавление репликации HIV гетеродимерным максизимом
- 47. Подавление репликации HIV гетеродимерным максизимом (окончание)
- 48. Аллостерический рибозим (аптазим) и его пространственная структура Место расщепления РНК Связывание ATP ингибирует рибозим
- 49. Некоторые реакции, осуществляемые дезоксирибозимами
- 50. ДНК в наноконструкторе
- 51. Примеры неканонических ветвящихся структур ДНК Концы стрелок соответствуют 3’-концам молекул ДНК
- 52. Образование двумерных решеток из стабильных конструкций с липкими концами
- 53. Топологические последствия лигирования молекул ДНК, содержащих четное и нечетное число полувитков на границах ячеек Нечетное Кольцевые
- 54. Сложные ДНК-оригами оцДНК фага M13 (7240 nt) смешивали с 250 олигонуклеотидами-помощниками (32 nt) и охлаждали 2
- 55. Куб как сумма линейных катенанов ДНК Линейные тройные катенаны ДНК (в центре рисунка) спонтанно собираются с
- 57. Скачать презентацию
 Детский лагерный отдых на Восточном берегу Крыма
Детский лагерный отдых на Восточном берегу Крыма Причины появления и виды банков
Причины появления и виды банков Статус женщины в обществе Китая
Статус женщины в обществе Китая Русская народная сказка. Теремок
Русская народная сказка. Теремок История и роль полиграфии в графическом дизайне. Введение в предпечатную подготовку. (Лекция 1)
История и роль полиграфии в графическом дизайне. Введение в предпечатную подготовку. (Лекция 1) Классификация малоэтажной жилой недвижимости
Классификация малоэтажной жилой недвижимости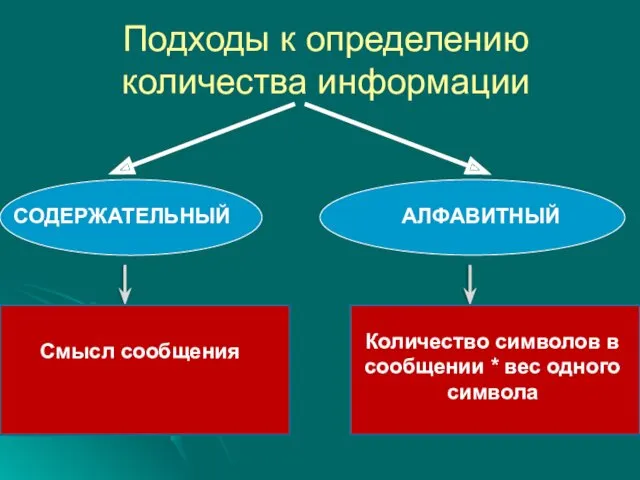 Подходы к определению количества информации
Подходы к определению количества информации Проект:Сохрани свое здоровье сам
Проект:Сохрани свое здоровье сам Клиника и патогенез аутоиммунного гепатита
Клиника и патогенез аутоиммунного гепатита Организация работы классного руководителя и воспитателя в свете национальной инициативы Наша новая школа
Организация работы классного руководителя и воспитателя в свете национальной инициативы Наша новая школа Детский православный журнал Божий лучик
Детский православный журнал Божий лучик Общий обзор строения и функций организма человека 8 класс
Общий обзор строения и функций организма человека 8 класс Системы телекоммуникации
Системы телекоммуникации Образование. Цель образования
Образование. Цель образования Долговечность и факторы, вызывающие износ зданий и сооружений
Долговечность и факторы, вызывающие износ зданий и сооружений Знаки препинания в бессоюзном сложном предложении
Знаки препинания в бессоюзном сложном предложении Презентация Проектная деятельность в ДОУ
Презентация Проектная деятельность в ДОУ Опухоли яичников (часть 1)
Опухоли яичников (часть 1) Диференціація звуків Д-Т
Диференціація звуків Д-Т Block diagrams (elements flowcharts block types)
Block diagrams (elements flowcharts block types) Презентация педагогического проекта Формирование элементарных математических представлений как средство развития мыслительной деятельности у дошкольников с задержкой психического развития
Презентация педагогического проекта Формирование элементарных математических представлений как средство развития мыслительной деятельности у дошкольников с задержкой психического развития Алгоритм диагностики пациента с болью в грудной клетке
Алгоритм диагностики пациента с болью в грудной клетке Направление государственной политики Новая модель образования
Направление государственной политики Новая модель образования Развитие коммуникативной культуры у младших школьников
Развитие коммуникативной культуры у младших школьников Блокада Ленинграда Диск
Блокада Ленинграда Диск Липецк на карте мира
Липецк на карте мира Развитие транспортно-логистической системы Республики Казахстан
Развитие транспортно-логистической системы Республики Казахстан Крестовые походы и инквизиция
Крестовые походы и инквизиция