Содержание
- 2. Основы квантовой физики Волновые свойства микрочастиц
- 3. Переход от классической физики и квантовой связан с проблемой теплового излучения и, в частности, с вопросом
- 4. В итоге изучения предыдущего раздела сформировывается представление о том, что электромагнитное излучение имеет двойственную корпускулярно-волновую природу
- 5. Известны 4 механики: классическая или ньютоновская механика, релятивиская механика (теория относительности), квантовая механика и релятивиская квантовая
- 6. Гипотеза Луи де Бройля В 1923 году французский физик Луи де Бройль высказал гипотезу о том,
- 9. Французский ученый Луи де Бройль (1892—1987), осознавая существующую в природе симметрию и развивая представления о двойственной
- 10. Итак, согласно де Бройлю, с каждым микрообъектом связываются, с одной стороны, корпускулярные характеристики — энергия Е
- 11. Найдем длину волны де Бройля, соответствующую движущемуся электрону. Кинетическая энергия, приобретенная электроном в ускоряющем поле равна
- 12. Вероятностный смысл волн де – Бройля Экспериментальное подтверждение идеи де Бройля об универ-сальности корпускулярно-волнового дуализма, ограниченность
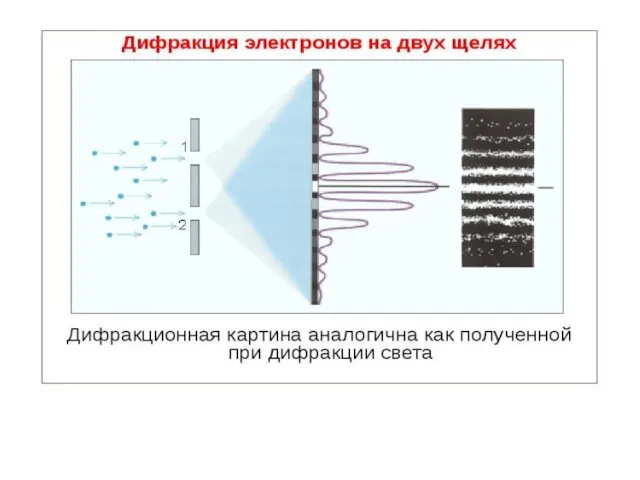
- 13. Для выяснения этой проблемы сравним дифракцию световых волн и микрочастиц. Дифракционная картина, наблюдаемая для световых волн,
- 14. Наличие максимумов в дифракционной картине с точки зрения волновой теории означает, что эти направления соответствуют наибольшей
- 15. Экспериментальные подтверждения гипотезы де Бройля. Критерием истинности любой физической теории, любой гипотезы всегда является эксперимент. Необходимость
- 16. Опыты Девиссона и Джермера Первое подтверждение гипотезы де Бройля было получено в 1927 году в опытах
- 17. Идея их опытов заключалась в следующем. Если пучок электронов обладает волновыми свойствами, то можно ожидать, даже
- 18. Детектор перемещали в плоскости падения, меняя угол θ. При угле θ = 50° и ускоряющем напряжении
- 19. Вычисленная по формуле (2.1) дебройлевская длина волны для U= 54В равна 0,167 нм. Соответствующая же длина
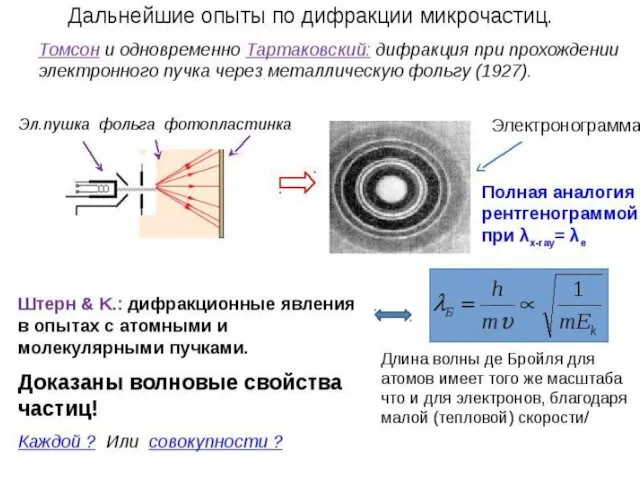
- 20. Опыты Томсона и Тартаковского Петр Саввич Тартаковский (1895–1940) В 1926-1927 гг. самостоятельно без соавторов ставит свои
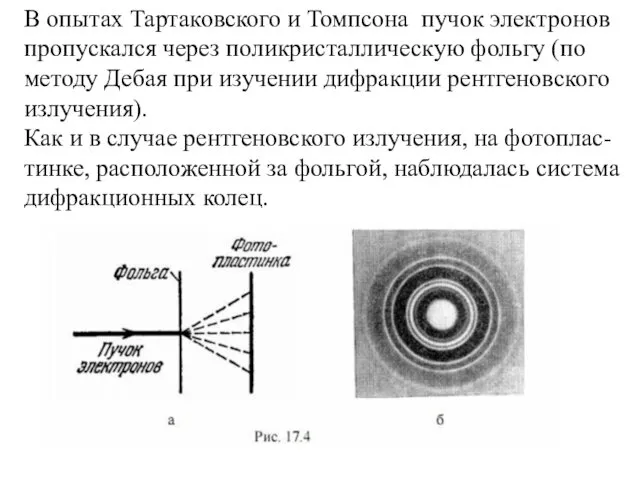
- 21. В опытах Тартаковского и Томпсона пучок электронов пропускался через поликристаллическую фольгу (по методу Дебая при изучении
- 23. Сходство обеих картин поразительно.
- 24. Подозрение, что система этих колец порождается не электронами, а вторичным рентгеновским излучением, возникающим в результате падения
- 25. Опыты с нейтронами и молекулами Для успешного наблюдения дифракции волн на кристаллах необходимо, чтобы длина волны
- 28. Если предположение де Бройля верно, то почему эти волновые свойства не обнаруживаются у движущихся тел? Например,
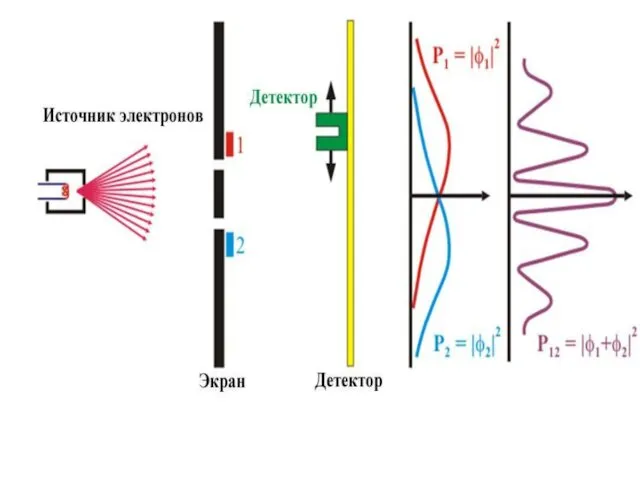
- 29. Опыты с одиночными электронами Описанные выше опыты выполнялись с использованием пучков частиц. Поэтому возникает естественный вопрос:
- 31. В. Фабрикант, Л. Биберман и Н. Сушкин осуществили в 1949 г. опыты, в которых применялись столь
- 37. Так было доказано, что волновыми свойствами обладают и отдельные частицы. Таким образом, мы имеем дело с
- 38. Из формулы де Бройля следовало, что волновые свойства должны быть присущи любой частице вещества, имеющей массу
- 39. Вероятностный смысл волн де Бройля
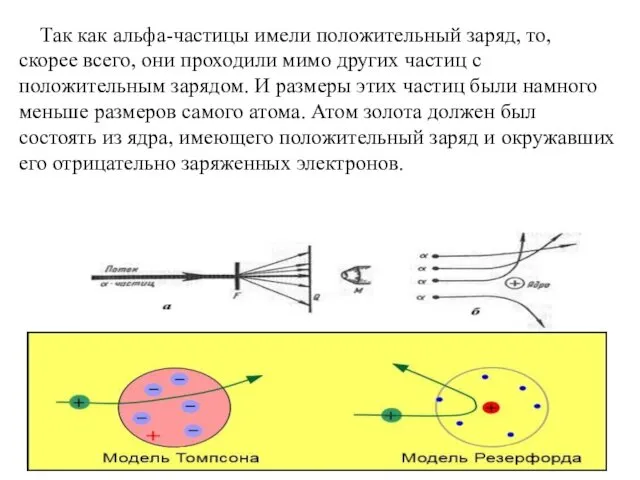
- 47. Физика атома Модели строения атома 1. Модель Томсона Первая модель строения атома была предложена Дж. Томсоном
- 48. 2.2 Модель Резерфорда Модель Томсона была опровергнута Э. Резерфордом (1911 г.), который доказал, что положительный заряд
- 50. Опыт Резерфорда В 1909 г. английский физик Эрнест Резерфорд провёл опыт с рассеиванием альфа-частиц, которые образуются
- 51. Так как альфа-частицы имели положительный заряд, то, скорее всего, они проходили мимо других частиц с положительным
- 52. Модель Резерфорда имела и другие противоречия. Так при непрерывном излучении энергии у атома должен наблюдаться непрерывный,
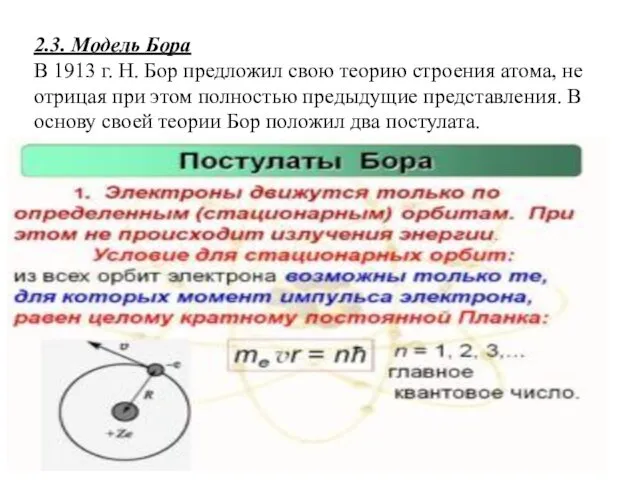
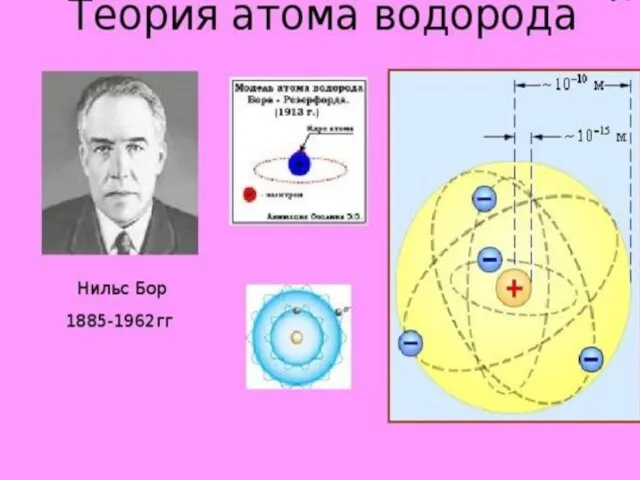
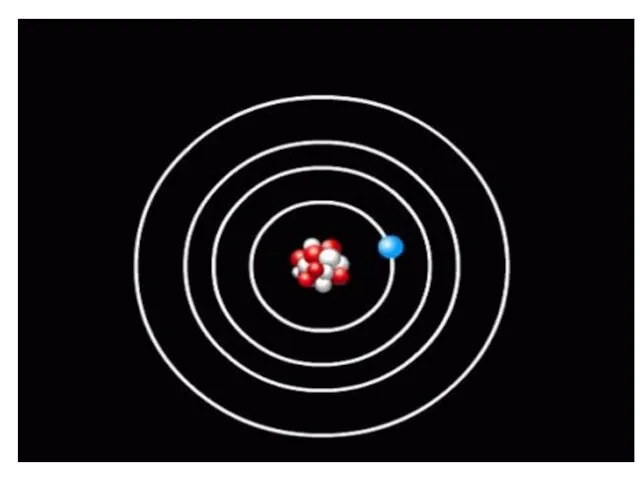
- 54. 2.3. Модель Бора В 1913 г. Н. Бор предложил свою теорию строения атома, не отрицая при
- 70. водородоподобных система - система, состоящих из ядра с зарядом Ze и одного электрона (например, ионы Не+,
- 71. Атом водорода. Атом водород состоит из ядра с зарядом , которое называется протоном, и одного электрона
- 72. 3. Выше отмечалось, что классическая физика перестаёт работать внутри атома. Так оно в действительности и есть,
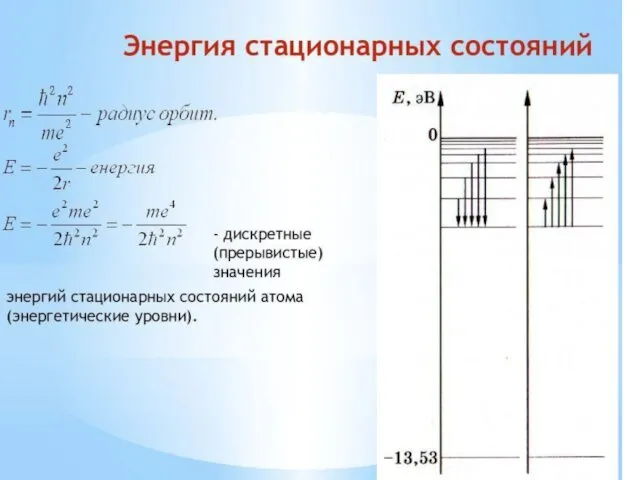
- 73. Отсюда получаем формулу для допустимых радиусов орбит электрона (3) перейдём к нахождению энергии электрона. Потенциальная энергия
- 74. По формуле (3) легко вычислить радиус орбиты основного состояния см. То есть, диаметр атома оказы- вается
- 75. Полная энергия, отрицательна. Если на радиус орбиты никаких ограничений не накладывается, как это имеет место в
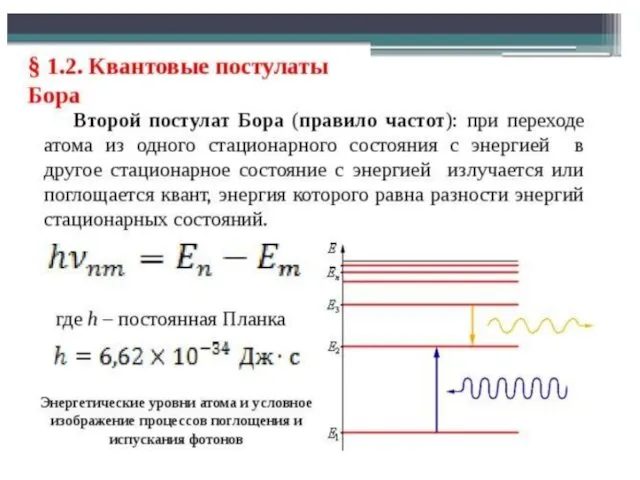
- 76. получим уравнение для определения энергии ε, излучаемой (или поглощаемой) атомом при переходе электрона с одной орбиты
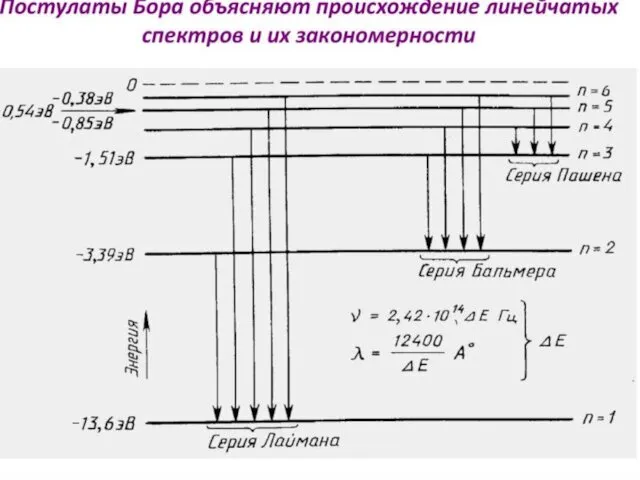
- 77. Например, возможен переход с любого уровня n≥2 на нормальный уровень 1. В спектре излучения водорода это
- 78. что ведет к излучению другой серии линий в спектре водорода, серии Бальмера Она лежит в видимойобласти
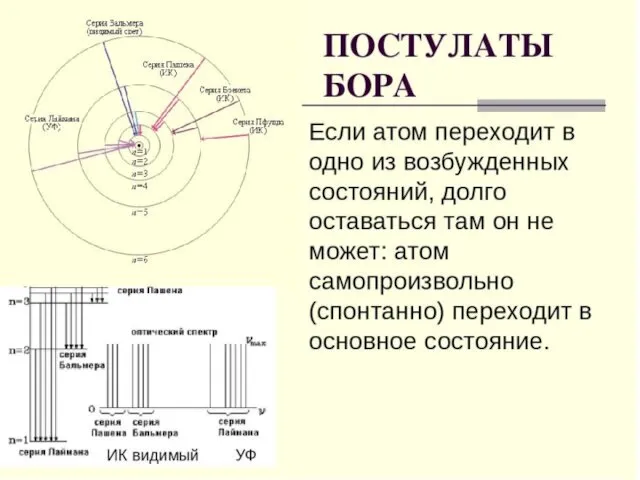
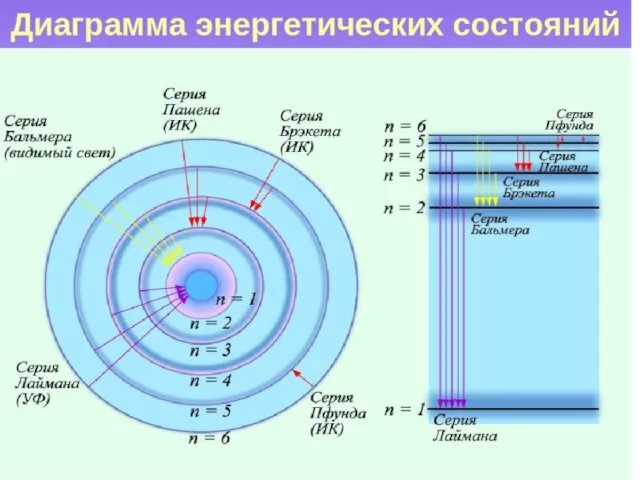
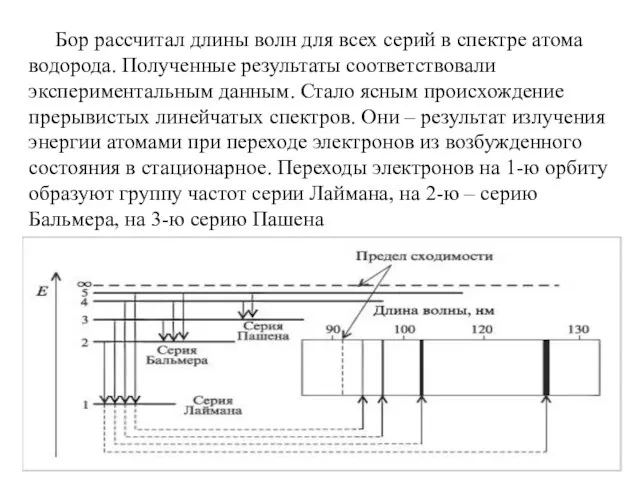
- 79. образование спектральных серий в излучении атома водорода при переходе электрона с высоких стационарных орбит на более
- 80. диаграмма энергетических уровней атома водорода и указаны переходы, соответствующие различным спектральным сериям. Для первых пяти линий
- 81. Прекрасное согласие боровской теории атома водорода с экспериментом служило веским аргументом в пользу ее справедливости. Однако
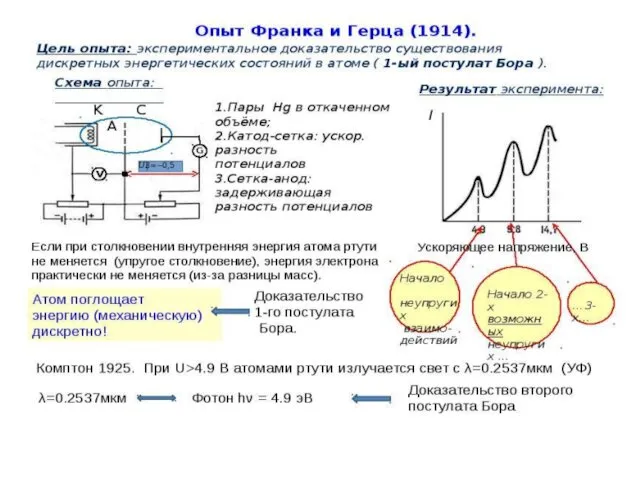
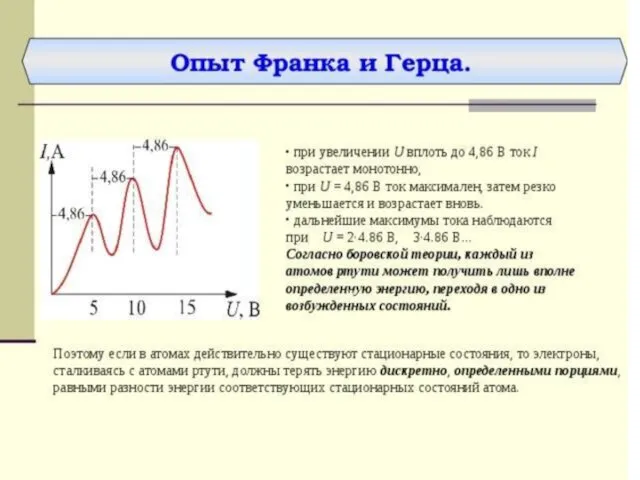
- 84. Оказалось, что если энергия электронов меньше 4,9 эВ, то их столкновение с атомами ртути происходит по
- 85. Квантовая физика не отменила фундаментальных классических законов сохранения энергии, импульса, электрического разряда и т. д. Согласно
- 86. Половинчатая, полуклассическая теория Бора явилась важным этапом в развитии квантовых представлений, введение которых в физику требовало
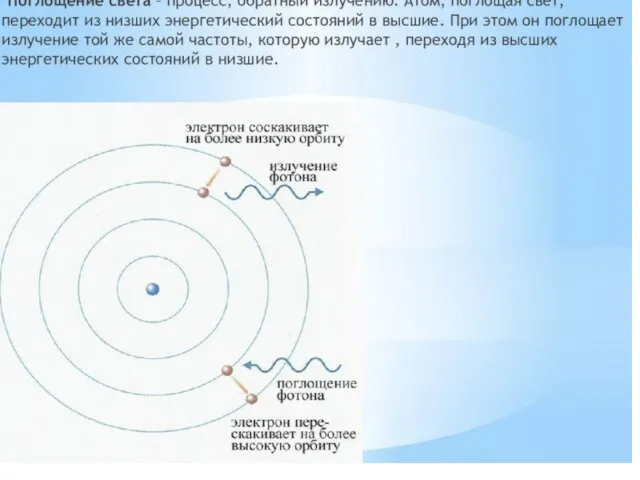
- 90. В модели атома водорода Бор использовал следующие положения ( постулаты): При движении по любой стационарной орбите
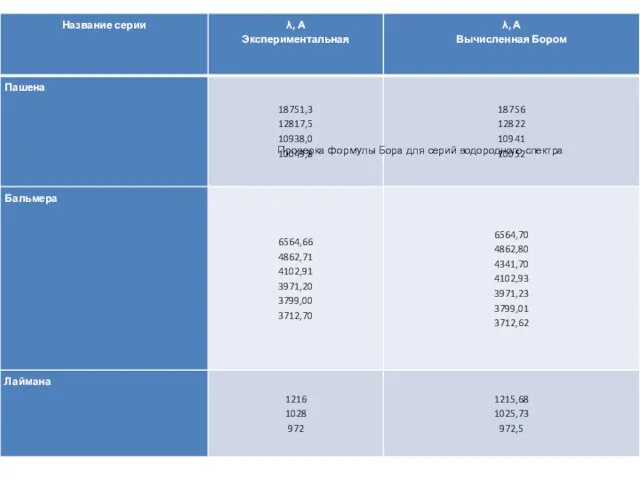
- 91. Бор рассчитал длины волн для всех серий в спектре атома водорода. Полученные результаты соответствовали экспериментальным данным.
- 93. Энергетические уровни электрона в атоме водорода и спектр его излучения
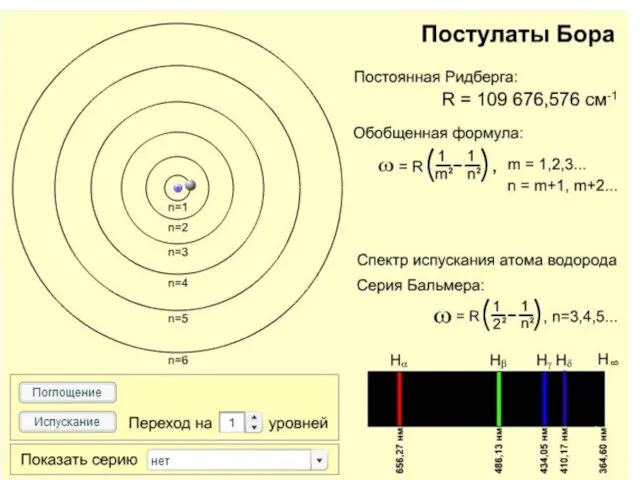
- 94. Спектр излучения атома водорода Формула Бальмера,1885 г. Видимые линии излучения водорода в серии Бальмера. Hα —
- 95. Обобщенная сериальная формула Бальмера Где R - постоянная Ридберга, m,n –главные квантовые числа, Z - порядковый
- 96. Проверка формулы Бора для серий водородного спектра
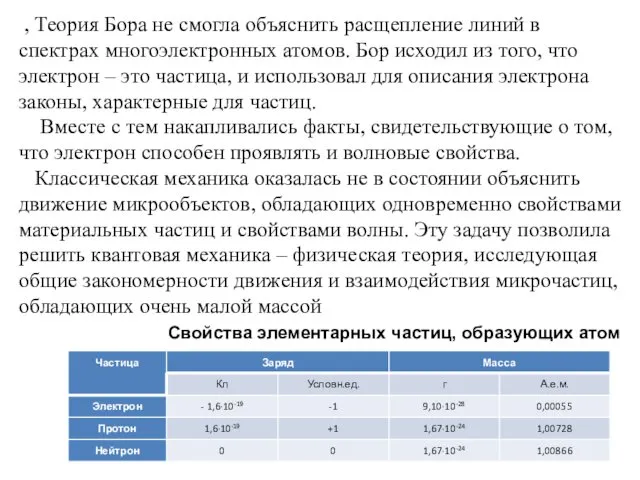
- 99. , Теория Бора не смогла объяснить расщепление линий в спектрах многоэлектронных атомов. Бор исходил из того,
- 100. Достоинства и недостатки теории Бора. О достоинствах модели атома водорода, предложенной Бором, мы так или иначе
- 101. щих дискретный набор. Этот факт оказался общим свойством объектов микромира. В рамках модели Бора удалось получить
- 102. уравнения движения электрона по круговой орбите Теория Бора не смогла дать адекватное описание самого простого после
- 109. Волновая функция Необходимость вероятностного подхода к описанию микро-частиц является важнейшей отличительной особенностью квантовой теории. Можно ли
- 110. Таким образом, описание состояния микрообъекта с помощью волновой функции имеет статистический, вероятностный характер: квадрат модуля волновой
- 111. Частица должна находиться где-то в пространстве. Следовательно, условие нормировки вероятностей де данный интеграл вычисляется по всему
- 113. Скачать презентацию

























































































 Античная философия
Античная философия Anatomie a fyziologie rostlin
Anatomie a fyziologie rostlin Организация ЭВМ и систем. Переход от CISC к чертам RISC архитектуры в семействе IA32. (Лекция 6)
Организация ЭВМ и систем. Переход от CISC к чертам RISC архитектуры в семействе IA32. (Лекция 6) Особые типы магматических формаций. Формации расслоенных интрузивов ультраосновных и основных пород
Особые типы магматических формаций. Формации расслоенных интрузивов ультраосновных и основных пород Электронное портфолио
Электронное портфолио Технологическое оборудование и и нвентарь
Технологическое оборудование и и нвентарь Дворцовая электростанция в Царском Селе
Дворцовая электростанция в Царском Селе Лекция 1: Введение в дисциплину Направляющие системы телекоммуникаций
Лекция 1: Введение в дисциплину Направляющие системы телекоммуникаций Презентации Диск
Презентации Диск Служба психолого-педагогического сопровождения в условиях современной школы интернатного типа.
Служба психолого-педагогического сопровождения в условиях современной школы интернатного типа. Методические рекомендации по подготовке проекта к конкурсу Мир театра
Методические рекомендации по подготовке проекта к конкурсу Мир театра Презентация Нет друга, ищи, а нашел, так береги к занятию по теме Дружба
Презентация Нет друга, ищи, а нашел, так береги к занятию по теме Дружба Мой опыт использования разнообразных форм работы с родителями
Мой опыт использования разнообразных форм работы с родителями ОГЭ по биологии 2020. Выполнение задания №26
ОГЭ по биологии 2020. Выполнение задания №26 Валеологический проект Здоровичок
Валеологический проект Здоровичок Космическая математика Викторина
Космическая математика Викторина Презентация к уроку технологии по теме: Архитектурная керамика. Изразец 4 класс
Презентация к уроку технологии по теме: Архитектурная керамика. Изразец 4 класс Профилактика и коррекция дисграфии на почве нарушения фонемного распознавания. Дифференциация Б-Т.
Профилактика и коррекция дисграфии на почве нарушения фонемного распознавания. Дифференциация Б-Т. Загальні принципи анестезіологічного забезпечення оперативних втручань
Загальні принципи анестезіологічного забезпечення оперативних втручань Snow Globe
Snow Globe Реализация приоритетного проекта Безопасные и качественные дороги в Кировской городской агломерации
Реализация приоритетного проекта Безопасные и качественные дороги в Кировской городской агломерации презентация Канада
презентация Канада Внеклассное мероприятие Права ребенка
Внеклассное мероприятие Права ребенка организация самооценки И ДОМАШНИХ ЗАДАНИЙ учащихся
организация самооценки И ДОМАШНИХ ЗАДАНИЙ учащихся Классный час Дружба каждому нужна
Классный час Дружба каждому нужна fedfd-38682f58
fedfd-38682f58 Мыши водят хоровод
Мыши водят хоровод Простое глагольное сказуемое
Простое глагольное сказуемое