Содержание
- 2. Основное содержание темы: Понятие о предельных углеводородах (алканах) Гомологический ряд алканов Изомерия и номенклатура алканов Способы
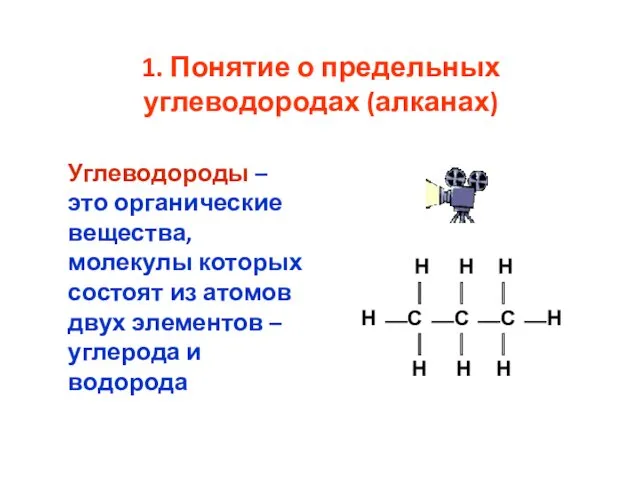
- 3. 1. Понятие о предельных углеводородах (алканах) Углеводороды – это органические вещества, молекулы которых состоят из атомов
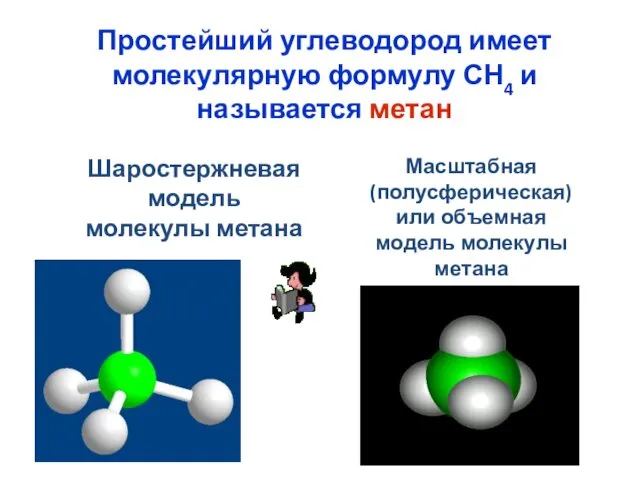
- 4. Простейший углеводород имеет молекулярную формулу СН4 и называется метан Масштабная (полусферическая) или объемная модель молекулы метана
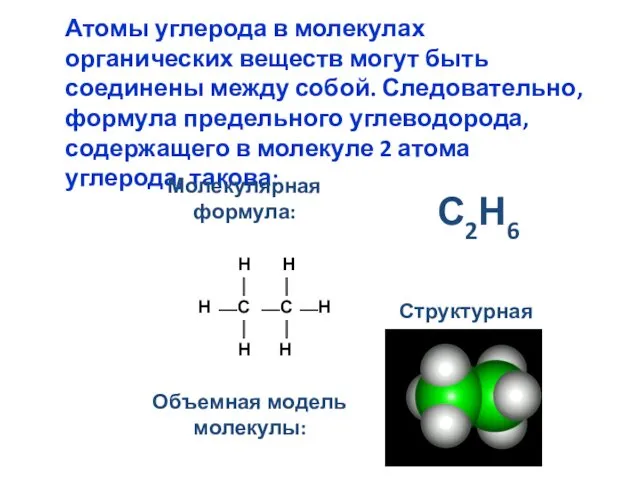
- 5. Атомы углерода в молекулах органических веществ могут быть соединены между собой. Следовательно, формула предельного углеводорода, содержащего
- 6. Алканами (предельными, насыщенными, парафиновыми углеводородами) называют углеводороды, в молекулах которых атомы связаны одинарными сигма-связями и которые
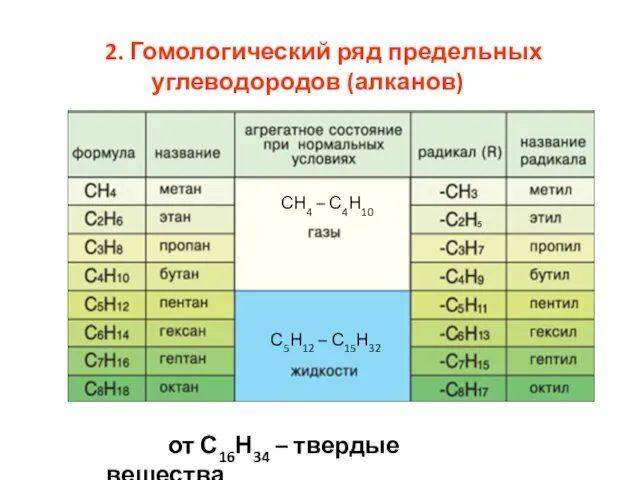
- 7. 2. Гомологический ряд предельных углеводородов (алканов) СН4 – С4Н10 С5Н12 – С15Н32 от С16Н34 – твердые
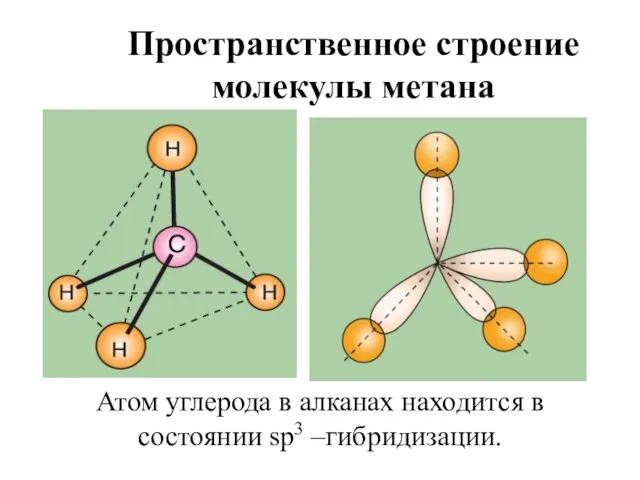
- 8. Пространственное строение молекулы метана Атом углерода в алканах находится в состоянии sp3 –гибридизации.
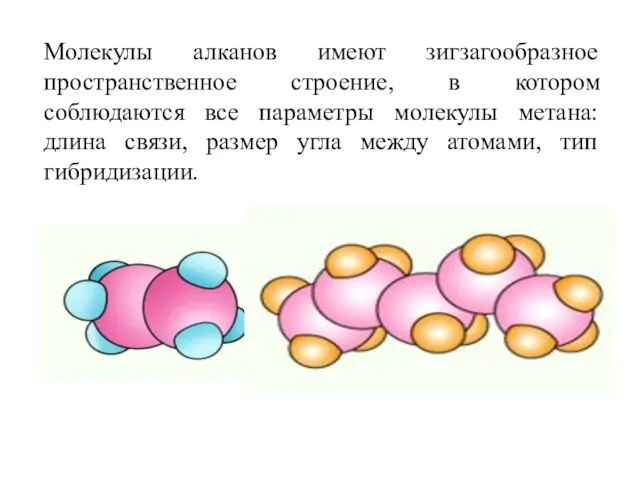
- 9. Молекулы алканов имеют зигзагообразное пространственное строение, в котором соблюдаются все параметры молекулы метана: длина связи, размер
- 10. 4. Физические свойства С увеличением относительных молекулярных масс предельных углеводородов закономерно повышаются их температуры кипения и
- 11. Ряд веществ, сходных по строению и свойствам, но отличающихся друг от друга по составу на одну
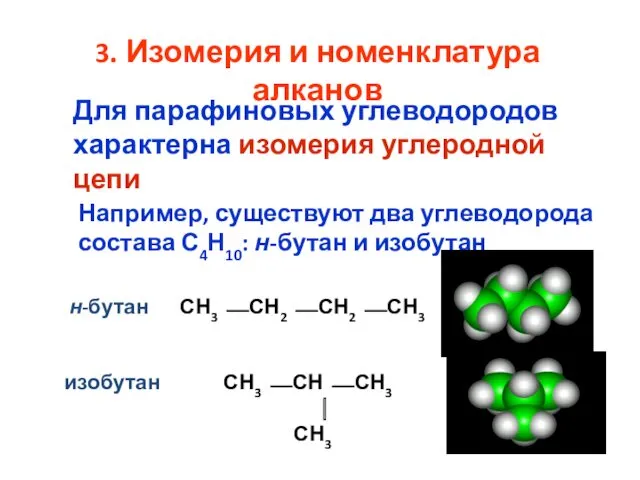
- 12. 3. Изомерия и номенклатура алканов Для парафиновых углеводородов характерна изомерия углеродной цепи СН3 ⎯ СН ⎯
- 13. Алгоритм составления названий алканов по международной номенклатуре Выбрать в молекуле самую длинную цепочку углеродных атомов. Пронумеровать
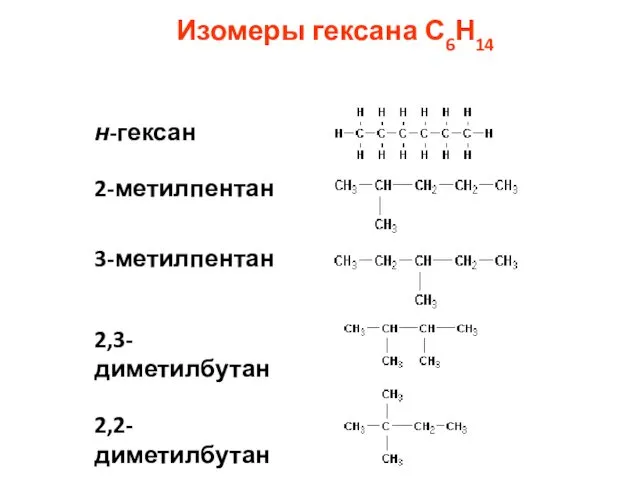
- 14. Изомеры гексана С6Н14 н-гексан 2-метилпентан 3-метилпентан 2,3-диметилбутан 2,2-диметилбутан
- 15. Потренируйтесь в составлении названий алканов Потренируйся в написании структурных формул алканов по их названям
- 16. 4. Способы получения алканов Промышленные способы получения 1. Выделение из природных источников углеводородов – природного газа,
- 17. 4. Получение Получение метана при сплавлении ацетата натрия со щелочью: t °C CH3COONa + NaOH ⎯⎯→
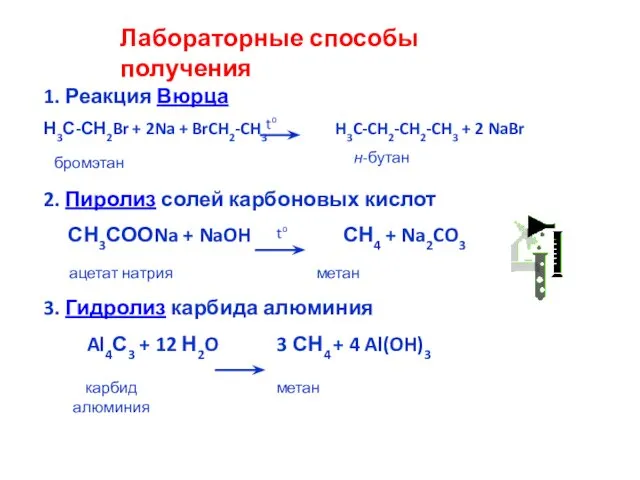
- 18. Лабораторные способы получения 1. Реакция Вюрца Н3С-СН2Br + 2Na + BrCH2-CH3 H3C-CH2-CH2-CH3 + 2 NaBr 2.
- 19. Реакция Вюрца (синтез Вюрца) проводят с целью получения алканов с более длинной углеродной цепью. Например: получение
- 20. Метан в лаборатории можно получить гидролизом карбида алюминия Al4C3 + 12H2O = 4Al(OH)3 + 3CH4
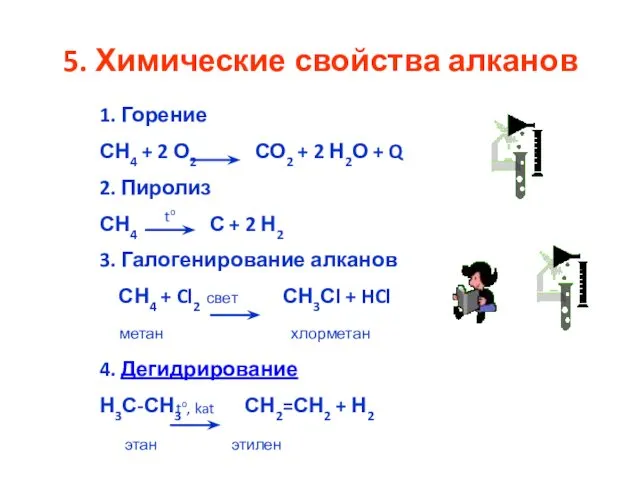
- 21. 5. Химические свойства алканов 1. Горение СН4 + 2 О2 СО2 + 2 Н2О + Q
- 22. Термин парафины произошел от латинских слов «parum» — «мало» и «affinis» — «сродство» из-за его низкой
- 23. 6. Применение предельных углеводородов 1. Газообразное и жидкое топливо (бытовой газ, бензин, дизельное топливо, керосин и
- 24. Назовите по международной номенклатуре алкан: 2. Напишите структурную формулу 2,2-диметилбутана 3. Напишите структурные формулы всех изомеров
- 26. Скачать презентацию













 Моя мама лучшая на свете
Моя мама лучшая на свете Научная теория и методы научного познания. Философия науки. (Лекция 5)
Научная теория и методы научного познания. Философия науки. (Лекция 5)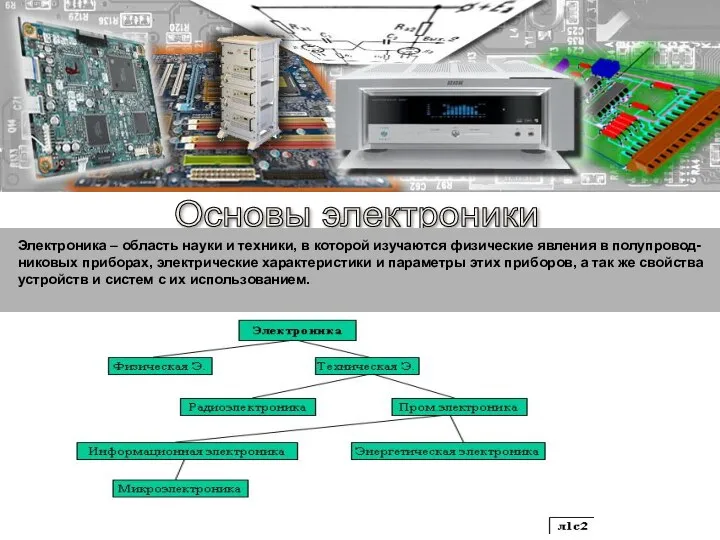 Основы электроники
Основы электроники Ассортимент для барменов
Ассортимент для барменов Инвестиционный меморандум АНГРЕНСОР ЭНЕРГО
Инвестиционный меморандум АНГРЕНСОР ЭНЕРГО Роль биологии в системе медицинского образования. Клеточный уровень организации живого
Роль биологии в системе медицинского образования. Клеточный уровень организации живого Урок по теме Кислоты
Урок по теме Кислоты Упрощение выражений
Упрощение выражений Площадь поверхности пирамиды
Площадь поверхности пирамиды Редакция 3.0: новые возможности 1С:Бухгалтерии 8
Редакция 3.0: новые возможности 1С:Бухгалтерии 8 C наступающим праздником Новый Год
C наступающим праздником Новый Год Визитная карточка
Визитная карточка Игры и задания на развитие интеллекта. 4 – 7 лет
Игры и задания на развитие интеллекта. 4 – 7 лет Подходы к управлению. Эволюция управления как науки
Подходы к управлению. Эволюция управления как науки Наплавляемая кровля
Наплавляемая кровля Религии мира. Христианство
Религии мира. Христианство Компьютеризованная вышивальная машина Brother. Руководство к действию.
Компьютеризованная вышивальная машина Brother. Руководство к действию. Об'єкти, масиви, формат JSON в JavaScript
Об'єкти, масиви, формат JSON в JavaScript 195 лет со дня рождения Александра Островского. Смех, слёзы и истина
195 лет со дня рождения Александра Островского. Смех, слёзы и истина Нижний Новгород в вопросах и ответах
Нижний Новгород в вопросах и ответах Природные ресурсы
Природные ресурсы Фашизм в Германии
Фашизм в Германии Прочитанная книга о войне - твой подарок ко Дню Победы
Прочитанная книга о войне - твой подарок ко Дню Победы Синтетические волокна. Их свойства. Классификация. Применение. Синтетический каучук
Синтетические волокна. Их свойства. Классификация. Применение. Синтетический каучук Софизмы в алгебре
Софизмы в алгебре Расслоение аневризмы аорты. Хирургическое лечение
Расслоение аневризмы аорты. Хирургическое лечение Ефекти радіаційного ураження
Ефекти радіаційного ураження ЭРДУ аппарата Smart 1
ЭРДУ аппарата Smart 1