Слайд 2

Слайд 3

Слайд 4

Слайд 5

Слайд 6

Слайд 7

Слайд 8

Слайд 9

Слайд 10

Слайд 11

В мире ежегодно огромное количество различных металлов и сплавов, и
примерно 10% этого количества разрушаются в результате коррозии. А из всего количества сплавов на основе железа теряется примерно 25%. Ржавеет только железо, а остальные металлы – корродируют.
Что же это за процесс – коррозия?
Коррозия (от латинского corrodere – «разъедать»)- самопроизвольное разрушение металлов и сплавов под влиянием окружающей среды.
Слайд 12

Коррозию вызывают:
Вода
Кислород
Оксиды углерода и серы
Водные растворы солей (морская вода, грунтовые воды)
Слайд 13

Виды коррозии.
1/Химическая – это разрушение металлов в результате их химического
взаимодействия с веществами окружающей среды.
Слайд 14
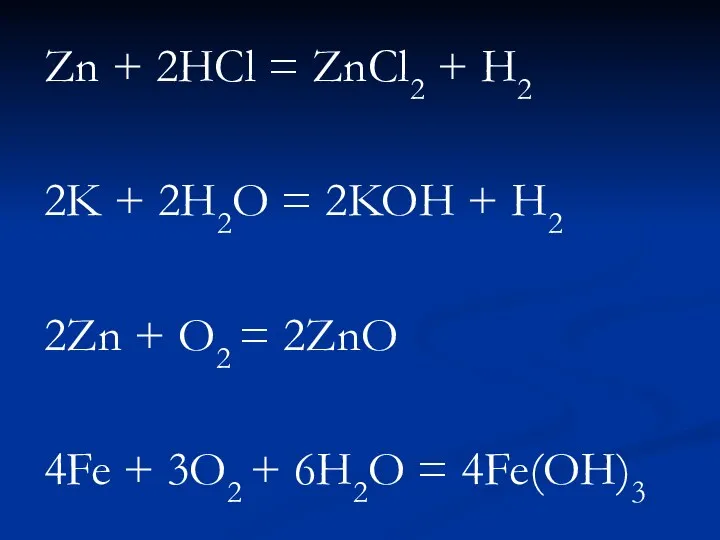
Zn + 2HCl = ZnCl2 + H2
2K + 2H2O = 2KOH
+ H2
2Zn + O2 = 2ZnO
4Fe + 3O2 + 6H2O = 4Fe(OH)3
Слайд 15

2/Электрохимическая – это разрушение металлов, которое сопровождается возникновением электрического тока.
Наряду с химическими процессами протекают электрические.
Слайд 16
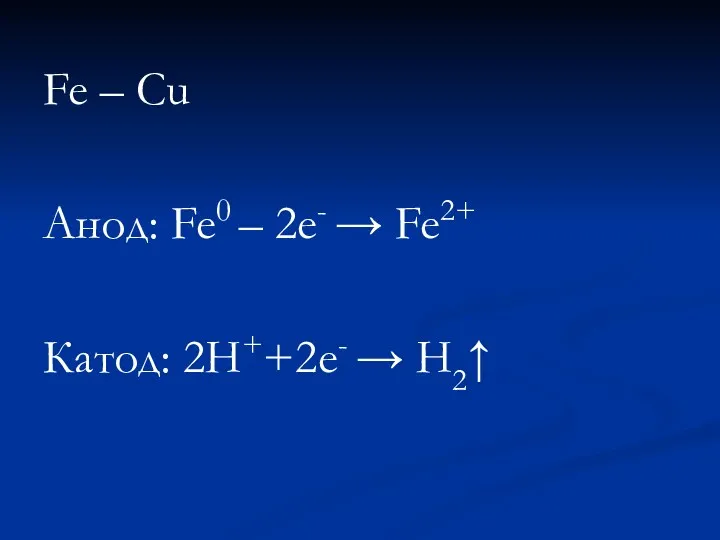
Fe – Cu
Анод: Fe0 – 2е- → Fe2+
Катод: 2H++2e- → H2↑
Слайд 17

Способы защиты от коррозии
Слайд 18

Закрепление
1. В подвале дома обнаружили ящик с гвоздями, но от неправильных
условий хранения многие из них были покрыты ржавчиной.
Что представляет собой ржавчина с химической точки зрения?
Каким простым способом можно удалить ржавчину?
Слайд 19

2. Молодая хозяйка повесила сушить бельё на железную проволоку, натянутую между
стойками. Когда бельё высохло, она с ужасом обнаружила на чистом белье желтые полосы.
Как объяснить появление полос на белье?
Как можно избавиться от этих пятен?
Слайд 20

3. В домашней мастерской всегда много инструментов, запчастей и материалов, которые
в основном изготовлены из металлов и их сплавов. Но вот беда – при хранении металлические изделия подвергаются коррозии.
Укажите условия хранения металлических изделий, которые продлят срок их службы.
Слайд 21

4. Соляная кислота с добавкой ингибитора нашла применение для очистки паровых
котлов от отложении накипи и удаления с поверхности металлов ржавчины и окалины.
Почему?












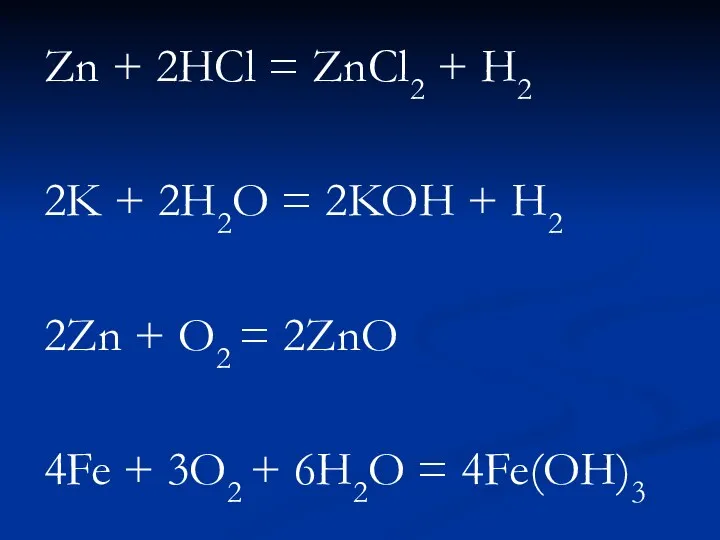

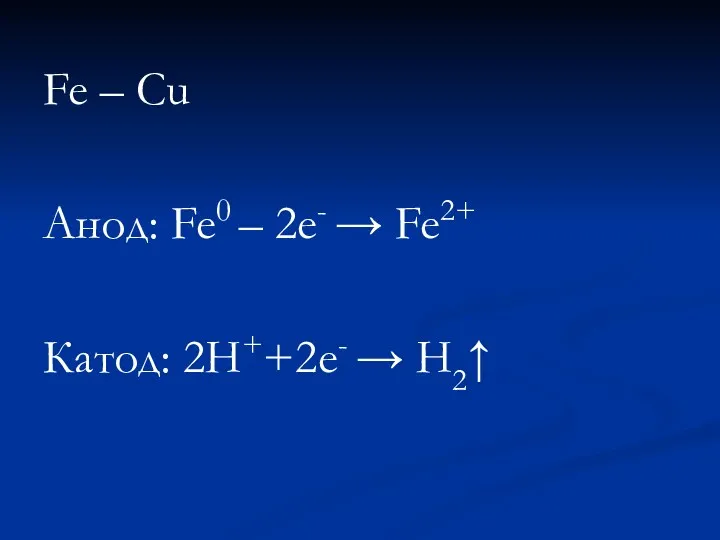





 Электронно-дырочный переход. Транзистор
Электронно-дырочный переход. Транзистор Сканеры. Устройства ввода информации в компьютер
Сканеры. Устройства ввода информации в компьютер Santa Claus or Saint Nicolas
Santa Claus or Saint Nicolas Отвод поверхностных вод. Водосборно-водоотводные сооружения (водоотводы)
Отвод поверхностных вод. Водосборно-водоотводные сооружения (водоотводы) Презентация Как помочь ребенку хорошо учиться
Презентация Как помочь ребенку хорошо учиться Курганский филиал РАНХиГС. Основы проекта
Курганский филиал РАНХиГС. Основы проекта Формирование соединений при контактной точечной сварке. (Лекция 4)
Формирование соединений при контактной точечной сварке. (Лекция 4) Информационные технологии в менеджменте качества
Информационные технологии в менеджменте качества Италия. Рим
Италия. Рим Мотивация дошкольников
Мотивация дошкольников Скользящая опалубка
Скользящая опалубка Свидетель эпохи. Жак-Луи Давид
Свидетель эпохи. Жак-Луи Давид Арифметические операции в позиционных системах счисления
Арифметические операции в позиционных системах счисления Роговица. Свойства и функции роговицы
Роговица. Свойства и функции роговицы Вторая фаза метаболизма ксенобиотиков и эндогенных соединений
Вторая фаза метаболизма ксенобиотиков и эндогенных соединений Сухопутные войска, их состав и предназначение
Сухопутные войска, их состав и предназначение Покров Пресвятой Богородицы
Покров Пресвятой Богородицы Проект планировки территории и проект межевания территории
Проект планировки территории и проект межевания территории Понятие, система, задачи, принципы уголовного права. Уголовная политика. Наука уголовного права
Понятие, система, задачи, принципы уголовного права. Уголовная политика. Наука уголовного права Интегрированный урок по химии и географии Почва 8 класс
Интегрированный урок по химии и географии Почва 8 класс 20231029_uroki_stariny_glubokoy
20231029_uroki_stariny_glubokoy Социализация детей с расстройствами аутистического спектра в сюжетно-ролевой игре
Социализация детей с расстройствами аутистического спектра в сюжетно-ролевой игре Бизнес идея создания сувенирной лавки РАЙские сувениры
Бизнес идея создания сувенирной лавки РАЙские сувениры Атеросклероз. Факторы риска
Атеросклероз. Факторы риска Суицид как форма девиантного поведения подростков
Суицид как форма девиантного поведения подростков Выбор марки насосов
Выбор марки насосов Обработка персональных данных
Обработка персональных данных Размещение рекламы в фильме Лицо со шрамом
Размещение рекламы в фильме Лицо со шрамом