Содержание
- 2. Знаете ли Вы…. В 1860 году были известны 60 химических элементов, на сегодняшний день открыты 118
- 3. Знаете ли Вы…. В организме человека около 70 химических элементов в составе простых и сложных веществ
- 4. Знаете ли Вы…. Для изготовления одной лампочки накаливания нужно использовать 7 различных металлов.
- 5. Знаете ли Вы…. Какой химический элемент называют царём «живой» природы, а какой – царём «неживой» природы?
- 6. Знаете ли Вы…. По мнению средневековых алхимиков природа создала 7 металлов по числу планет.
- 7. Знаете ли Вы…. Во время I мировой войны применение ядовитого желто-зеленого газа привело к гибели многих
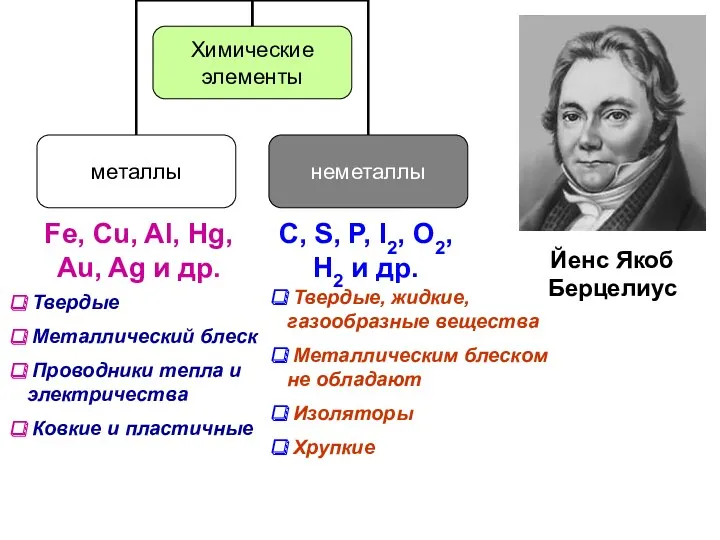
- 8. Fe, Cu, Al, Hg, Au, Ag и др. С, S, P, I2, O2, H2 и др.
- 9. Задание. Даны физические и химические свойства простых веществ. Определите химические элементы, образующие данные вещества.
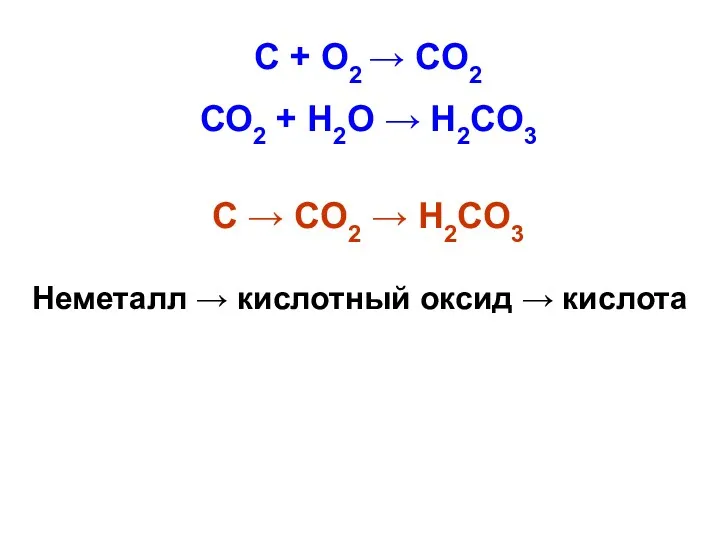
- 10. Неметалл → кислотный оксид → кислота C → CO2 → H2CO3 В 1844 году Г.Дэви и
- 11. C + О2 → CO2 СО2 + Н2О → H2CO3
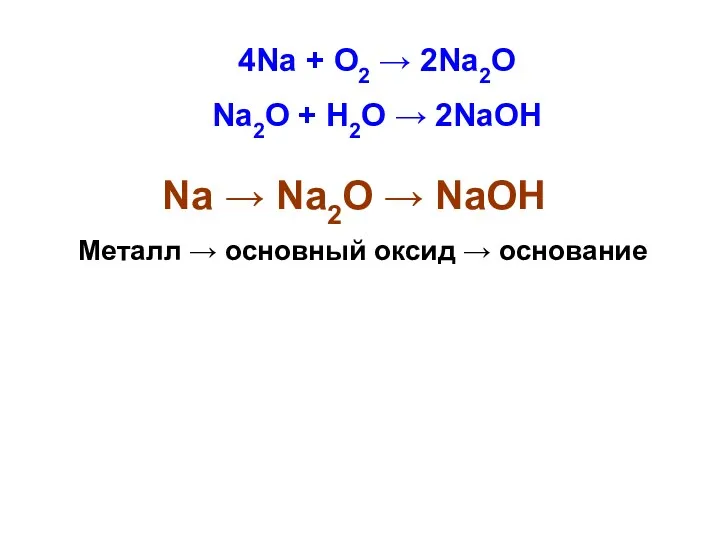
- 12. 4Na + O2 → 2Na2O Na2O + H2O → 2NaOH
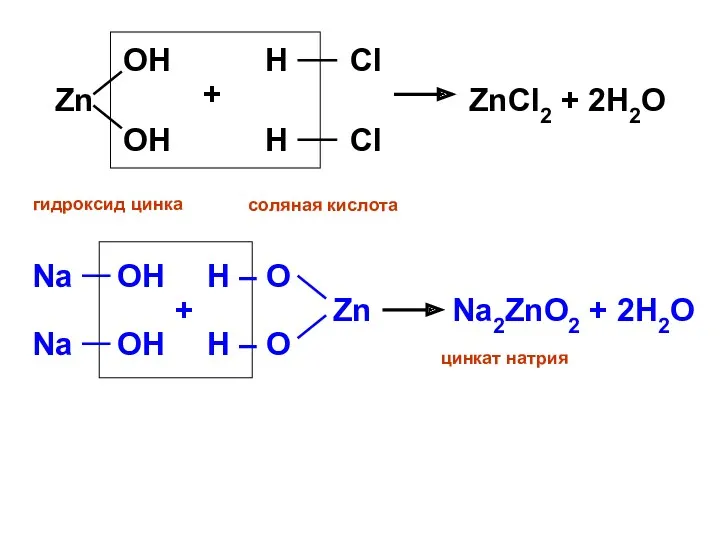
- 14. гидроксид цинка соляная кислота
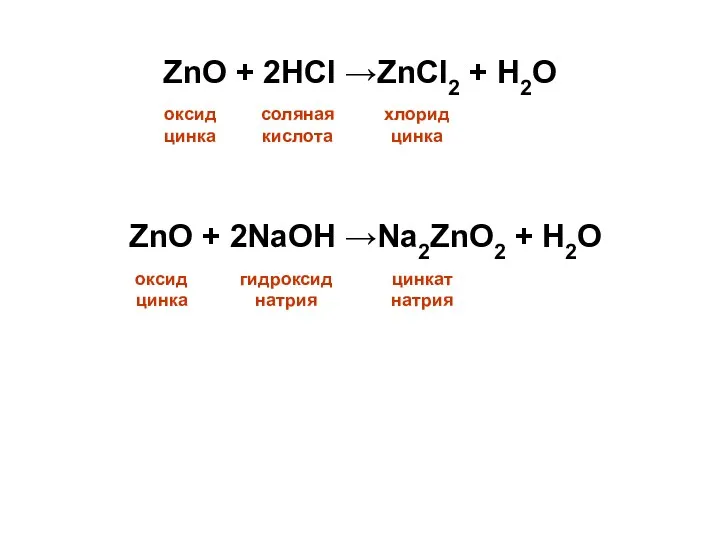
- 15. ZnO + 2NaOH →Na2ZnO2 + H2O оксид цинка гидроксиднатрия цинкат натрия
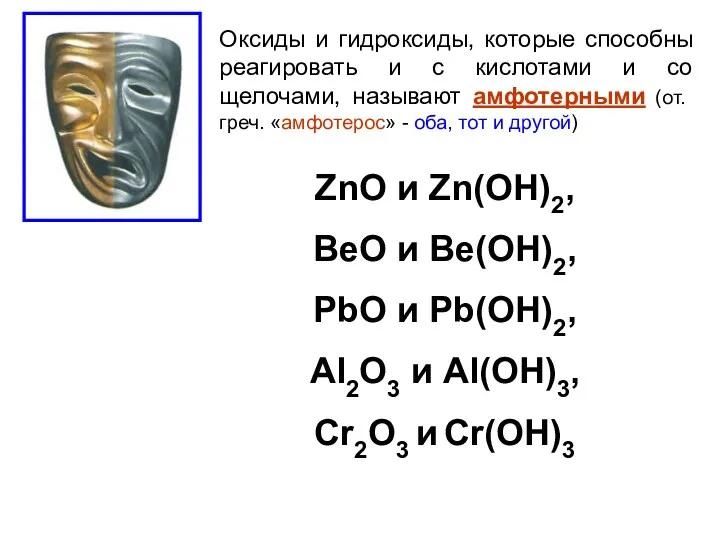
- 16. Оксиды и гидроксиды, которые способны реагировать и с кислотами и со щелочами, называют амфотерными (от. греч.
- 17. Zn, Be, Al, Pb, Cr
- 19. Скачать презентацию






 Внеклассное мерорпиятие Поговорим о доброте
Внеклассное мерорпиятие Поговорим о доброте Урок технологии в 3 классе УМК Перспектива
Урок технологии в 3 классе УМК Перспектива Vegetables
Vegetables Презентация Новогодняя игрушка
Презентация Новогодняя игрушка Кушва - уральский городок
Кушва - уральский городок Обучение сотрудников. Металлопрокат
Обучение сотрудников. Металлопрокат Профилактика травматизма на уроках по легкой атлетике
Профилактика травматизма на уроках по легкой атлетике Ориентирование на местности
Ориентирование на местности Протоколы шин. Дисциплина Структура компьютерных средств Тема №5 Организация шин Занятие №2/2
Протоколы шин. Дисциплина Структура компьютерных средств Тема №5 Организация шин Занятие №2/2 Россия в 1900-1916 гг
Россия в 1900-1916 гг Ряды динамики и их использование в экономике и праве
Ряды динамики и их использование в экономике и праве Понятийный аппарат научного исследования, его содержание и характеристика
Понятийный аппарат научного исследования, его содержание и характеристика Социальное и психическое здоровье
Социальное и психическое здоровье Туркеста́но-Сиби́рская магистра́ль
Туркеста́но-Сиби́рская магистра́ль А.П.Гайдар Тимур и его команда
А.П.Гайдар Тимур и его команда Сердечно-легочная и мозговая реанимация
Сердечно-легочная и мозговая реанимация Конкурсная документация на изготовление торгового оборудования из дерева для магазинов сети СЕМЬЯ
Конкурсная документация на изготовление торгового оборудования из дерева для магазинов сети СЕМЬЯ Атомная энергетика
Атомная энергетика Синдром дефицита внимания и гиперактивности (СДВГ; Attention-Deficit/Hyperactivity Disorder(ADHD)
Синдром дефицита внимания и гиперактивности (СДВГ; Attention-Deficit/Hyperactivity Disorder(ADHD) Развитие персонала
Развитие персонала Технико-экономическое обоснование проекта строительства ВОЛС на участке
Технико-экономическое обоснование проекта строительства ВОЛС на участке Humor pro zle casy
Humor pro zle casy Тест по русскому языку по теме: Имя существительное
Тест по русскому языку по теме: Имя существительное Цунами, его название. Объяснение этого явления
Цунами, его название. Объяснение этого явления Методика обучения с использованием ресурсов компьютерного многоцелевого открытого банка заданий
Методика обучения с использованием ресурсов компьютерного многоцелевого открытого банка заданий Пайка и лужение проводов и наконечников
Пайка и лужение проводов и наконечников Мастер-класс Грибное лукошко
Мастер-класс Грибное лукошко Форма художественного произведения и её основные компоненты
Форма художественного произведения и её основные компоненты