Содержание
- 2. Экспресс опрос класса: 1. Какие элементы называются галогенами? 2. Охарактеризуйте положение галогенов в Периодической системе Д.И.Менделеева.
- 3. Галогеноводороды: HF - фтороводородная кислота ( плавиковая) HCl - хлороводородная кислота (соляная) HBr - бромоводородная кислота
- 4. Почему сила кислоты HJ>HF ? F +53 J +9 2 7 2 8 18 18 7
- 5. Лабораторная работа по теме: «ПОЛУЧЕНИЕ ХЛОРОВОДОРОДА И ИССЛЕДОВАНИЕ ЕГО СВОЙСТВ».
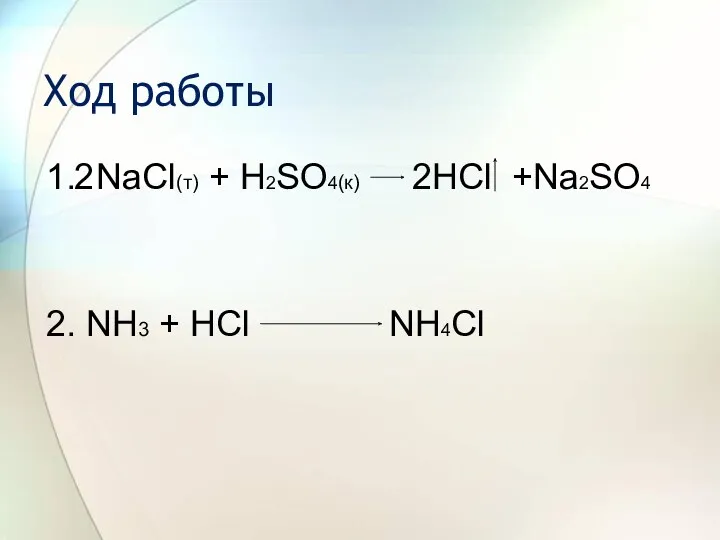
- 6. Ход работы 1. NaCl(т) + H2SO4(к) 2. NH3 + HCl 2HCl +Na2SO4 NH4Cl 2
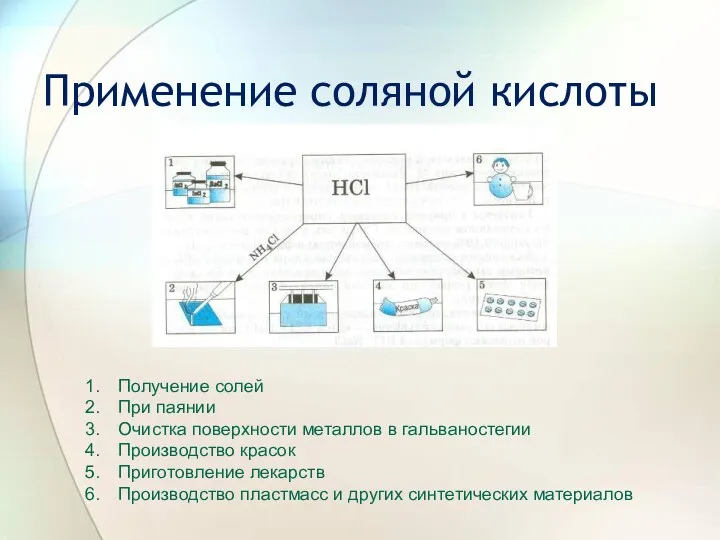
- 7. Применение соляной кислоты Получение солей При паянии Очистка поверхности металлов в гальваностегии Производство красок Приготовление лекарств
- 8. Соли: F фториды CL хлориды хлорид натрия(галит) Br бромиды бромид серебра J йодиды йодид калия фторид
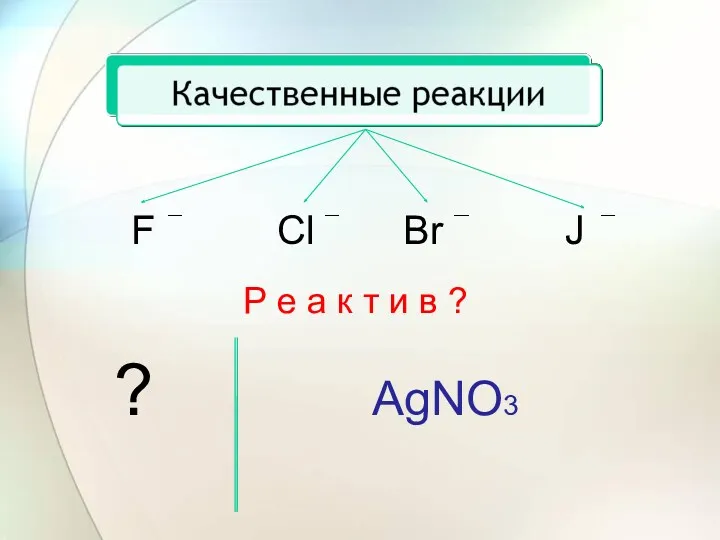
- 9. F Cl Br J Р е а к т и в ? ? AgNO3
- 10. Качественные реакции NaCl + AgNO3 = NaBr + AgNO3 = NaJ + AgNO3 = AgCl +
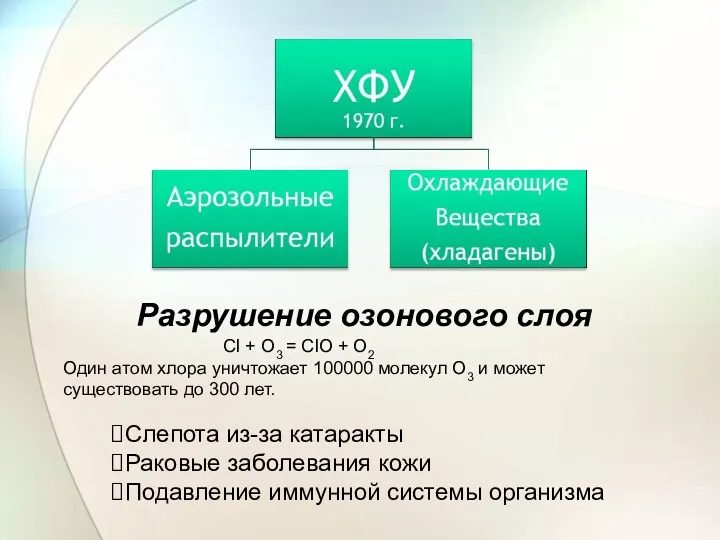
- 11. Разрушение озонового слоя Слепота из-за катаракты Раковые заболевания кожи Подавление иммунной системы организма CI + O3
- 12. Тест по теме: «Галогены и их соединения».
- 13. Ответы на вопросы теста:
- 15. Скачать презентацию








 Воспитательная работа в начальной школе. Мой 4 класс
Воспитательная работа в начальной школе. Мой 4 класс Виды холодильного оборудования
Виды холодильного оборудования Управление качеством
Управление качеством Группы крови
Группы крови Реакция поликонденсации фенолов с формальдегидами
Реакция поликонденсации фенолов с формальдегидами Математический аукцион 9 класс
Математический аукцион 9 класс Юридические лица как субъекты МЧП
Юридические лица как субъекты МЧП Питание. Обучающее интерактивное приложение. 5 - 6 классы
Питание. Обучающее интерактивное приложение. 5 - 6 классы Что такое криоэлектроника
Что такое криоэлектроника Соотношение динамики реального ВВП и реального потребительского спроса (потребительских расходов)
Соотношение динамики реального ВВП и реального потребительского спроса (потребительских расходов) Пароконвектоматы фирмы UNOX итальянского производства
Пароконвектоматы фирмы UNOX итальянского производства Spa программы
Spa программы Добро пожаловать в ООО Газпром питание
Добро пожаловать в ООО Газпром питание Острое повреждение почек. Функции почек
Острое повреждение почек. Функции почек Объем перевозок и грузооборот
Объем перевозок и грузооборот Презентация Что не так?
Презентация Что не так? Поэма М.Ю. Лермонтова Мцыри
Поэма М.Ю. Лермонтова Мцыри Спортивное волонтерство
Спортивное волонтерство Обмен белков
Обмен белков М.М. Сперанский
М.М. Сперанский Заслуги ученых, развитие микробиологии, этапы развития микробиологии
Заслуги ученых, развитие микробиологии, этапы развития микробиологии И. Токмакова Мы играли в хохотушки, Я. Тайц Волк, Г. Кружков РРРы!
И. Токмакова Мы играли в хохотушки, Я. Тайц Волк, Г. Кружков РРРы! Основы экономики. Деньги
Основы экономики. Деньги Пропаганда трезвости в современном мире
Пропаганда трезвости в современном мире Принципы трудового права
Принципы трудового права Фото презентация по теме Я-классный руководитель
Фото презентация по теме Я-классный руководитель Стандартные исследования образцов горных пород
Стандартные исследования образцов горных пород Выступление на РМО учителей начальных классов
Выступление на РМО учителей начальных классов