Слайд 2
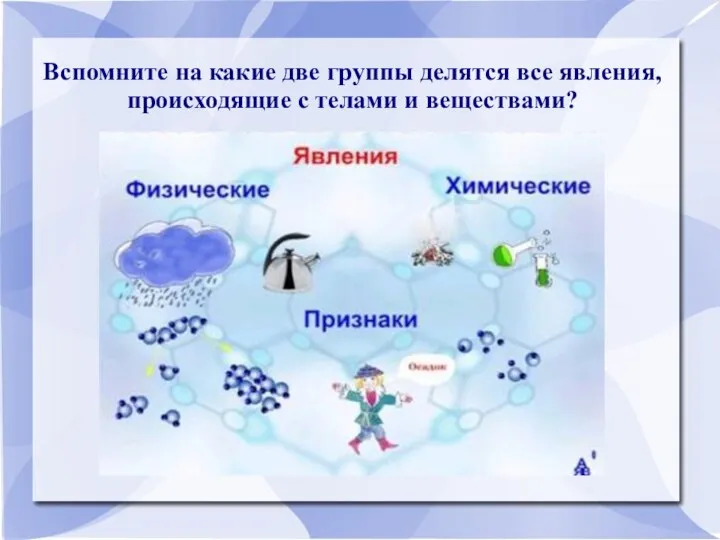
Вспомните на какие две группы делятся все явления, происходящие с телами
и веществами?
Слайд 3

Какие признаки химических реакций вы знаете?
Слайд 4

Какие условия должны выполняться,чтобы произошла химическая реакция?
Необходимо,чтобы реагирующие вещества соприкоснулись.
Нагревание.
Электрический ток
или свет.
Слайд 5

“Все изменения,которые случаются в действительности,находятся в таком состоянии,что сколь от одного
тела отнимается,столько прибавляется к другому,так что где убудет немного материи,то умножится в другом месте”
М.В.Ломоносов(1756г)
Слайд 6

Современная формулировка закона сохранения массы веществ:
Масса веществ,вступивших в химическую реакцию,равна массе
веществ,получившихся в результате её.
Слайд 7

На основании закона сохранения массы веществ составляют уравнения химических реакций
Слайд 8

Запишите уравнение:
железо+сера=сульфид железа(II)
Fe+S=FeS
Слайд 9

Алгоритм расстановки коэффициентов в уравнениях химических реакций
Подсчитать количество атомов каждого элемента
в правой и левой части уравнения химической реакции.
Определить, у какого элемента количество атомов меняется, найти НОК.
Разделить НОК на индексы – получить коэффициенты. Поставить их перед формулами.
Пересчитать количество атомов, при необходимости действие повторить.
Последним проверить количество атомов кислорода.
Слайд 10

Расставьте коэффициенты в уравнениях химических реакций:
1) KCLO3→KCL+O2
2) Na+Cl2→NaCl
3) KNO3→KNО2+O2
4) H2O+SO3→H2SO4
5) Al+S→Al2S3
6) H2O2→H2O+O2
7) Rb2O+H2O→RbOH
8) Ba+O2→BaO
Слайд 11

Домашнее задание:
параграф 27 стр139-145,упражнение1; расставьте коэффициенты в уравнениях реакций:
P + Cl2
→ PCl5
Na + S → Na2S
HCl + Mg → MgCl2 + H2
N2 + H2 → NH3
H2O → H2 + O2










 Патология зрительной системы
Патология зрительной системы Технология ручной дуговой сварки
Технология ручной дуговой сварки электро магнитное реле
электро магнитное реле Классный час. Планета Здоровье.
Классный час. Планета Здоровье. Поздравления с 8 марта
Поздравления с 8 марта Текстовый процессор Word 2007. Дополнительные возможности
Текстовый процессор Word 2007. Дополнительные возможности Подготовка к ЕГЭ. Царство животные
Подготовка к ЕГЭ. Царство животные Проект Красивая речь. В гостях у Говоруши. Учимся рассказывать по сюжетным картинкам
Проект Красивая речь. В гостях у Говоруши. Учимся рассказывать по сюжетным картинкам Лекарственные растения
Лекарственные растения HELLP – синдром
HELLP – синдром Презентация для классного часа на тему 25 лет со дня выхода войск из Афганистана
Презентация для классного часа на тему 25 лет со дня выхода войск из Афганистана Разработка автоматизированной системы учета заказов на кондитерские изделия
Разработка автоматизированной системы учета заказов на кондитерские изделия Формирование базовых учебных действий у обучающихся с умственной отсталостью
Формирование базовых учебных действий у обучающихся с умственной отсталостью Рождественское печенье
Рождественское печенье Празднование Святок.
Празднование Святок. Образовательный проект Вместе в космос полетим!
Образовательный проект Вместе в космос полетим! Электронный микроскоп
Электронный микроскоп s
s Гонорея. Гонорея девочек. ВИЧ-инфекция, кожные проявления. Профилактика венерических болезней и ВИЧ-инфекции
Гонорея. Гонорея девочек. ВИЧ-инфекция, кожные проявления. Профилактика венерических болезней и ВИЧ-инфекции Педагогическое общение
Педагогическое общение Математическое и имитационное моделирование
Математическое и имитационное моделирование Цели автоматизации организации, задачи и функции ИС
Цели автоматизации организации, задачи и функции ИС Признаки делимости на 3 и на 9
Признаки делимости на 3 и на 9 Жасуша патофизиологиясы
Жасуша патофизиологиясы презентация защита программы воспитательной работа 1-4
презентация защита программы воспитательной работа 1-4 Горячее водоснабжение
Горячее водоснабжение Знакомство с конвенциях о правах ребенка
Знакомство с конвенциях о правах ребенка Системно-деятельностный подход как методологическая основа Федерального Гос Образовательного Стандарта начального образования
Системно-деятельностный подход как методологическая основа Федерального Гос Образовательного Стандарта начального образования