Содержание
- 2. Девиз урока : « Жить – значит узнавать» S
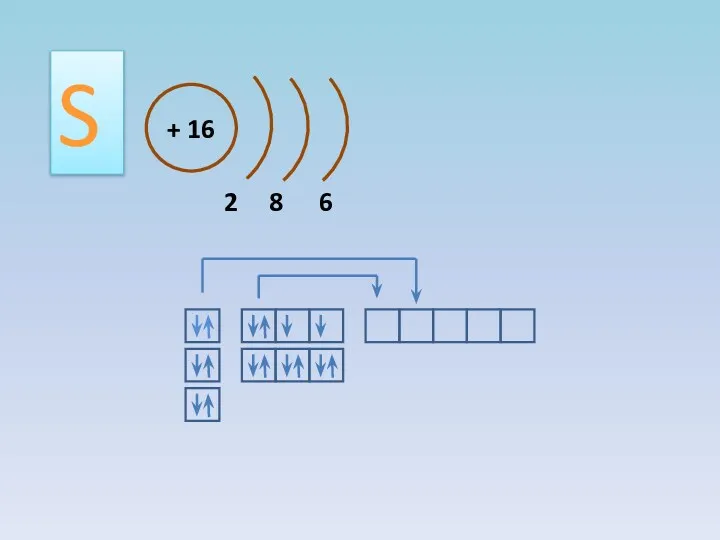
- 3. + 16 2 8 6 S
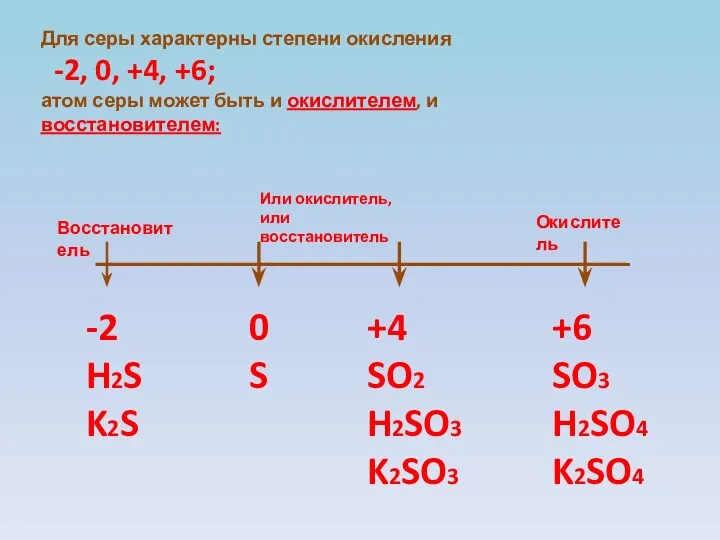
- 4. Для серы характерны степени окисления -2, 0, +4, +6; атом серы может быть и окислителем, и
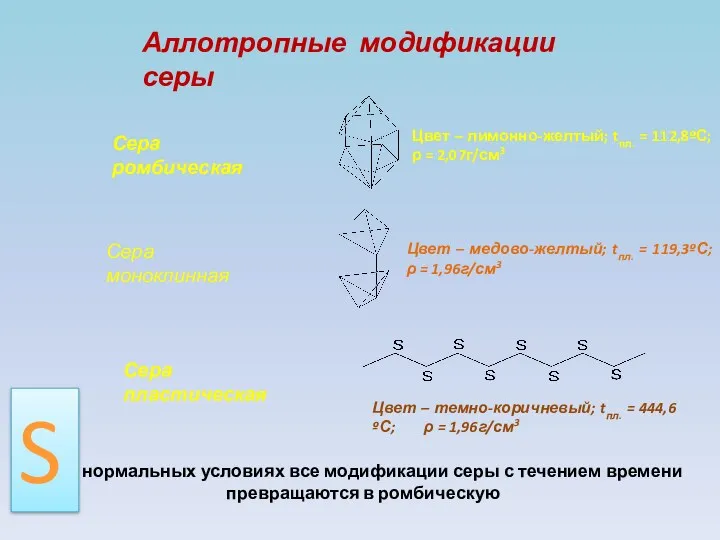
- 5. Сера ромбическая Сера пластическая Сера моноклинная Цвет – лимонно-желтый; tпл. = 112,8ºС; ρ = 2,07г/см3 Цвет
- 6. У жёлтой серы есть корона, Но нет ни подданных, ни трона. Корону сера надевает, Когда устойчивой
- 7. В природе сера встречается в трёх формах самородная сульфидная сульфатная
- 8. О каких соединениях серы упоминал А.С.Пушкин в стихотворении, написанном в 1832г.? Тогда услышал я (о диво)
- 9. Химические свойства серы S 1. Взаимодействие с металлами. 2 1 восстановитель окислитель
- 10. Взаимодействие серы с натрием (видеоопыт) http://files.school-collection.edu.ru/dlrstore/3e6b77cf-8fff-882a-d3c3-c50221c6eba9/index.htm
- 11. 2.Взаимодействие с водородом 1 1 окислитель восстановитель S
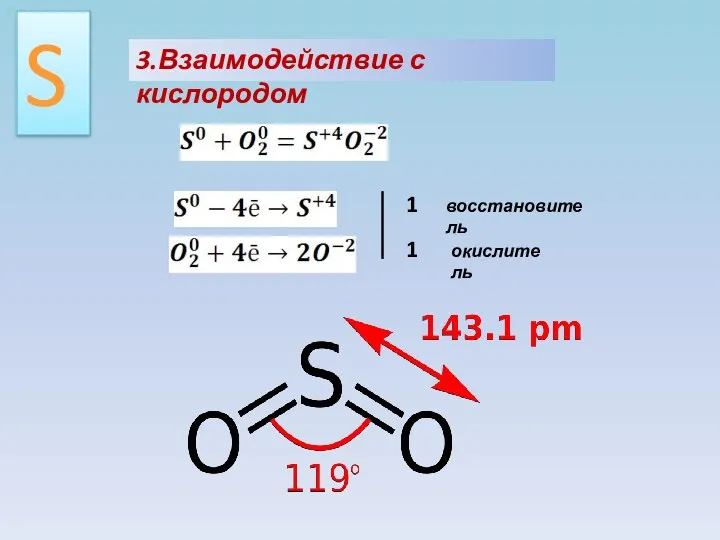
- 12. 3.Взаимодействие с кислородом S 1 1 восстановитель окислитель
- 13. Диоксид серы – загрязнитель атмосферы
- 14. S
- 15. Уравнение реакции, в котором сера является окислителем: А. Zn + S → ZnS Б. 2SO2 +
- 17. Скачать презентацию








 Классный час Ежели Вы вежливы
Классный час Ежели Вы вежливы Система питания двигателя от впрыска топлива
Система питания двигателя от впрыска топлива физкультминутки
физкультминутки Социально-экономическое развитие Руси в XI веке
Социально-экономическое развитие Руси в XI веке Болезни желудка и двенадцатиперстной кишки
Болезни желудка и двенадцатиперстной кишки Презентация Наши земляки - Герои Советского Союза (О брасовцах)
Презентация Наши земляки - Герои Советского Союза (О брасовцах) Презентация к празднику День матери Диск
Презентация к празднику День матери Диск Презентация к занятию Давайте разберемся! (программа Планета здоровья)
Презентация к занятию Давайте разберемся! (программа Планета здоровья) Дошкольное образование в Великобритании.
Дошкольное образование в Великобритании. Налог на имущество физических лиц
Налог на имущество физических лиц CREDO бағдарламасы. Konverter
CREDO бағдарламасы. Konverter обобщение знаний по теме Главные особенности природы Земли презентация
обобщение знаний по теме Главные особенности природы Земли презентация Предпринимательство. Защита нематериальных благ. Причинение и возмещение вреда
Предпринимательство. Защита нематериальных благ. Причинение и возмещение вреда Урок Земля отцов - моя земля!
Урок Земля отцов - моя земля! Хранение лекарственных средств
Хранение лекарственных средств Родительское собрание Подростковый алкоголизм
Родительское собрание Подростковый алкоголизм Текст и предложение
Текст и предложение Диалог между верами в целях религиозного плюрализма
Диалог между верами в целях религиозного плюрализма Презентация для работы гражданско-патриотического клуба Моя Россия
Презентация для работы гражданско-патриотического клуба Моя Россия ОСОБЕННОСТИ РАЗВИТИЯ И ВОСПИТАНИЯ ДЕТЕЙ ОТ 3 ДО 4 ЛЕТ
ОСОБЕННОСТИ РАЗВИТИЯ И ВОСПИТАНИЯ ДЕТЕЙ ОТ 3 ДО 4 ЛЕТ Дидактические системы и модели обучения, факторы и цели
Дидактические системы и модели обучения, факторы и цели Рождество
Рождество Организация медицинской помощи сельскому населению
Организация медицинской помощи сельскому населению Урок химии для 8 класса на тему Ковалентная связь.ФГОС.
Урок химии для 8 класса на тему Ковалентная связь.ФГОС. России милый уголок (презентация)
России милый уголок (презентация) Компьютерная графика
Компьютерная графика Ортопедиялық стоматологияда қолданылатын анестезия препараттары. Олардың сипаттамасы
Ортопедиялық стоматологияда қолданылатын анестезия препараттары. Олардың сипаттамасы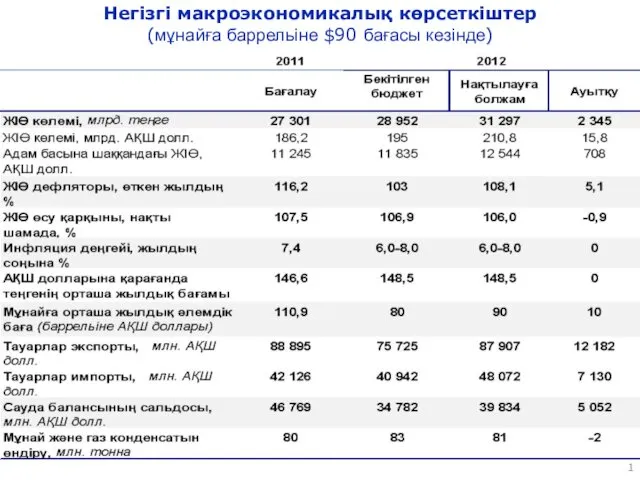 Негізгі макроэкономикалық көрсеткіштер (мұнайға баррельіне $90 бағасы кезінде)
Негізгі макроэкономикалық көрсеткіштер (мұнайға баррельіне $90 бағасы кезінде)