Слайд 2

План урока:
Место данной темы в современной науке;
Теории растворов;
Образование кристаллов;
Классификация растворов.
Слайд 3

Почему мы изучаем растворы?
Растворы играют важную роль в природе, науке
и технике:
Вода (особенно морская) содержит до 3,5% растворенных солей;
Кровь нашего организма содержит до 0,9% солей;
Усвоение пищи связано с переводом питательных веществ в раствор;
Природные водные растворы участвуют в процессах почвообразования и снабжают растительный организм питательными веществами;
Получение соды, удобрений, бумаги, кислот, металлов и т.д. протекает в растворах.
Слайд 4

Вывод:
Изучение растворов занимает важное место в современной науке
Слайд 5

Теории растворов:
Физическая теория
(В.Оствальд, С.Аррениус, Я.Вант-Гофф)
Слайд 6

Сторонники теории под раствором понимали однородные смеси, состоящие из двух или
более однородных частей.
Они считали, что растворение является результатом проникновения растворенного вещества в промежутки между молекулами воды.
Слайд 7

2. Химическая теория (Менделеев)
Сторонники теории доказывали, что растворение является результатом химического
взаимодействия растворенного вещества с молекулами воды
Слайд 8

Как вы считаете, какая из этих теорий верна?
Слайд 9

3. Физико-химическая теория (современная точка зрения)
Теорию эту предсказал сам Д.И.Менделеев в
своем знаменитом учебнике «Основы химии» в 1906 г.:
«Две указанные стороны растворения и гипотезы, до сих пор приложенные к рассмотрению растворов, хотя имеют отчасти различные исходные точки, но без всякого сомнения, по всей вероятности, приведут к общей теории растворов, потому что одни общие законы управляют как физическими, так и химическими явлениями».
Слайд 10

Исходя из физико-химической теории растворов определение выглядит следующим образом:
Раствор - это
однородная система, состоящая из частиц растворенного вещества, растворителя и продуктов их взаимодействия.
Слайд 11

При взаимодействии растворенного вещества с водой образуются гидраты.
Гидраты – непрочные соединения
веществ с водой, существующие в растворе.
Процесс образования гидратов называют гидратацией.
Как доказать их образование?
Слайд 12

Кристаллогидраты – это вещества кристаллической природы, в состав которых входит вода.
Ее
в такой случае называют кристаллизационной.
Например,
CuSO4 * 5H2O – пятиводный сульфат меди (II), или медный купорос;
Na2CO3 * 2H2O – двухводный карбонат натрия, или сода;
CaSO4 * 2H2O – двухводный сульфат кальция, или гипс.
Слайд 13

Получение медного купороса
CuSO4 + H2O CuSO4 * 5H2O
Белый порошок Синие
кристаллы
Слайд 14

Слайд 15

Классификация растворов
По агрегатному состоянию:
Твердые (сплавы);
Газообразные (воздух);
Жидкие
Слайд 16
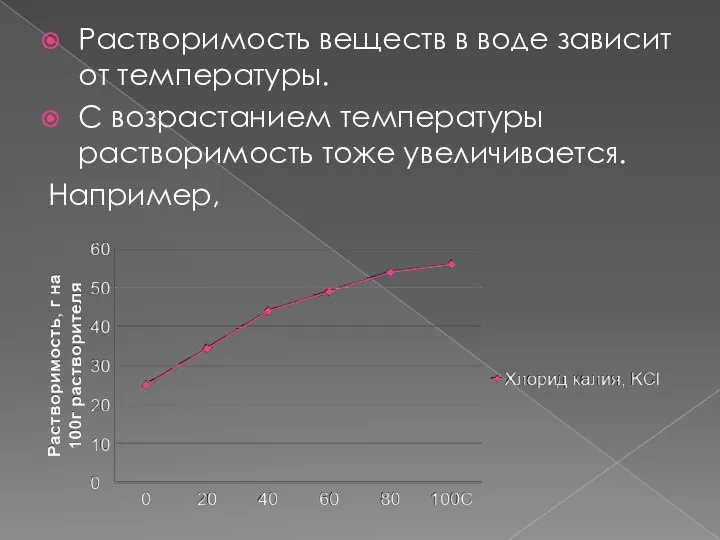
Растворимость веществ в воде зависит от температуры.
С возрастанием температуры растворимость тоже
увеличивается.
Например,
Слайд 17

2. По растворимости твердого вещества в воде:
Насыщенные – растворы, в которых
при данной температуре вещество больше не растворяется;
Ненасыщенные – растворы, в которых при данной температуре находится меньше растворяемого вещества, чем в его насыщенном растворе;
Пересыщенные – растворы, в которых при данной температуре находится в растворенном состоянии больше вещества, чем в его насыщенном растворе при тех же условиях.
Слайд 18

По их растворимости все вещества делят на:
Хорошо растворимые (более
1 г на 100 г воды);
Малорастворимые (менее 1 г на 100 г воды);
Нерастворимые (менее 0,01 г на 100 г воды).
Слайд 19

Домашнее задание:
Параграф 34


















 Древесина – конструкционный материал
Древесина – конструкционный материал Презентация История кружева
Презентация История кружева Виды, способы и техника лепки в детском саду
Виды, способы и техника лепки в детском саду Методичская разработка открытого урока для специальности 230115 по дисциплине Основы программирования
Методичская разработка открытого урока для специальности 230115 по дисциплине Основы программирования Использование перфокарт в работе с дошкольниками
Использование перфокарт в работе с дошкольниками Ассоциация военно-патриотических клубов. ВПК Гвардия Иланский район
Ассоциация военно-патриотических клубов. ВПК Гвардия Иланский район ВКР: Техническое обслуживание электроприводов участка формовки трубы ТЭСЦ – 3
ВКР: Техническое обслуживание электроприводов участка формовки трубы ТЭСЦ – 3 О проведении Всероссийской олимпиады школьников по вопросам избирательного права и избирательного процесса
О проведении Всероссийской олимпиады школьников по вопросам избирательного права и избирательного процесса Необычные растения и животные в природе.
Необычные растения и животные в природе. Вышивание крестиком Диск
Вышивание крестиком Диск Защита малых рек
Защита малых рек Совершенствование логистических процессов на складах транспортного предприятия
Совершенствование логистических процессов на складах транспортного предприятия Презентации для урочной и внеурочной деятельности
Презентации для урочной и внеурочной деятельности Презентация к уроку природоведения ПРИЗНАКИ ЖИВОТНЫХ 5 класс
Презентация к уроку природоведения ПРИЗНАКИ ЖИВОТНЫХ 5 класс Humour toujours
Humour toujours презентация 2 февраля-Сталинградская битва
презентация 2 февраля-Сталинградская битва Трудовое право. Понятие, предмет и метод
Трудовое право. Понятие, предмет и метод Игра 4 лишний
Игра 4 лишний Конспект занятия математического кружка Старинные задачи на дроби
Конспект занятия математического кружка Старинные задачи на дроби Энергия от ветра
Энергия от ветра Паровая ТЭС
Паровая ТЭС Новое в правовом регулировании градостроительной деятельности
Новое в правовом регулировании градостроительной деятельности Суицид как форма девиантного поведения подростков
Суицид как форма девиантного поведения подростков Компьютерные вирусы
Компьютерные вирусы Северная война (1700-1721)
Северная война (1700-1721) Микеланджело Буонарроти - краткая биография и картины
Микеланджело Буонарроти - краткая биография и картины Новая мотивация
Новая мотивация Моніторинг і коментарі до нормативно-правових актів у сфері оподаткування, грудень 2016 ч1
Моніторинг і коментарі до нормативно-правових актів у сфері оподаткування, грудень 2016 ч1