Слайд 2

Тема урока «Водород»
План урока
1. Водород в природе.
2. Историческая справка.
3. Водород –
химический элемент.
4. Водород – простое вещество.
5. Получение и собирание водорода.
6. Физические свойства водорода.
7. Применение водорода.
Слайд 3

Водород в природе.
Первый я на белом свете:
Во вселенной, на
планете
Превращаюсь в лёгкий гелий,
Зажигаю Солнце в небе.
Гость из космоса пришёл
В воде приют себе нашёл!
(Объясните смысл этого стихотворения изучив материал учебника нахождение водорода в природе стр. 71)
Слайд 4
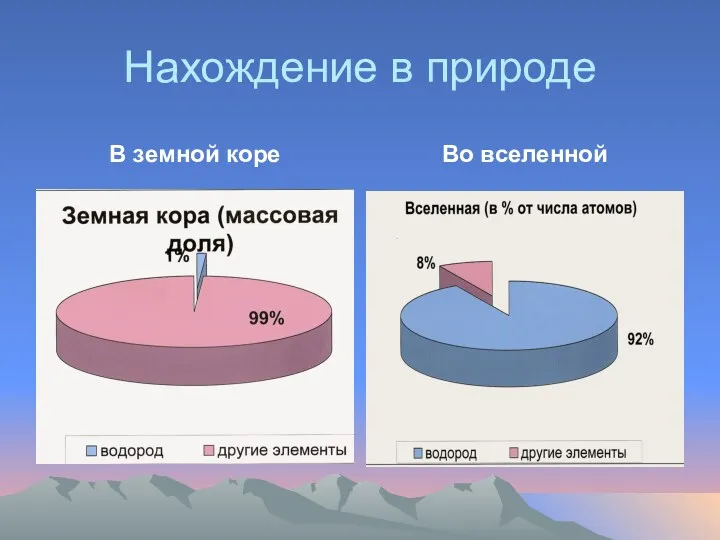
Нахождение в природе
В земной коре
Во вселенной
Слайд 5

Исторические сведения
Водород был известен ещё в XVI веке Теофрасту Парацельсу (1493-1541)
Его
получали Ван-Гельмонт(1577-1644),
Роберт Бойль (1627-1691),
Николя Лемери (1645-1715),
Михаил Васильевич Ломоносов (1711-1765),
Джозеф Пристли и др.
Слайд 6

Всё те же открытия.
В 1766 году известный английский учёный Генри Кавендиш
получил «искусственный воздух» действием цинка на разведённую соляную кислоту. Это было совершенно новое вещество, которое хорошо горело и получило название «горючего воздуха»
Слайд 7

Открытие водорода
Лишь в 1787 году Антуан Лавуазье доказал, что «горючий воздух»,открытый
в 1766 году входит в состав воды и дал ему название «гидрогениум», т.е. «рождающий воду», «водород».
Слайд 8

Водород – химический элемент.
Характеристика водорода по периодической системе.
1. Порядковый
номер.
2. Номер периода.
3. Номер группы.
4. Относительная атомная масса.
5. Валентность водорода.
Слайд 9

Водород – простое вещество.
Н2
Слайд 10

Водород как простое вещество и как химический элемент
Слайд 11

Ответьте на вопрос.
Если бы перед вами стояла задача получить большое количество
водорода, какое сырьё вы бы выбрали и почему?
Слайд 12

Получение водорода из воды с помощью солнечной энергии
Слайд 13

Получение водорода
В промышленности :
2СН4 + О2 = 2СО + 4Н2
↑
2H2O = 2H2 ↑ + O2 ↑
В лаборатории :
Zn + H2SO4 = ZnSO4 + H2↑
Слайд 14

Получение водорода в лаборатории
Слайд 15
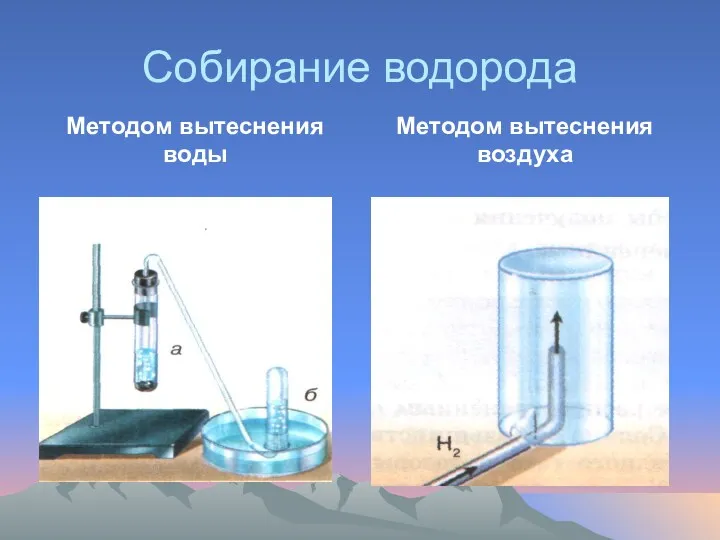
Собирание водорода
Методом вытеснения воды
Методом вытеснения воздуха
Слайд 16

Слайд 17

Образование гремучей смеси
Обычно лёгок и летуч,
Он вдруг становится могуч:
Его нагрев неосторожно
Взорвать
в округе всё возможно.
Слайд 18

Физические свойства водорода
Лёгкий горючий газ без цвета, запаха и вкуса.
Температура плавления
-259,15
Температура кипения -252,7
Плохо растворим в воде.
Слайд 19

Некоторые области применения водорода
Слайд 20

Применение водорода
Водородом заполняли дирижабли вплоть до 1937 года, пока не взорвался
немецкий дирижабль «Гинденбург». Погибло 36 человек. Размеры дирижабля достигали размеров двух футбольных полей.
Слайд 21

Водород в качестве горючего
Слайд 22

Водород – аккумулятор энергии
Слайд 23

Если вы согласны с утверждениями, поставьте плюс.
1. Я узнал много нового
и интересного.
2. На все возникшие в ходе урока вопросы я получил ответы.
3. Мне это пригодится в будущей профессиональной деятельности и в повседневной жизни.
4. Считаю, что работал добросовестно и достиг цели урока.






















 Метод проектов, как образовательная технология. (Лекции 5, 6)
Метод проектов, как образовательная технология. (Лекции 5, 6) Правовая природа и Порядок государственной регистрации хозяйствующих субъектов
Правовая природа и Порядок государственной регистрации хозяйствующих субъектов Полисахариды. Целлюлоза
Полисахариды. Целлюлоза Измерение вибрации и частоты вращения механизмов, физико-химических свойств и состава жидкостей и газов
Измерение вибрации и частоты вращения механизмов, физико-химических свойств и состава жидкостей и газов Стиль канзаши
Стиль канзаши 20231218_urok_diskoteka
20231218_urok_diskoteka Уголовный кодекс Республики Казахстан
Уголовный кодекс Республики Казахстан Архаикалық мәдениеттегі діннің алғашқы формалары
Архаикалық мәдениеттегі діннің алғашқы формалары Профессионально-этические основы социальной работы
Профессионально-этические основы социальной работы Антарктида. Тест.
Антарктида. Тест. Древнейшие люди
Древнейшие люди Презентация урока: Экологические и водные проблемы Поволжья по географии 9 класса
Презентация урока: Экологические и водные проблемы Поволжья по географии 9 класса Залесские земли.
Залесские земли. Изучаем головные уборы
Изучаем головные уборы Методика Профессиональная готовность
Методика Профессиональная готовность Комплексная игровая площадка в микрорайоне Орский городок
Комплексная игровая площадка в микрорайоне Орский городок A l’école
A l’école Принципы работы стипендиальных комиссий в образовательных организациях
Принципы работы стипендиальных комиссий в образовательных организациях Управление финансами. Теория и практика. Книжная выставка
Управление финансами. Теория и практика. Книжная выставка Противоэпидемические мероприятия в очагах с фекальнооральным механизмом передачи
Противоэпидемические мероприятия в очагах с фекальнооральным механизмом передачи проект Люди вокруг нас
проект Люди вокруг нас Пр. додел (1)
Пр. додел (1) Как помочь ребенку в подготовке дом. заданий
Как помочь ребенку в подготовке дом. заданий Планирование деятельности предприятия (часть II). Лекция 10
Планирование деятельности предприятия (часть II). Лекция 10 Испытания РЭА на повреждающую нагрузку
Испытания РЭА на повреждающую нагрузку Структурно-функциональная организация дыхательной системы. Этапы дыхания. Регуляция дыхания
Структурно-функциональная организация дыхательной системы. Этапы дыхания. Регуляция дыхания Measurement automation in laboratory physical modeling of seismic data
Measurement automation in laboratory physical modeling of seismic data Презентация Времена года
Презентация Времена года