Содержание
- 2. Алгоритм расстановки коэффициентов в ОВР методом электронного баланса Запишите схему реакции: C + HNO3 → CO2
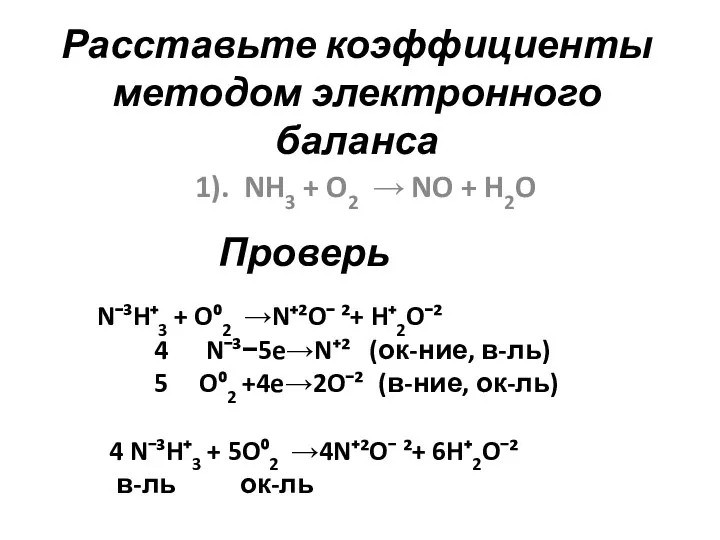
- 3. Расставьте коэффициенты методом электронного баланса 1). NH3 + O2 → NO + H2O N⁻³H⁺3 + O⁰2
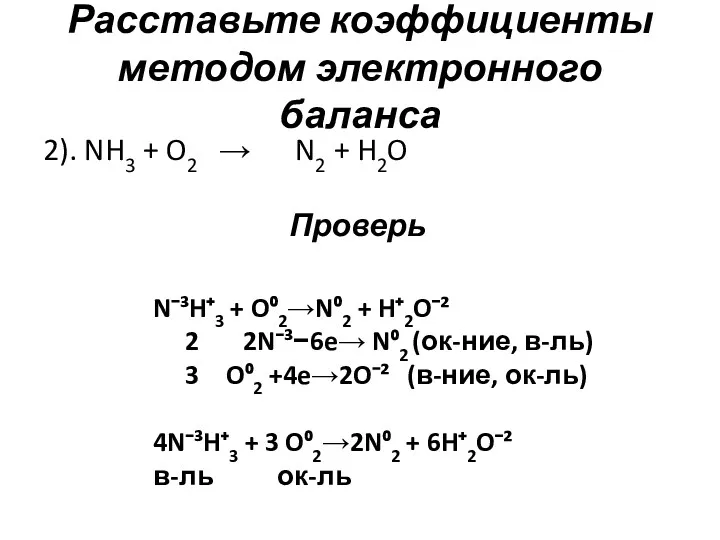
- 4. Расставьте коэффициенты методом электронного баланса 2). NH3 + O2 → N2 + H2O Проверь N⁻³H⁺3 +
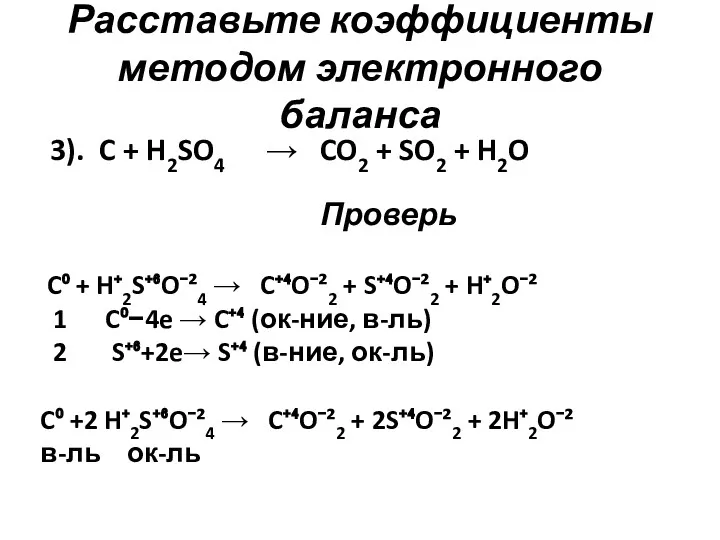
- 5. Расставьте коэффициенты методом электронного баланса 3). C + H2SO4 → CO2 + SO2 + H2O Проверь
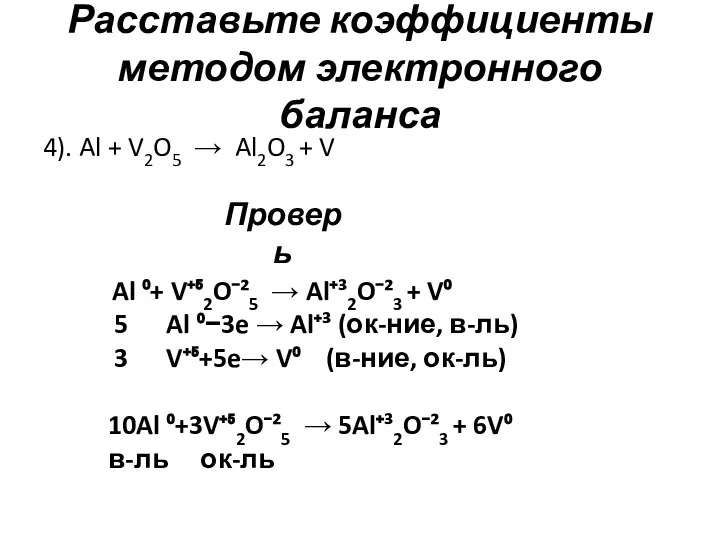
- 6. Расставьте коэффициенты методом электронного баланса 4). Al + V2O5 → Al2O3 + V Проверь Al ⁰+
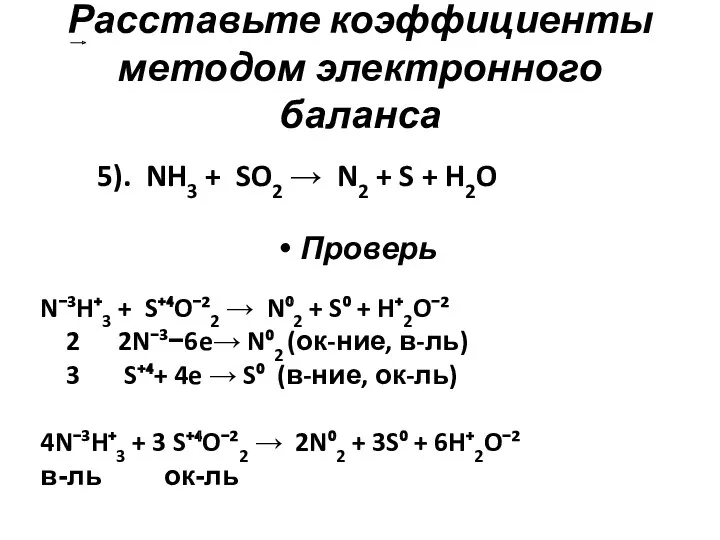
- 7. Расставьте коэффициенты методом электронного баланса Проверь 5). NH3 + SO2 → N2 + S + H2O
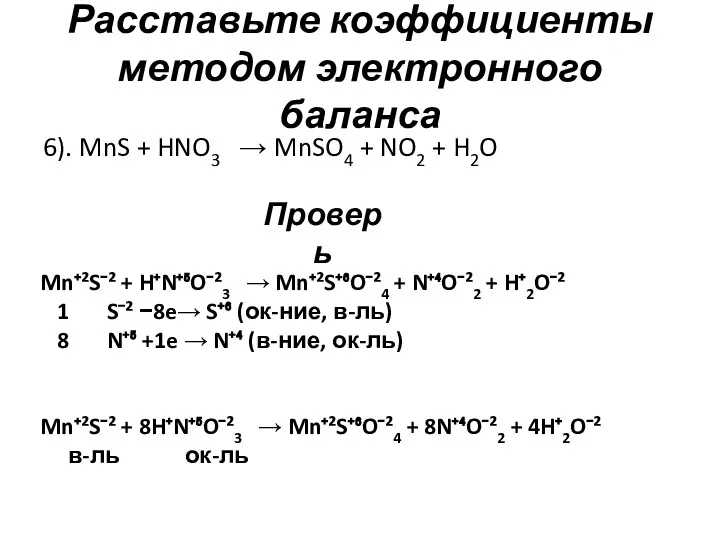
- 8. Расставьте коэффициенты методом электронного баланса 6). MnS + HNO3 → MnSO4 + NO2 + H2O Проверь
- 9. Расставьте коэффициенты методом электронного баланса 7). ZnS + O2 → ZnO + SO2 Проверь Zn⁺²S⁻² +
- 10. Расставьте коэффициенты методом электронного баланса 8). KI + Cu(NO3)2 → CuI + I2 + KNO3 Проверь
- 11. Расставьте коэффициенты методом электронного баланса 9). FeCl3 + H2S→ FeCl2 + S + HCl Проверь Fe⁺³Cl⁻3
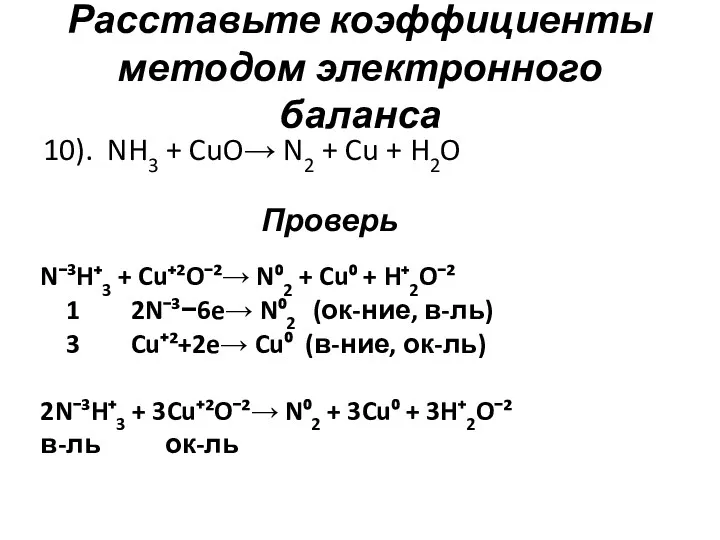
- 12. Расставьте коэффициенты методом электронного баланса 10). NH3 + CuO→ N2 + Cu + H2O Проверь N⁻³H⁺3
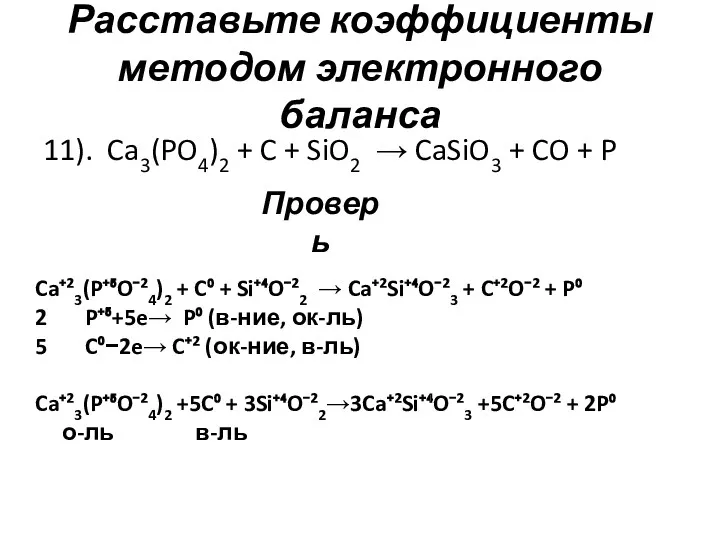
- 13. Расставьте коэффициенты методом электронного баланса 11). Ca3(PO4)2 + C + SiO2 → CaSiO3 + CO +
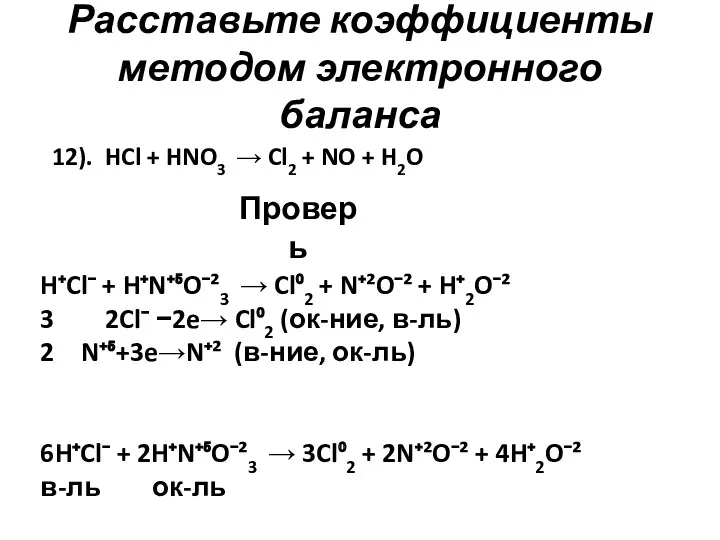
- 14. Расставьте коэффициенты методом электронного баланса 12). HCl + HNO3 → Cl2 + NO + H2O Проверь
- 15. Расставьте коэффициенты методом электронного баланса 13). CrO3 + H2S + H2SO4 →Cr2(SO4)3 + S + H2O
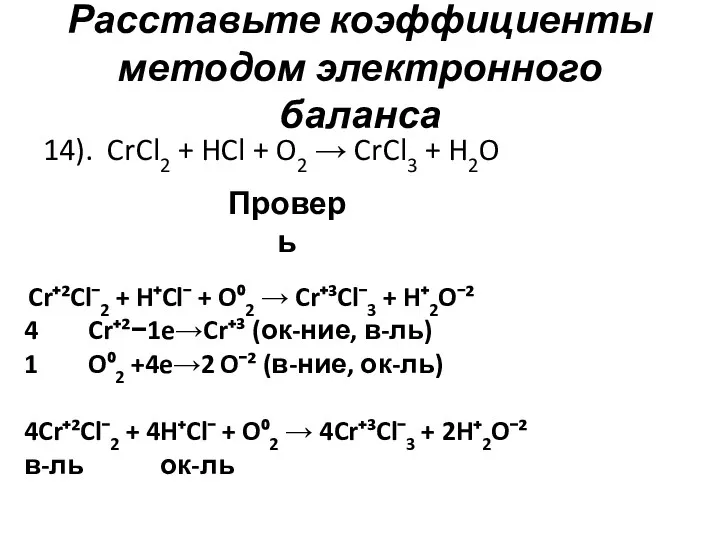
- 16. Расставьте коэффициенты методом электронного баланса 14). CrCl2 + HCl + O2 → CrCl3 + H2O Проверь
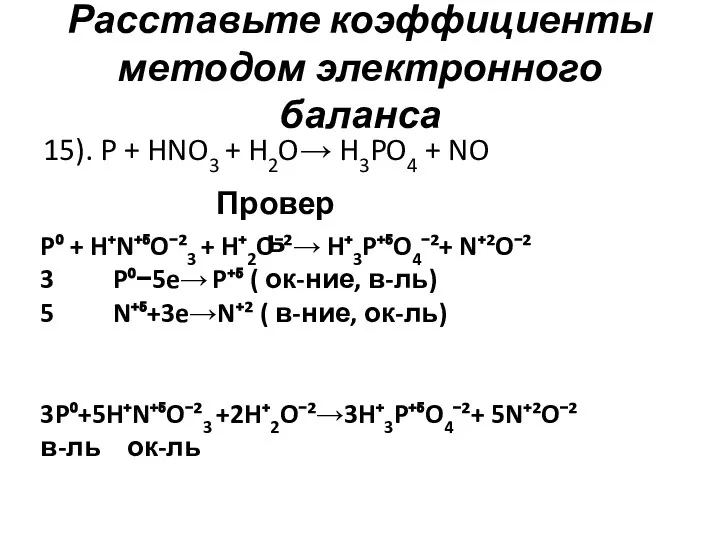
- 17. Расставьте коэффициенты методом электронного баланса 15). P + HNO3 + H2O→ H3PO4 + NO Проверь P⁰
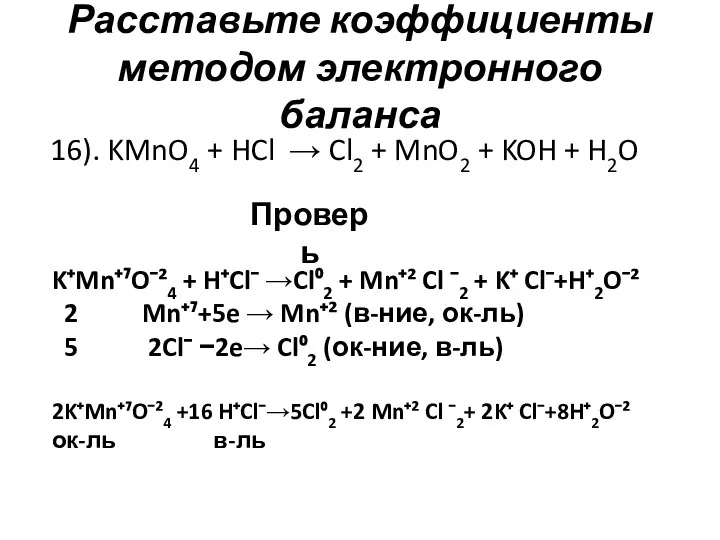
- 18. Расставьте коэффициенты методом электронного баланса 16). KMnO4 + HCl → Cl2 + MnO2 + KOH +
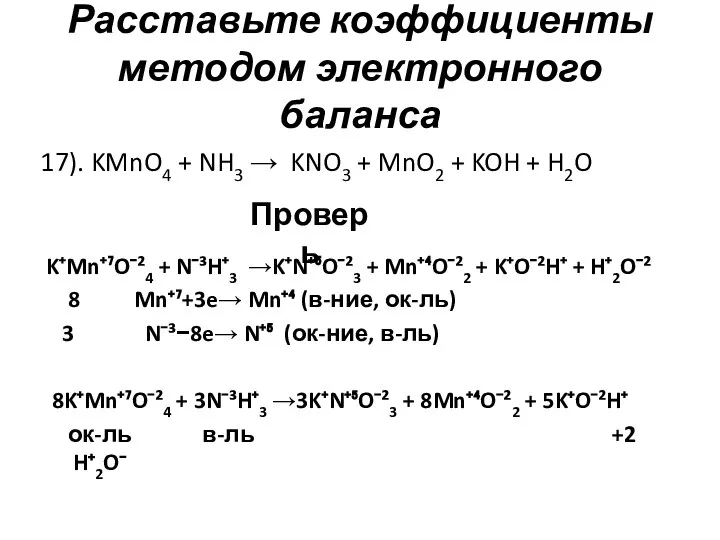
- 19. Расставьте коэффициенты методом электронного баланса K⁺Mn⁺⁷O⁻²4 + N⁻³H⁺3 →K⁺N⁺⁵O⁻²3 + Mn⁺⁴O⁻²2 + K⁺O⁻²H⁺ + H⁺2O⁻² 8
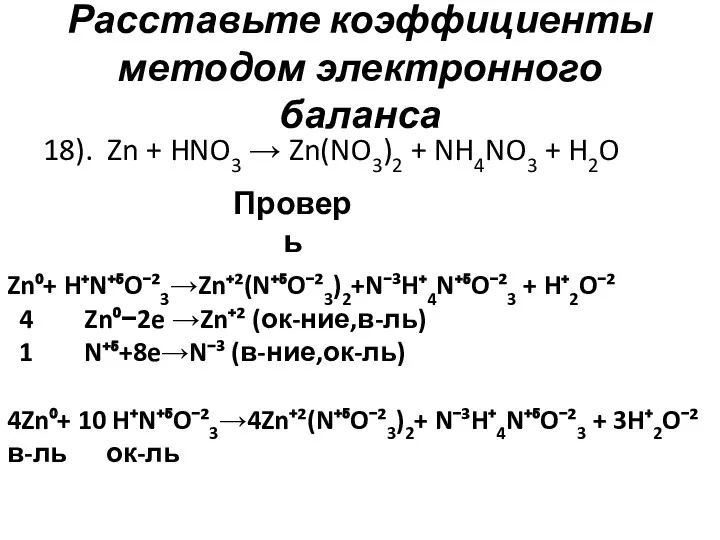
- 20. Расставьте коэффициенты методом электронного баланса 18). Zn + HNO3 → Zn(NO3)2 + NH4NO3 + H2O Проверь
- 22. Скачать презентацию





 Моя мама лучшая на свете
Моя мама лучшая на свете Научная теория и методы научного познания. Философия науки. (Лекция 5)
Научная теория и методы научного познания. Философия науки. (Лекция 5) Основы электроники
Основы электроники Ассортимент для барменов
Ассортимент для барменов Инвестиционный меморандум АНГРЕНСОР ЭНЕРГО
Инвестиционный меморандум АНГРЕНСОР ЭНЕРГО Роль биологии в системе медицинского образования. Клеточный уровень организации живого
Роль биологии в системе медицинского образования. Клеточный уровень организации живого Урок по теме Кислоты
Урок по теме Кислоты Упрощение выражений
Упрощение выражений Площадь поверхности пирамиды
Площадь поверхности пирамиды Редакция 3.0: новые возможности 1С:Бухгалтерии 8
Редакция 3.0: новые возможности 1С:Бухгалтерии 8 C наступающим праздником Новый Год
C наступающим праздником Новый Год Визитная карточка
Визитная карточка Игры и задания на развитие интеллекта. 4 – 7 лет
Игры и задания на развитие интеллекта. 4 – 7 лет Подходы к управлению. Эволюция управления как науки
Подходы к управлению. Эволюция управления как науки Наплавляемая кровля
Наплавляемая кровля Религии мира. Христианство
Религии мира. Христианство Компьютеризованная вышивальная машина Brother. Руководство к действию.
Компьютеризованная вышивальная машина Brother. Руководство к действию. Об'єкти, масиви, формат JSON в JavaScript
Об'єкти, масиви, формат JSON в JavaScript 195 лет со дня рождения Александра Островского. Смех, слёзы и истина
195 лет со дня рождения Александра Островского. Смех, слёзы и истина Нижний Новгород в вопросах и ответах
Нижний Новгород в вопросах и ответах Природные ресурсы
Природные ресурсы Фашизм в Германии
Фашизм в Германии Прочитанная книга о войне - твой подарок ко Дню Победы
Прочитанная книга о войне - твой подарок ко Дню Победы Синтетические волокна. Их свойства. Классификация. Применение. Синтетический каучук
Синтетические волокна. Их свойства. Классификация. Применение. Синтетический каучук Софизмы в алгебре
Софизмы в алгебре Расслоение аневризмы аорты. Хирургическое лечение
Расслоение аневризмы аорты. Хирургическое лечение Ефекти радіаційного ураження
Ефекти радіаційного ураження ЭРДУ аппарата Smart 1
ЭРДУ аппарата Smart 1