Применение национальных стандартов РФ в КДЛ. Контроль качества клинических лабораторных исследований презентация
Содержание
- 2. Национальные стандарты Национальный (государственный) стандарт — стандарт, принятый органом по стандартизации государства – члена Евразийского экономического
- 3. Органы по стандартизации
- 4. Национальные стандарты в России России национальные стандарты имеют добровольное применение, за исключением применения стандартов для оборонной
- 5. Документы по стандартизации в России 1. Документы национальной системы стандартизации: национальные стандарты Российской Федерации: основополагающий национальный
- 6. Документы по стандартизации в России Разработчиком документов национальной системы стандартизации, за исключением национальных основополагающих стандартов и
- 7. Стандартизация в России (история) Республиканские стандарты на продукцию (РСТ РСФСР) утверждались Госпланом РСФСР по номенклатуре продукции.
- 8. Стандартизация в России (история) В 1990 году было установлено, что государственные стандарты СССР и республиканские стандарты
- 9. Стандартизация в РФ Цели и принципы стандартизации в РФ установлены Федеральным законом от 27.12.2002 г №
- 10. Национальные стандарты Федеральный закон № 184-ФЗ от 27.12.2002 «О техническом регулировании» Определил подход к вопросам установления
- 11. Стандарты, определяющие общие требования к деятельности КДЛ ГОСТ Р ИСО 15195-2012 Лаборатории медицинские. Частные требования к
- 12. ГОСТ Р ИСО 15189 - 2012 «Лаборатории медицинские. Частные требования к качеству и компетентности» Принят в
- 13. ГОСТ Р ИСО 15189 - 2012 «Лаборатории медицинские. Частные требования к качеству и компетентности» Отражает подход
- 14. ГОСТ Р ИСО 15189 - 2012 «Лаборатории медицинские. Частные требования к качеству и компетентности» Организация и
- 15. ГОСТ Р ИСО 15189 - 2012 «Лаборатории медицинские. Частные требования к качеству и компетентности» Технические требования:
- 16. ГОСТ Р 53079 - 2008 «Технологии лабораторные медицинские. Обеспечение качества клинических лабораторных исследований» Часть 1. Описание
- 17. ГОСТ Р 53022 - 2008 «Технологии лабораторные медицинские. Требования к качеству клинических лабораторных исследований» Часть 1.
- 18. ГОСТ Р 53133 - 2008 «Технологии лабораторные медицинские. Контроль качества клинических лабораторных исследований» Часть 1. Пределы
- 19. Стандарты по месту лечения ГОСТ Р ИСО 15197-2009 Системы диагностические in vitro. Требования к системам мониторного
- 20. Стандарты, определяющие требования к референтной системе ГОСТ Р ИСО 17511-2006 Изделия медицинские для диагностики in vitro.
- 21. Стандарты, определяющие требования по аналитическим технологиям ГОСТ Р -2009 Технологии комплексных медицинских услуг. Технология клинического лабораторного
- 22. Основная нормативная база Актуальные версии ГОСТов на сайте: www.protect.gost.ru
- 23. РУКОВОДСТВО ПО КАЧЕСТВУ
- 24. Нормативные документы Приказ МЗ РФ № 45 от 07.02.2000 г. «О системе мер по повышению качества
- 25. Нормативные документы ГОСТ Р ИСО 15189-2007 «Лаборатории медицинские. Частные требования к качеству и компетентности» 4.2.3 Политика,
- 26. Типовая модель «Руководства по качеству» 2.1 Общая часть Документы, входящие в общую часть "Руководства по качеству",
- 27. Типовая модель «Руководства по качеству» 2.2. Система обеспечения качества деятельности КДЛ Система обеспечения качества КДЛ строится
- 28. Типовая модель «Руководства по качеству» 2.3 Учетно - отчетная документация. Унифицированные формы учетно - отчетной документации
- 29. Типовая модель «Руководства по качеству» 2.4 Перечень основных ведомственных нормативных документов, используемых при разработке "Руководства по
- 30. СМК «Руководство по качеству» (ГОСТ Р ИСО 15189-2012) Руководство по качеству направлено на успешную реализацию политики
- 31. СМК «Руководство по качеству» (ГОСТ Р ИСО 15189-2012) Введение 1.1. Общие положения (общая информация об организации,
- 32. СМК «Руководство по качеству» (ГОСТ Р ИСО 15189-2012) Введение 1.3 Действующая политика в области качества (Основной
- 33. СМК «Руководство по качеству» (ГОСТ Р ИСО 15189-2012) 1. Введение 2. Нормативные ссылки 3. Термины, определения
- 34. СМК «Руководство по качеству» (ГОСТ Р ИСО 15189-2012) 4. Требования к управлению 4.1.5 Конфиденциальная информация Вся
- 35. СМК «Руководство по качеству» (ГОСТ Р ИСО 15189-2012) 4.2. Система менеджмента качества 4.2.2 Система менеджмента качества
- 36. СМК «Руководство по качеству» (ГОСТ Р ИСО 15189-2012) 4.2. Система менеджмента качества 4.2.3. Политика и цели
- 37. СМК «Руководство по качеству» (ГОСТ Р ИСО 15189-2012) 4.3. Управление документацией для методических нужд описания СМК
- 38. СМК «Руководство по качеству» (ГОСТ Р ИСО 15189-2012) 4.3. Управление документацией Основным видом документов СМК лабораторного
- 39. Проблемы разработки и внедрения СМК медицинских лабораторий на базе ГОСТ Р ИСО 15189-2012 Недостаточность опыта в
- 40. Проблемы лабораторной медицины в РФ Низкая квалификация клиницистов в сфере лабораторной медицины Низкая квалификация среднего медперсонала
- 41. Предотвращение ошибок в ЛМ Специалист ЛМ отвечает за лабораторную часть исследования, но должен контролировать и внелабораторную
- 42. СТАНДАРТНЫЕ ОПЕРАЦИОННЫЕ ПРОЦЕДУРЫ
- 43. Нормативные документы ГОСТ Р 53079.2 - 2008 «Технологии лабораторные клинические. Обеспечение качества клинических лабораторных исследований. Часть
- 44. Нормативные документы ГОСТ Р 53079.2 - 2008 «Технологии лабораторные клинические. Обеспечение качества клинических лабораторных исследований. Часть
- 45. Нормативные документы ГОСТ Р 53079.2 - 2008 «Технологии лабораторные клинические. Обеспечение качества клинических лабораторных исследований. Часть
- 46. Нормативные документы ГОСТ 33044 - 2014 «Межгосударственный стандарт. Принципы надлежащей лабораторной практики» (дата введения 01.08.2015 г)
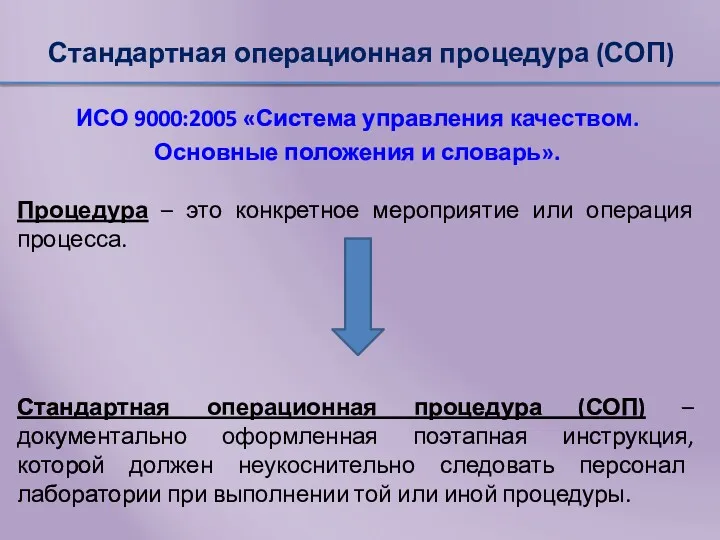
- 47. Стандартная операционная процедура (СОП) ИСО 9000:2005 «Система управления качеством. Основные положения и словарь». Процедура – это
- 48. Стандартная операционная процедура (СОП) Должна быть ясной и отражать детали Должна быть составлена наиболее квалифицированными сотрудниками
- 49. Рекомендуемый перечень СОП-ов 1. Для преаналитического этапа (за пределами лаборатории) 1.1 Заполнение бланка-запроса на исследование. 1.2
- 50. Рекомендуемый перечень СОП-ов 2. Для преаналитического этапа (внутри лаборатории) 2.1 Прием, регистрация и контроль качества биоматериала
- 51. Рекомендуемый перечень СОП-ов 3. Для аналитического этапа 3.1 СОПы по всем «ручным методам» и методам, где
- 52. Рекомендуемый перечень СОП-ов 3. Для аналитического этапа 3.8 Правила работы с информационными системами лаборатории 3.9 Организация
- 53. Рекомендуемый перечень СОП-ов 4. Для постаналитического этапа 4.1 Правила оформления, верификации и утверждения данных протокола исследований
- 54. Рекомендуемый перечень СОП-ов 5. Дополнительные СОПы: 5.1 Правила хранения реагентов 5.2 Правила хранения биоматериала 5.3 Техническое
- 55. Общая схема создания СОП-ов 2.1. Приказ о создании СОПа в устном или письменном виде отдает исполнителю
- 56. Титульная страница СОП 1. Название СОПа 2. Идентификатор (код) СОПа 3. ФИО и должность разработчика СОПа
- 57. Разделы СОП 1. Назначение и область применения В данном разделе необходимо указать в общем виде цель
- 58. Разделы СОП 5. Применяемое оборудования/инструменты Указать, какое оборудование/инструменты необходимо для выполнения СОПа. Помимо простого перечисления рекомендуется
- 59. Разделы СОП 9. Квалификация исполнителей Указать требования к квалификации персонала, допущенного к работе с СОПом 10.
- 60. Ведение реестра внутренних документов Необходимо вести реестр СОПов. В идеале, в лаборатории должна быть установлена система
- 61. Актуализация СОП Проводится не реже, чем один раз в год Проводится разработчиком СОП или ответственным сотрудником
- 62. Стандартизация в РФ Цели и принципы стандартизации в РФ установлены Федеральным законом от 27.12.2002 г №
- 64. Скачать презентацию



























































 Знаменитые люди Великобритании
Знаменитые люди Великобритании Возникновение ислама. Арабский халифат и его распад
Возникновение ислама. Арабский халифат и его распад Падение редуцированных и последствия этого процесса в истории языка
Падение редуцированных и последствия этого процесса в истории языка Презентация к исследовательской работе Жевательная резинка - друг или враг
Презентация к исследовательской работе Жевательная резинка - друг или враг Роль школьной библиотеки в формированииустойчивого познавательного интереса школьников.
Роль школьной библиотеки в формированииустойчивого познавательного интереса школьников. Тамақ және жеңіл өнеркәсіптерінің салалары
Тамақ және жеңіл өнеркәсіптерінің салалары Краткосрочный проект для детей пятого года жизни
Краткосрочный проект для детей пятого года жизни Хто хоче стати міліонером на тему: Перша світова війна
Хто хоче стати міліонером на тему: Перша світова війна Баскетбол
Баскетбол Открытка к 9 Мая. Мастер и мастерица
Открытка к 9 Мая. Мастер и мастерица Сложные эфиры
Сложные эфиры Алкадиены.
Алкадиены. Болезнь Альцгеймера
Болезнь Альцгеймера Развивающая предметно-пространственная среда по физическому развитию детей дошкольного возраста
Развивающая предметно-пространственная среда по физическому развитию детей дошкольного возраста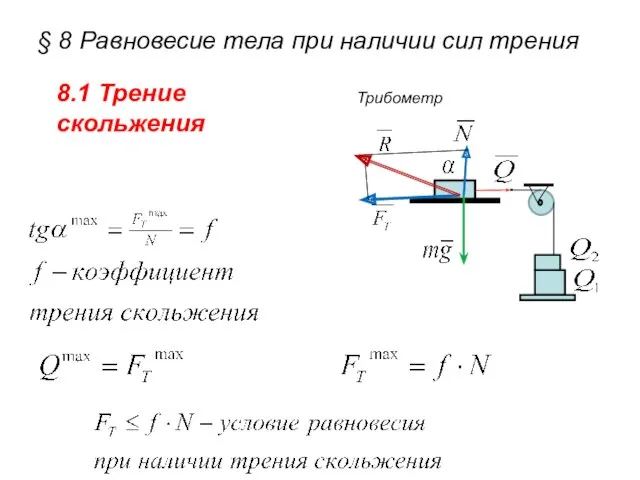 §8. Равновесие тела при наличии сил трения
§8. Равновесие тела при наличии сил трения Энергия ветра
Энергия ветра Бог нас любит
Бог нас любит Свободные экономические зоны и их роль в мировой экономике
Свободные экономические зоны и их роль в мировой экономике Презентация по обучению детей грамоте
Презентация по обучению детей грамоте как определить падеж сущ-х
как определить падеж сущ-х Психология развития: концепция Э. Эриксона психостадиального развития личности
Психология развития: концепция Э. Эриксона психостадиального развития личности Алтайская ГЭС. Фундамент устойчивого развития Республики Алтай
Алтайская ГЭС. Фундамент устойчивого развития Республики Алтай Презентация к уроку по теме Страны Европы
Презентация к уроку по теме Страны Европы Особо охраняемые природные территории. Тамбовская область
Особо охраняемые природные территории. Тамбовская область Раздел Портфолио 2
Раздел Портфолио 2 Религия, её виды, функции, структура
Религия, её виды, функции, структура Работа по проекту Классическая музыка в детском саду С ДМШ имени Йозефа Гайдна.
Работа по проекту Классическая музыка в детском саду С ДМШ имени Йозефа Гайдна. Проект в средней группе на тему: День рожденье куклы Даши
Проект в средней группе на тему: День рожденье куклы Даши