Слайд 2
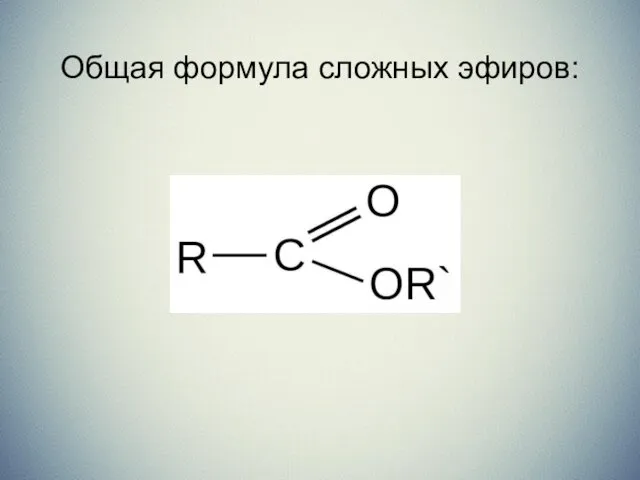
Общая формула сложных эфиров:
Слайд 3

Физические свойства.
Сложные эфиры - бесцветные жидкости, малорастворимые или совсем не растворимые
в воде, обладают специфическим запахом. Сложные эфиры высших спиртов и высших кислот - твердые вещества.
Слайд 4

Химические свойства.
Наиболее характерная реакция для сложных эфиров – гидролиз.При гидролизе сложного
эфира в присутствии кислот образуется карбоновая кислота и спирт:
Слайд 5

Применение сложных эфиров.
Этилформиат НСООС2Н5 и этилацетат Н3СООС2Н5 используются как растворители целлюлозных лаков
используются в пищевой промышленности при создании фруктовых эссенций, а сложные эфиры на основе ароматических спиртов – в парфюмерной промышленности.
Жиры вместе с углеводами и белками составляют набор необходимых для питания пищевых продуктов, они входят в состав всех растительных и животных клеток, кроме того, накапливаясь в организме, играют роль энергетического запаса. Из-за низкой теплопроводности жировой слой хорошо предохраняет животных от переохлаждения.
Животные и растительные жиры представляют собой сырье для получения высших карбоновых кислот, моющих средств и глицерина, используемого в косметической промышленности.
Нитроглицерин – известный лекарственный препарат и взрывчатое вещество, основа динамита.
На основе растительных масел изготавливают олифы ,составляющие основу масляных красок.
Эфиры серной кислоты используют в органическом синтезе как алкилирующие реагенты, а эфиры фосфорной кислоты– как инсектициды.
Слайд 6
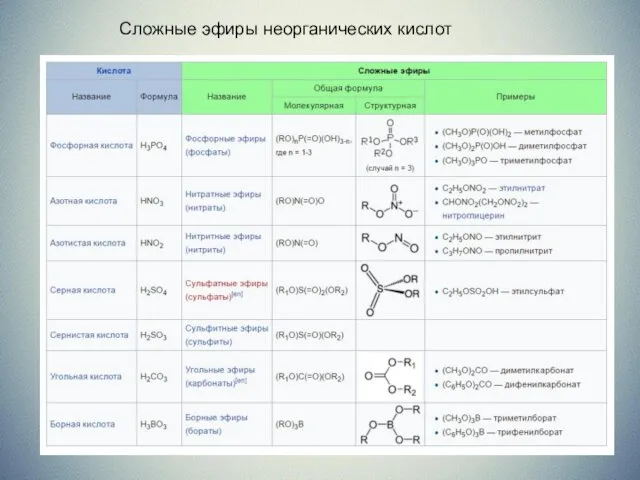
Сложные эфиры неорганических кислот
Слайд 7
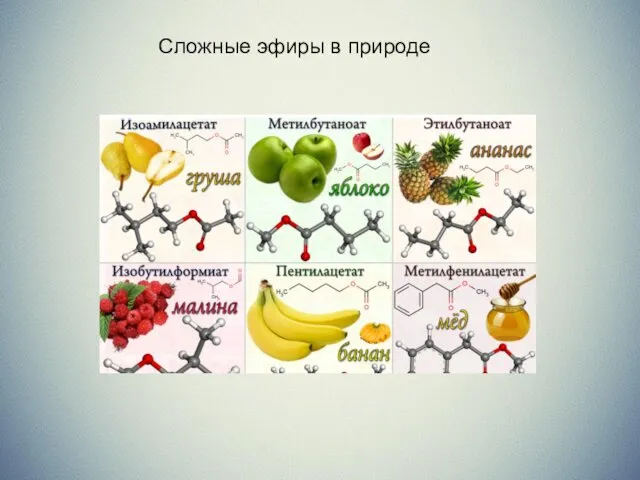
Слайд 8

Номенклатура сложных эфиров.
Название создается следующим образом: вначале указывается группа R,
присоединенная к кислоте, затем – название кислоты с суффиксом «ат» (как и в названиях неорганических солей: карбонат натрия, нитрат хрома).







 Презентация ФГОС Основное общее образование
Презентация ФГОС Основное общее образование Народные промыслы России
Народные промыслы России Художественная культура первой половины XIX века
Художественная культура первой половины XIX века футбольные фанаты
футбольные фанаты Петербургские повести Н. В. Гоголя. Образ маленького человека
Петербургские повести Н. В. Гоголя. Образ маленького человека Пакетные предложения с мобильной связью Конвергент
Пакетные предложения с мобильной связью Конвергент Классный час Делу - время, потехе - час для 3 класса.
Классный час Делу - время, потехе - час для 3 класса. Основные положения и понятия, принятые в строительстве
Основные положения и понятия, принятые в строительстве Интеллектуальная игра Что? Где? Когда?
Интеллектуальная игра Что? Где? Когда? Мое хобби - конструктор Лего
Мое хобби - конструктор Лего Работа с пластилином. Подснежники. Диск
Работа с пластилином. Подснежники. Диск Glad to meet you!
Glad to meet you! Правила дорожного движения
Правила дорожного движения Нейролингвистика. Экспериментальная и клиническая лингвистика
Нейролингвистика. Экспериментальная и клиническая лингвистика Никто не забыт, ничто не забыто...
Никто не забыт, ничто не забыто... Транзисторы и тиристоры
Транзисторы и тиристоры Електроємність. Конденсатори. (Лекция 6)
Електроємність. Конденсатори. (Лекция 6) Как я провёл лето
Как я провёл лето 195 лет со дня рождения Александра Островского. Смех, слёзы и истина
195 лет со дня рождения Александра Островского. Смех, слёзы и истина Выдающийся русский генетик-эволюционист Четвериков Сергей Сергеевич (1880 - 1959)
Выдающийся русский генетик-эволюционист Четвериков Сергей Сергеевич (1880 - 1959) Демоверсия PP2003 - презентация Дня качества Promenade EXPO-A
Демоверсия PP2003 - презентация Дня качества Promenade EXPO-A Токарные резцы
Токарные резцы Туляремия. Этиология
Туляремия. Этиология Антропометрическое соответствие одежды
Антропометрическое соответствие одежды А.С. Пушкин. Борис Годунов
А.С. Пушкин. Борис Годунов Папка классного руководителя
Папка классного руководителя День Матери
День Матери Ühiskonnaõpetus. Ühiskonna mõiste
Ühiskonnaõpetus. Ühiskonna mõiste