Содержание
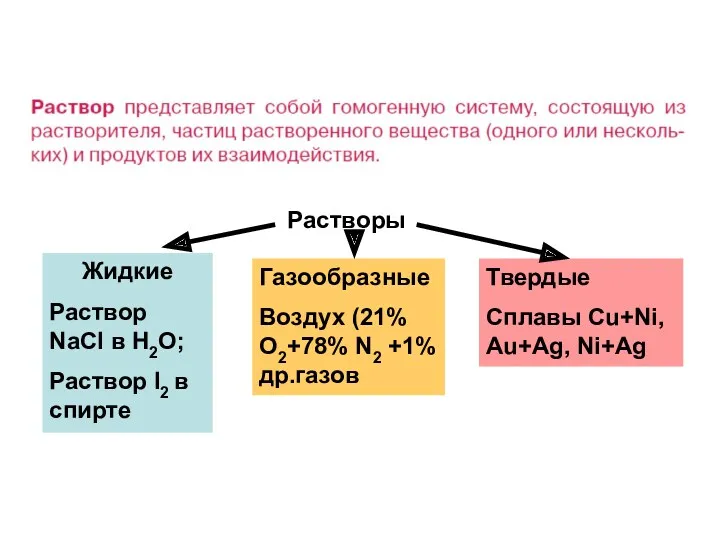
- 2. Растворы Жидкие Раствор NaCl в H2O; Раствор I2 в спирте Газообразные Воздух (21% О2+78% N2 +1%
- 3. Растворение веществ это сложный физико-химический процесс. Разрушение структуры растворяемого вещества и распределение его частиц между молекулами
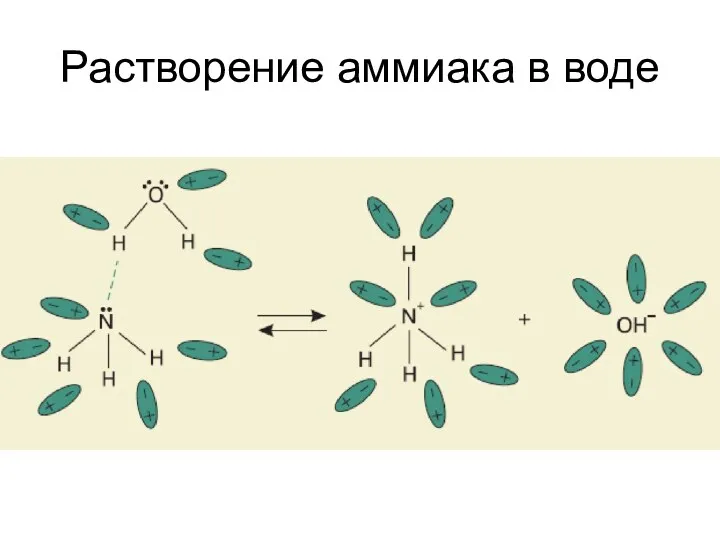
- 4. Растворение аммиака в воде
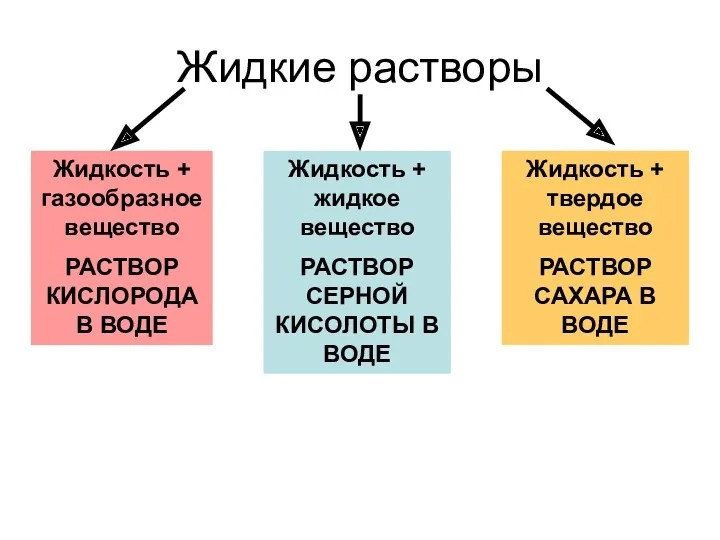
- 5. Жидкие растворы Жидкость + газообразное вещество РАСТВОР КИСЛОРОДА В ВОДЕ Жидкость + жидкое вещество РАСТВОР СЕРНОЙ
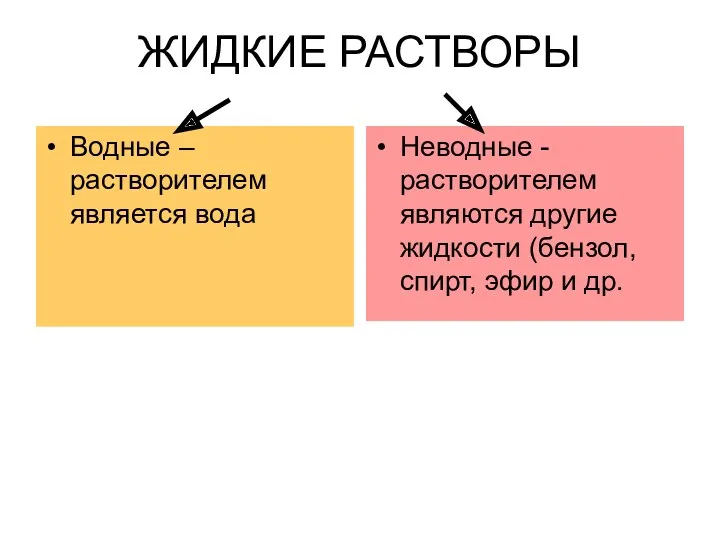
- 6. ЖИДКИЕ РАСТВОРЫ Водные – растворителем является вода Неводные - растворителем являются другие жидкости (бензол, спирт, эфир
- 7. Растворимость веществ Насыщенные растворы – это раствор который содержит максимальное количество растворяемого вещества при данной температуре
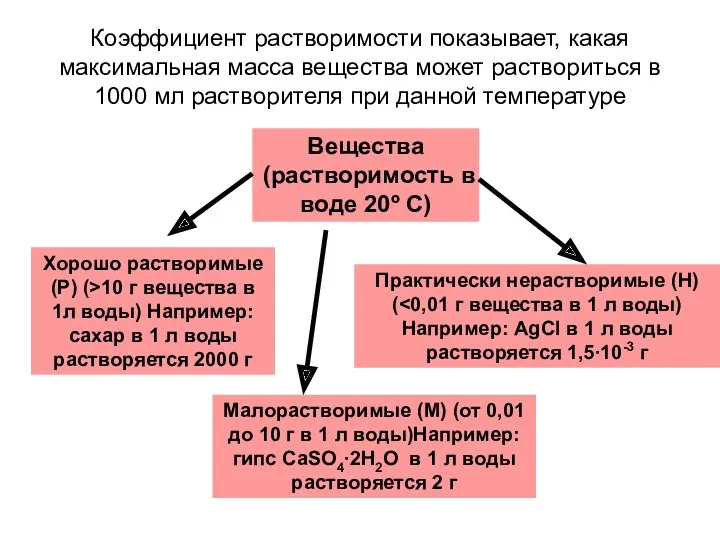
- 8. Коэффициент растворимости показывает, какая максимальная масса вещества может раствориться в 1000 мл растворителя при данной температуре
- 9. Растворимость вещества зависит от: Природы растворенного вещества Температуры Давления (для газов) Растворимость газов при повышении температуры
- 10. Зависимость растворимости твердых веществ от температуры показывают кривые растворимости. Растворимость многих твердых веществ увеличивается при повышении
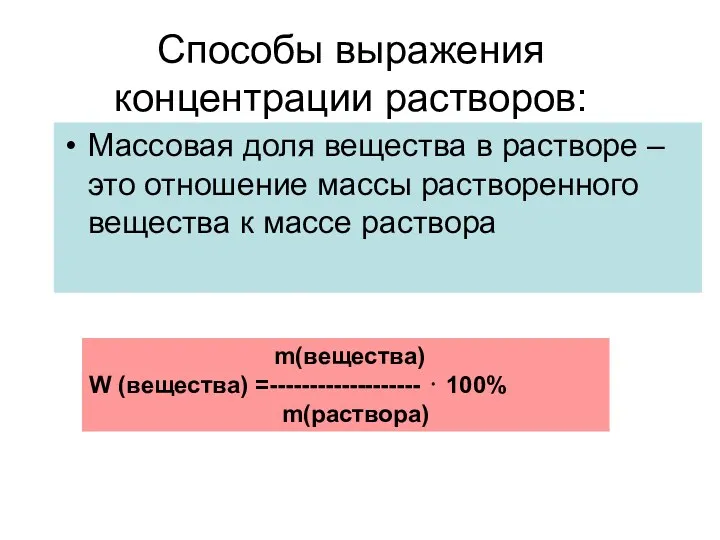
- 11. Способы выражения концентрации растворов: Массовая доля вещества в растворе – это отношение массы растворенного вещества к
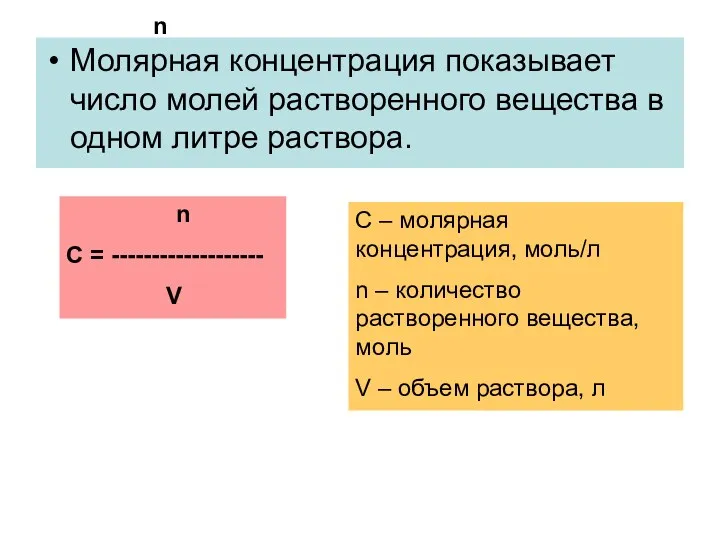
- 12. n С = ------------------- V Молярная концентрация показывает число молей растворенного вещества в одном литре раствора.
- 14. Скачать презентацию




 Кинезиологические упражнения как средство помощи детям с проблемами в развитии
Кинезиологические упражнения как средство помощи детям с проблемами в развитии Арифметика здоровья. Внеклассное занятие по математике для учащихся 5 класса
Арифметика здоровья. Внеклассное занятие по математике для учащихся 5 класса Великая Отечественная война 1941-1945
Великая Отечественная война 1941-1945 Инструменты и приспособления, применяемые при выполнении ручных работ
Инструменты и приспособления, применяемые при выполнении ручных работ Курс Эконометрика
Курс Эконометрика Шкаф знаний, или 33 совета по практике английского языка
Шкаф знаний, или 33 совета по практике английского языка ФГОС дошкольного образования
ФГОС дошкольного образования Эмфизема легких, дыхательная недостаточность, ХЛС
Эмфизема легких, дыхательная недостаточность, ХЛС Организация исследовательской деятельности в ДОУ
Организация исследовательской деятельности в ДОУ Организация работы с детьми по ФЭМП.
Организация работы с детьми по ФЭМП. Консультация для родителей. Волшебные точки здоровья. Самомассаж по методике А.А. Уманской
Консультация для родителей. Волшебные точки здоровья. Самомассаж по методике А.А. Уманской Технико-экономический инструментарий процессов управления в транспортной логистике
Технико-экономический инструментарий процессов управления в транспортной логистике КАЭС – первая атомная электростанция России
КАЭС – первая атомная электростанция России Сценарий Мама, папа, я - спортивная семья
Сценарий Мама, папа, я - спортивная семья Проектирование механосборочного производства
Проектирование механосборочного производства Вышивание крестиком Диск
Вышивание крестиком Диск Обмен веществ в клетке
Обмен веществ в клетке Фокус-группа. Методики, используемые в качественных исследованиях товаров
Фокус-группа. Методики, используемые в качественных исследованиях товаров Максимилиан Александрович Волошин (1877-1932) – русский поэт серебряного века, художник, критик
Максимилиан Александрович Волошин (1877-1932) – русский поэт серебряного века, художник, критик презентация к уроку алюминий, 9 класс
презентация к уроку алюминий, 9 класс Учет нематериальных активов
Учет нематериальных активов 20231002_sovety_po_podgotovke_k_ege
20231002_sovety_po_podgotovke_k_ege Дорожная математика
Дорожная математика Организм человека
Организм человека Who am I?
Who am I? Презентация к занятию Путешествие в страну Фантазии
Презентация к занятию Путешествие в страну Фантазии Топливная промышленность России
Топливная промышленность России Правление Ивана IV Грозного (внутренняя политика)
Правление Ивана IV Грозного (внутренняя политика)