Слайд 2

Щелочные металлы — это элементы 1-й группы периодической таблицы химических веществ: литий Li, натрий Na, калий K, рубидий Rb, цезий Cs, франций Fr.
При растворении щелочных металлов в воде образуются растворимые гидроксиды, называемые щелочами.
Слайд 3

Все металлы этой подгруппы имеют серебристо-белый цвет (кроме серебристо-жёлтого цезия), они очень мягкие,
их можно резать скальпелем.
Слайд 4
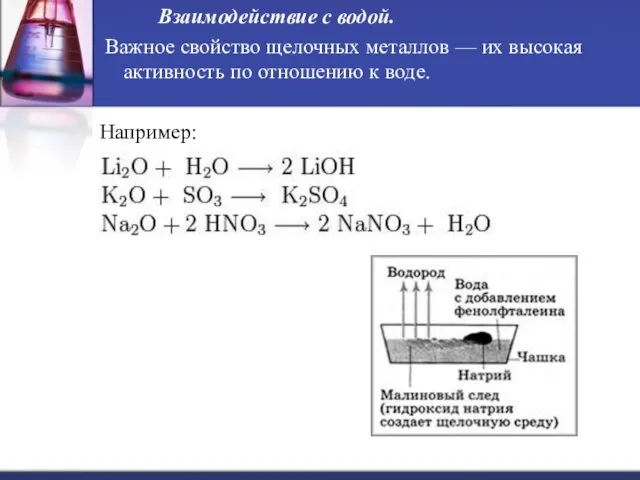
Взаимодействие с водой.
Важное свойство щелочных металлов — их высокая активность по отношению
к воде.
Например:
Слайд 5

Взаимодействие с кислородом.
Продукты горения щелочных металлов на воздухе имеют разный состав в зависимости
от активности металла.
Все кислородные соединения имеют различную окраску, интенсивность которой увеличивается в ряду от Li до Cs:
Слайд 6

Взаимодействие с другими веществами.
Щелочные металлы реагируют со многими неметаллами. При нагревании они
соединяются с водородом с образованием гидридов, с галогенами , с серой сульфидов, азотом - нитридов, фосфором - фосфитов, углеродом - карбидов и кремнием - силицидов:





 Сочинение по данному началу. Моё утро
Сочинение по данному началу. Моё утро Коммуникативная , социальная, эмоционально-волевая готовность детей к школьному обучению
Коммуникативная , социальная, эмоционально-волевая готовность детей к школьному обучению Угловые соединения
Угловые соединения План-конспект внеклассного мероприятия в 1 классе по теме: Осенины.
План-конспект внеклассного мероприятия в 1 классе по теме: Осенины. Культура освоения новой технологии. Руководитель ШППО Бейбулатова Е.А.
Культура освоения новой технологии. Руководитель ШППО Бейбулатова Е.А. Великая Отечественная Война
Великая Отечественная Война Формы взаимодействия психолога с коллективом
Формы взаимодействия психолога с коллективом Церковь Иль - Джезу
Церковь Иль - Джезу Миф о Йиркапе
Миф о Йиркапе Прохождение практики ООО Виал Комфорт
Прохождение практики ООО Виал Комфорт Понятия и уравнения кинематики
Понятия и уравнения кинематики Теории происхождения нефти и газа – основа прогнозирования перспектив нефтеносности недр
Теории происхождения нефти и газа – основа прогнозирования перспектив нефтеносности недр Поделки из помпонов
Поделки из помпонов Автоматизация звука [Р] в середине слова (интервокальная позиция)
Автоматизация звука [Р] в середине слова (интервокальная позиция) Я и мой школьный спортивный клуб. Ясырева Елена
Я и мой школьный спортивный клуб. Ясырева Елена Формирование личностной идентичности человека
Формирование личностной идентичности человека Презентация Дерево моей семьи
Презентация Дерево моей семьи General equilibrium in the open (trading) economy
General equilibrium in the open (trading) economy Петр Алексеевич (Первый) Романов
Петр Алексеевич (Первый) Романов Развитие критического мышления у учащихся
Развитие критического мышления у учащихся Кілегей қабықтын жарақаттаушы әсерлерден зақымдануы. Лейкоплакия
Кілегей қабықтын жарақаттаушы әсерлерден зақымдануы. Лейкоплакия Родительское собрание
Родительское собрание Презентация Les inventions françaises
Презентация Les inventions françaises винокуров презентация
винокуров презентация Сталь. Свойства
Сталь. Свойства С праздником 8 марта
С праздником 8 марта Рождественские узоры Поволжья. Порядок участия в Межрегиональной выставке-ярмарке
Рождественские узоры Поволжья. Порядок участия в Межрегиональной выставке-ярмарке Геохимия урана и тория в осадочном процессе
Геохимия урана и тория в осадочном процессе