Строение вещества. Химическая связь и кристаллическое строение. Ионная и ковалентная связи презентация
Содержание
- 2. Химическая связь — явление взаимодействия атомов. Химическая связь и кристаллическое строение.
- 3. Химическая связь в веществах
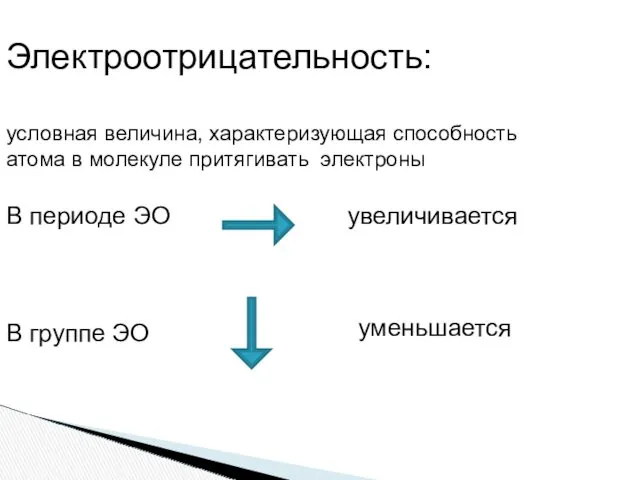
- 4. Электроотрицательность: условная величина, характеризующая способность атома в молекуле притягивать электроны В периоде ЭО увеличивается В группе
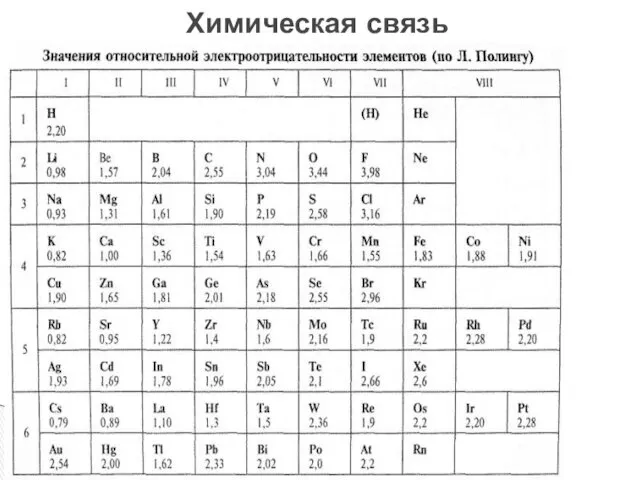
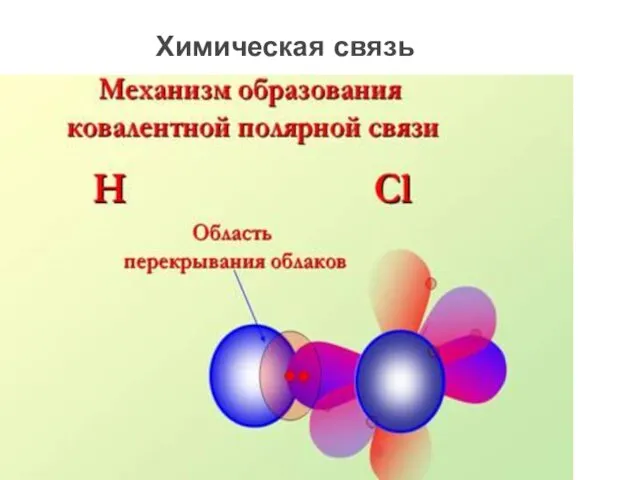
- 5. Химическая связь
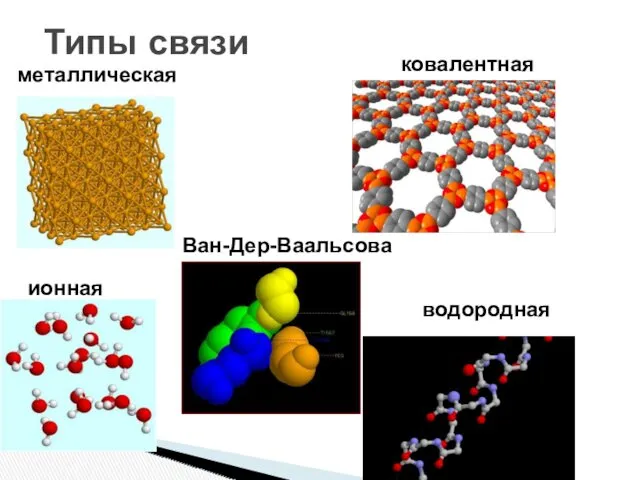
- 6. Типы связи металлическая ковалентная ионная Ван-Дер-Ваальсова водородная
- 7. Определение типа связи по разности ЭО элементов в соединении: ∆ ЭО 0 ковалентная неполярная связь ∆
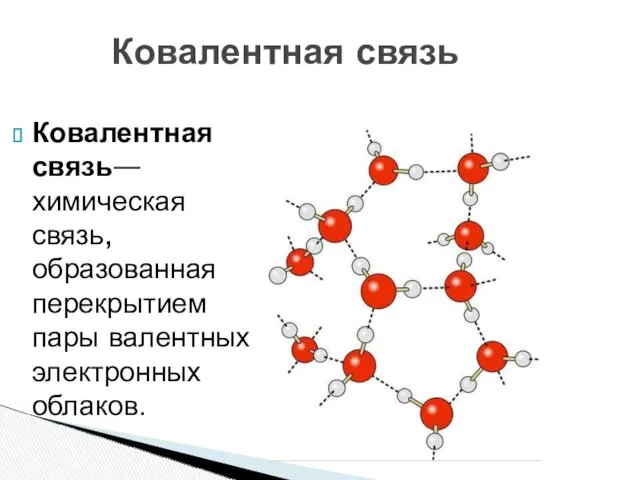
- 8. Ковалентная связь— химическая связь, образованная перекрытием пары валентных электронных облаков. Ковалентная связь
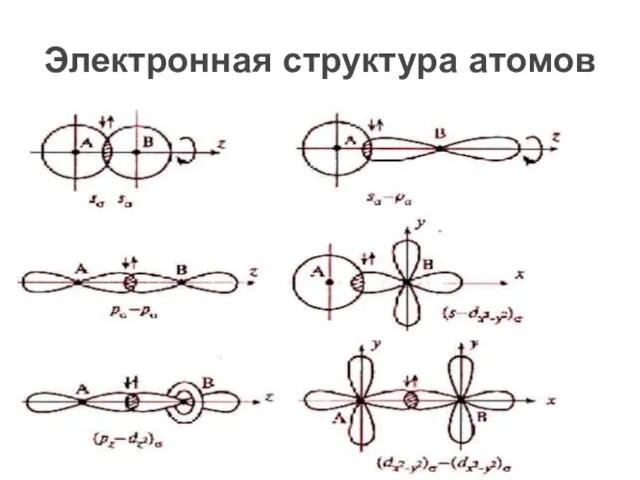
- 9. Электронная структура атомов
- 10. Химическая связь
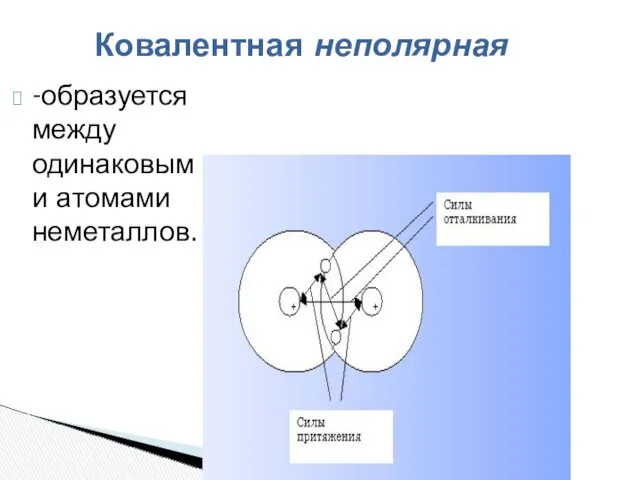
- 11. Ковалентная неполярная -образуется между одинаковыми атомами неметаллов.
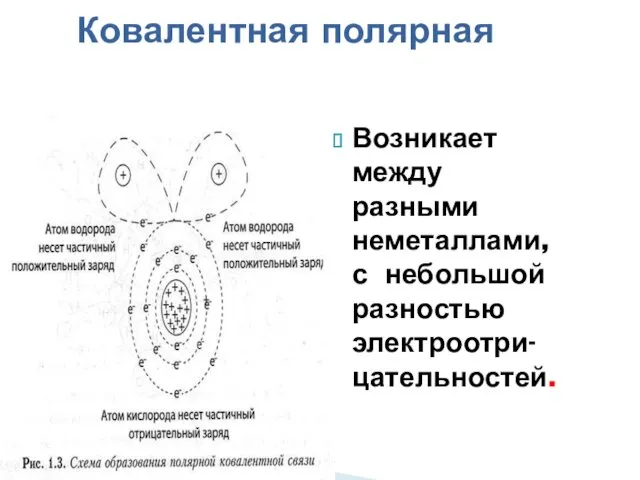
- 12. Ковалентная полярная Возникает между разными неметаллами, с небольшой разностью электроотри-цательностей.
- 13. Химическая связь
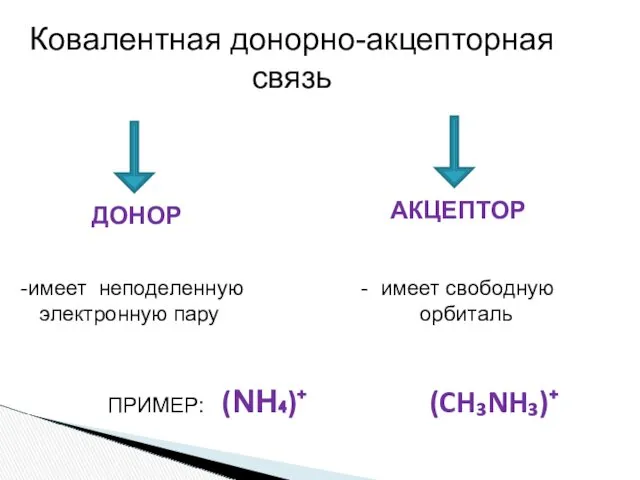
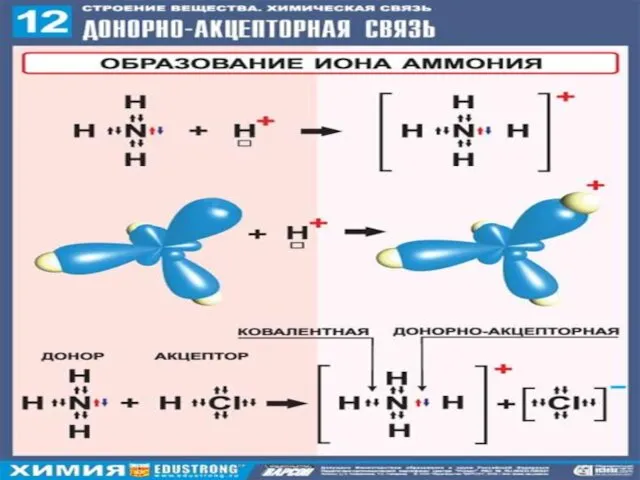
- 14. Ковалентная донорно-акцепторная связь ДОНОР АКЦЕПТОР имеет неподеленную - имеет свободную электронную пару орбиталь ПРИМЕР: (NH₄)⁺ (CH₃NH₃)⁺
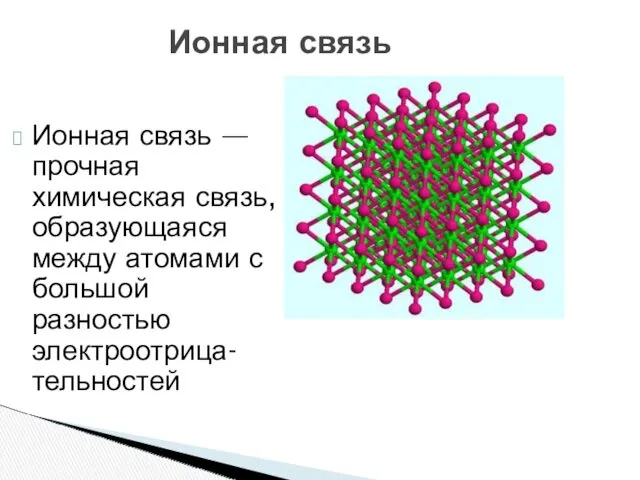
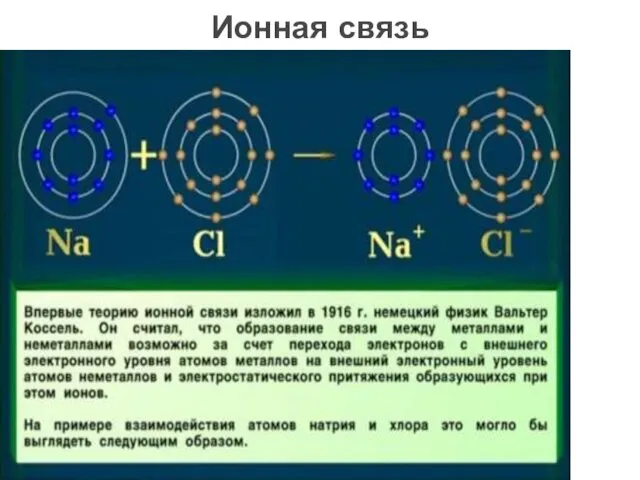
- 16. Ионная связь — прочная химическая связь, образующаяся между атомами с большой разностью электроотрица-тельностей Ионная связь
- 17. Ионная связь
- 18. Сте́пень окисле́ния ( формальный заряд) — условная численная величина электрического заряда, приписываемого атому в молекуле в
- 19. Степень окисления Алгоритм определения степени окисления: Найдите элемент(-ты) с постоянной степенью окисления ( постоянная валентность; таблицы
- 20. Степень окисления 1.Определите степень окисления элементов в соединениях: KCl Na₂O ZnCl₂ HCl Al₂O₃ MgS N₂O₃ Fe₂O₃
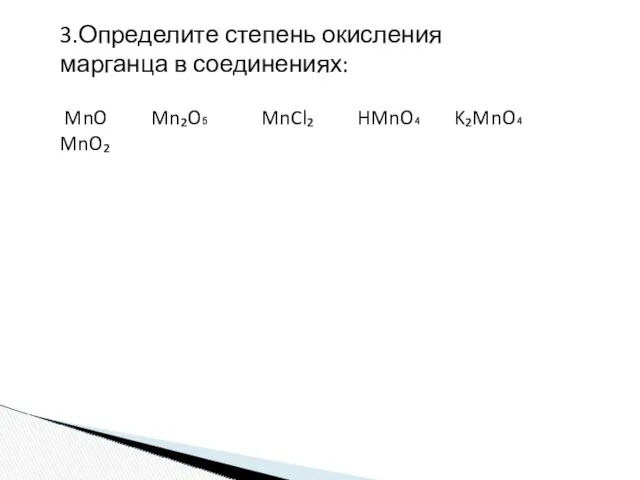
- 21. 3.Определите степень окисления марганца в соединениях: MnO Mn₂O₅ MnCl₂ HMnO₄ K₂MnO₄ MnO₂
- 22. Определите вид химической связи в соединениях: Cl₂ , H₂O , CO , OF₂ , H₂ ,
- 24. Скачать презентацию







 Основные тригонометрические тождества
Основные тригонометрические тождества Оплодотворение. Эмбриогенез
Оплодотворение. Эмбриогенез ПрезентацияУглеводы
ПрезентацияУглеводы Мнемосказки в развитии связной речи у дошкольников
Мнемосказки в развитии связной речи у дошкольников Рельеф России
Рельеф России Теоретическое и прикладное материаловедение. Классификация двойных систем
Теоретическое и прикладное материаловедение. Классификация двойных систем Контроль качества поверхности при различных видах обработки
Контроль качества поверхности при различных видах обработки Сетевые технологии систем связи с коммутацией каналов
Сетевые технологии систем связи с коммутацией каналов Seminar on Sound Card
Seminar on Sound Card Бестраншейные бурения
Бестраншейные бурения Разработка VAD алгоритма для ГЛОНАСС/GPS навигатора
Разработка VAD алгоритма для ГЛОНАСС/GPS навигатора Зимние забавы
Зимние забавы Добыча полезных ископаемых скважинным способом
Добыча полезных ископаемых скважинным способом Пластмассы: получение, применение, утилизация
Пластмассы: получение, применение, утилизация Технологии презентаций
Технологии презентаций Пускать ли в ход кулаки
Пускать ли в ход кулаки Определение геометрической прогрессии. Формула n-го члена геометрической прогрессии. 9 класс
Определение геометрической прогрессии. Формула n-го члена геометрической прогрессии. 9 класс Международный информационно-исследовательский проект. Общая характеристика стран Зарубежной Европы (на примере Франции)
Международный информационно-исследовательский проект. Общая характеристика стран Зарубежной Европы (на примере Франции) Психолого-педагогические основы взаимодействия с родителями воспитанников ДОУ в соответствии с требованиями ФГОС.
Психолого-педагогические основы взаимодействия с родителями воспитанников ДОУ в соответствии с требованиями ФГОС. дебаты на тему: Субкультуры: за и против
дебаты на тему: Субкультуры: за и против Регулирование напряжения в электрической системе группы цехов машиностроительного завода
Регулирование напряжения в электрической системе группы цехов машиностроительного завода Процесс очистки и диагностики промысловых газопроводов
Процесс очистки и диагностики промысловых газопроводов Цеолит - символ чистой воды
Цеолит - символ чистой воды Конвенция о правах ребенка
Конвенция о правах ребенка Религиозное многообразие России
Религиозное многообразие России Особенности русского языка
Особенности русского языка Об изобретателях
Об изобретателях презентация Праздник осени Диск
презентация Праздник осени Диск