Содержание
- 2. План: Введение. Ингибиторы факторов роста. Таргетные препараты, блокирующие рецепторы ангиогенеза. Таргетные препараты – ингибиторы тирозинкиназы. Таргетные
- 3. Введение. Фундаментальным достижением последнего десятилетия является образование нового класса «таргетных, молекулярно‐ориентированных препаратов», создаваемых для воздействия на
- 4. Все эти мишени имеются и в нормальной клетке, но при опухолевой трансформации происходит их гиперэкспрессия или
- 5. То есть цели таргетных препаратов в онкологии это собственные белки организма, участвующие в процессах канцерогенеза и
- 6. Большинство таргетных препаратов не обладает способностью убивать или выраженно повреждать опухолевые клетки (цитотоксическое воздействие), а лишь
- 7. В связи с этим основным эффектом при их использовании является не излечение, а длительное сдерживание опухолевого
- 8. В онкологии целями для воздействия таргетных препаратов являются:
- 9. «малые молекулы» (низкомолекулярные ингибиторы). антитела По своей химической структуре таргетные средства подразделяют на
- 10. антитела Это продукты природного происхождения с очень высокой специфичностью. Они не проникают внутрь клетки, мишенью являются
- 11. антитела В-лимфоциты, полученные от иммунизируемой мыши, иммортализуются посредством слияния с бессмертными клетками – клетками миеломы. «Чистые»
- 12. «малые молекулы» (низкомолекулярные ингибиторы). Это продукт химического синтеза с умеренной специфичностью («мультитаргетные препараты»). Они проникают внутрь
- 14. 1. Ингибиторы рецепторов факторов роста Рецепторы факторов роста представлены большим семейством различных трансмембранных белков, локализованными в
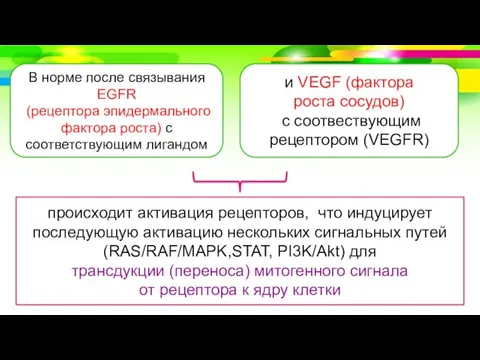
- 15. В норме после связывания EGFR (рецептора эпидермального фактора роста) c соответствующим лигандом и VEGF (фактора роста
- 17. В опухолях часто встречается гиперактивация сигнала от этих рецепторов. Этот феномен является результатом нескольких событий:
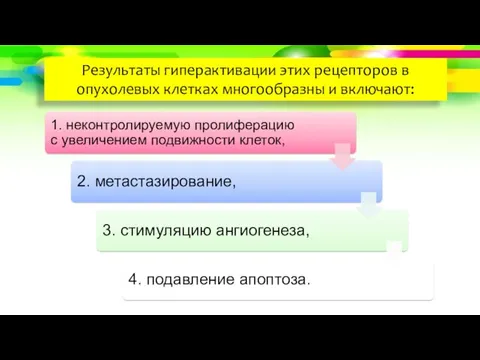
- 18. Результаты гиперактивации этих рецепторов в опухолевых клетках многообразны и включают:
- 20. Исходя из этих данных, в качестве противоопухолевых агентов предложено использовать моноклональные антитела к EGFR и VEGF,
- 21. Моноклональные антитела Механизм действия препаратов: связываясь с экстрацеллюлярным доменом EGFR, они препятствуют его связыванию с природным
- 23. 2. Таргетные препараты, блокирующие рецепторы ангиогенеза Неоангиогенез является важным патогенетическим фактором роста и прогрессирования опухолей, т.
- 24. Важнейшую роль в неоангиогенезе играет пролиферация эндотелиальных клеток, для развития которой наибольшее значение имеет действие фактора
- 25. Бевацизумаб (авастин) Рекомбинантное гуманизированное моноклональное антитело против фактора роста эндотелия сосудов (VEGF). Бевацизумаб реагирует с участком
- 26. 3. Таргетные препараты – ингибиторы тирозинкиназы. Тирозинкиназы — одно из важнейших звеньев в системе передачи сигналов
- 28. Препарат иматиниб (гливек) ингибирует тирозинкиназную активность не только рецепторов некоторых факторов роста, но и химерного белка,
- 29. В результате экспрессии гена BCR/ABL образуется химерный белок р210BCR/ABL, обладающий повышенной тирозинкиназной активностью. Появление этого белка
- 30. В конце 1990-х гг., была обнаружена экспрессия на поверхности клеток стромальных опухолей ЖКТ мутантного онкобелка с-kit,
- 31. 4. Таргетные препараты, блокирующие белки, осуществляющие проведение митогенных сигналов. mTOR – это внутриклеточный белок – серин-треониновая
- 32. Перспективы и разочарования таргетной терапии. Благодаря таргетной терапии улучшены контроль симптомов и качество жизни больных. Заболевания
- 36. Скачать презентацию





























 Оперативная память ЭВМ
Оперативная память ЭВМ Презентации по химии для 9 класса
Презентации по химии для 9 класса Липиды и везикулярный транспорт (лекция 6)
Липиды и везикулярный транспорт (лекция 6) Охрана зеленых памятников
Охрана зеленых памятников Основные показатели качества воды
Основные показатели качества воды Экология в производстве полимербетона
Экология в производстве полимербетона Прочностной мониторинг как составная часть научно-технического сопровождения
Прочностной мониторинг как составная часть научно-технического сопровождения Применение использование компьютера и ИКТ в работе музыкального руководителя
Применение использование компьютера и ИКТ в работе музыкального руководителя Биопластики: область применения
Биопластики: область применения Родительское собрание Как помочь ребёнку быть внимательным
Родительское собрание Как помочь ребёнку быть внимательным Патологическая анатомия, ее содержание и задачи. Патологоанатомическая служба, её роль и место в системе здравоохранения
Патологическая анатомия, ее содержание и задачи. Патологоанатомическая служба, её роль и место в системе здравоохранения Транспортные операции
Транспортные операции Финансовый рынок (рынок ссудного капитала)
Финансовый рынок (рынок ссудного капитала) Использование ИКТ на уроках географии.
Использование ИКТ на уроках географии. Тактика допроса и очной ставки
Тактика допроса и очной ставки Презентация творческой работы по теме: Сенсорное воспитание через развивающие игры
Презентация творческой работы по теме: Сенсорное воспитание через развивающие игры Компьютерная анимация. GIF-анимация в GIMP
Компьютерная анимация. GIF-анимация в GIMP Моніторинг процесу децентралізації влади та реформування місцевого самоврядування
Моніторинг процесу децентралізації влади та реформування місцевого самоврядування Лекция 4. Взаимодействие в деловом общении
Лекция 4. Взаимодействие в деловом общении Управление реактивной мощностью
Управление реактивной мощностью О ні, ніхто нас не розлучить з Христом
О ні, ніхто нас не розлучить з Христом Графовые модели систем защиты информации. Лекция
Графовые модели систем защиты информации. Лекция Наш дружный комитет! Портфолио Родительского комтета
Наш дружный комитет! Портфолио Родительского комтета видеообращение
видеообращение Как вести себя в школе.
Как вести себя в школе. Тест по рассказу В.М. Шукшина Срезал
Тест по рассказу В.М. Шукшина Срезал Метод проектов
Метод проектов Пирамида, её основание, вершина, боковые рёбра, высота, боковая поверхность
Пирамида, её основание, вершина, боковые рёбра, высота, боковая поверхность