Слайд 2

Понятие о химическом уравнении.
Число атомов химических элементов до реакции и после
неё, остаётся неизменным, а значит, их общая масса тоже не изменяется.
На основании Закона сохранения массы веществ составляются уравнения химических реакций.
Слайд 3

Понятие о химическом уравнении.
Химическое уравнение – это условная запись химической реакции
с помощью химических формул и математических знаков.
Слайд 4

Правила составления уравнений химических реакций.
В левой части уравнения пишутся формулы веществ,
вступающих в реакцию (исходные вещества), в правой –формулы получившихся веществ (продукты реакции).
Затем на основании закона сохранения массы веществ начинают уравнивать атомы. Число атомов каждого химического элемента в правой части должно равняться числу атомов этого же элемента в левой части.
Уравнивание атомов производится с помощью подбора коэффициентов – чисел, которые выставляют перед формулами.
Слайд 5

Правила составления уравнений химических реакций.
1. Составим уравнение реакции горения углерода:
1.
С + О2 →
2. С + О2 →CO2
3. 1 атом С + 2 атома О → 1 атом С и 2 атома О
Слайд 6

Правила составления уравнений химических реакций.
2. Реакция разложения оксида ртути.
1. HgO →
2.
HgO → Hg + O2
3. 1 атом Нg и 1 атом О → 1 атом Нg + 2 атома О
4. 2HgO → Hg + O2
5. 2 атома Нg и 2 атома О → 1 атом Нg + 2 атома О
6. 2HgO → 2Hg + O2
Слайд 7

Типы химических реакций.
По изменению числа исходных и конечных продуктов реакции делят
на:
Реакции разложения.
Реакции соединения.
Реакции замещения.
Реакции обмена.
Слайд 8

Реакции разложения -
это реакции, в результате которых из одного вещества
получается несколько новых веществ.
2HgO → 2Hg + O2
2КNO3 →2KNO2 + O2
CaCO3 →CaO + CO2
2KMnO4 →K2MnO4+ MnO2 + O2
Слайд 9

Реакции соединения -
- это реакции, в результате которых из двух или
нескольких простых или сложных веществ образуется одно более сложное.
С + О2 →CO2
2Сu + O2 →2CuO
Na2O + CO2 → Na2CO3
Слайд 10

Реакции замещения -
это реакции между простым и сложным веществом, в
результате которых атомы простого вещества замещают атомы одного из химических элементов в сложном веществе.
Zn +2HCl → ZnCl2 +H2
CuSO4 + Fe →Cu + FeSO4
2Na + 2H2O →2NaOH + H2
Слайд 11

Реакции обмена -
это реакции, между двумя сложными веществами, при протекании
которых их молекулы обмениваются своими составными частями.
CuSO4 + 2NaOH→Сu(OH)2↓+ Na2SO4
2HNO3 + Ba(OH)2→ Ba(NO3)2 + 2SO4
NH4Cl + KOH → KCl + NH3↑+ H2O
Слайд 12

Закрепление.
1. Расставьте коэффициенты в следующих
уравнениях реакций. Определите типы реакций:
СаСО3 → СаО
+ CO2
Na2SO4 + ВаСl2 → NaСl + ВаSO4
SO3 + H2O → H2SO4
Cu +HNO3(конц) →Cu(NO3)2 + NO2↑+ H2O
Fe(OH)3 → Fe2O3 + H2O
Аl2(SO4)3 + NaOH → Na2SO4 + Аl(OH)3↓











 Презентация Формирование творческих компетенций детей в процессе рисования нетрадиционными техниками и материалами
Презентация Формирование творческих компетенций детей в процессе рисования нетрадиционными техниками и материалами Стратегические ориентиры развития образования Кировской области
Стратегические ориентиры развития образования Кировской области Классификация гравитационных методов обогащения
Классификация гравитационных методов обогащения Антарктида. Географическое положение и история исследования
Антарктида. Географическое положение и история исследования Технология конструкционных материалов. Оптимальная точность обработки
Технология конструкционных материалов. Оптимальная точность обработки Театрально-игровая деятельность в развитии младших дошкольников
Театрально-игровая деятельность в развитии младших дошкольников Елизавета Петровна
Елизавета Петровна Життя моєї групи. Фотоальбом
Життя моєї групи. Фотоальбом Методические рекомендации по оформлению научных работ
Методические рекомендации по оформлению научных работ Искусство Фландрии XVII века
Искусство Фландрии XVII века Строительство школы нового поколения в г. Мичуринске
Строительство школы нового поколения в г. Мичуринске Специфика создания материального потока при транспортировке крупногабаритных тяжеловесных грузов
Специфика создания материального потока при транспортировке крупногабаритных тяжеловесных грузов Конспект непосредственно образовательной деятельности по духовно-нравственному воспитанию для детей старшего дошкольного возраста Праздник Покрова Пресвятой Богородицы
Конспект непосредственно образовательной деятельности по духовно-нравственному воспитанию для детей старшего дошкольного возраста Праздник Покрова Пресвятой Богородицы Ганс Гольбейн Младший
Ганс Гольбейн Младший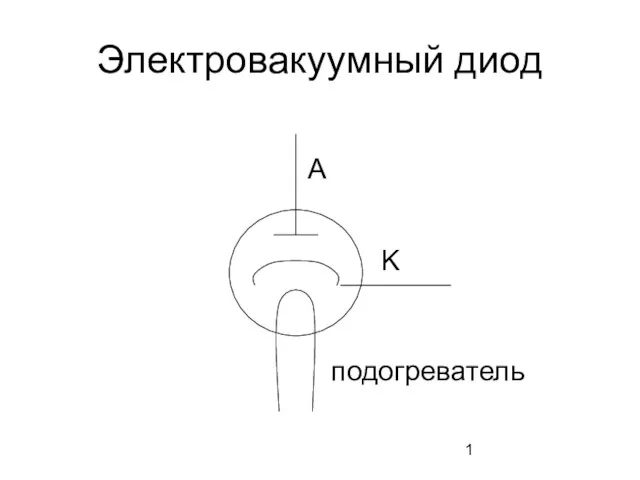 Электровакуумный диод
Электровакуумный диод Эрнест Хемингуэй 1899-1961
Эрнест Хемингуэй 1899-1961 Силикаты. Классификация силикатов
Силикаты. Классификация силикатов Установки для электрошлаковой сварки
Установки для электрошлаковой сварки Презентация
Презентация Круглый стол на тему Наркомания и СПИД: сущность и проблема (методика проведения вебинара)
Круглый стол на тему Наркомания и СПИД: сущность и проблема (методика проведения вебинара) Специальная оценка условий труда
Специальная оценка условий труда HLA жүйесі, құрылысы, қызметтері. Трансплантациялық иммунитет
HLA жүйесі, құрылысы, қызметтері. Трансплантациялық иммунитет В. А. Жуковский. Спящая царевна как литературная сказка
В. А. Жуковский. Спящая царевна как литературная сказка Весна. Время посева и глубина заделки семян
Весна. Время посева и глубина заделки семян Знание
Знание Букет для мамы
Букет для мамы Пой, живи, Россия!
Пой, живи, Россия! Аңыз әңгімелер
Аңыз әңгімелер