Слайд 2

Цели и задачи урока:
❒Развитие познавательного интереса учащихся к предмету химии.
❒Обобщение, повторение и систематизация знаний учащихся за курс 8 класса.
❒Развитие умений учащихся
-сосредоточиться и применить свои знания в коллективном творчестве и в нестандартных игровых формах учебной деятельности;
-четко и полно формулировать свои мысли.
❒ Воспитывать у ребят культуру поведения, общения друг с другом в процессе учебной деятельности.
Слайд 3

План.
Вступительное слово учителя.
Организация класса, знакомство учащихся с условиями игры.
Игра «Вы знаете?
Вы все, конечно, знаете!»
1. Знакомство с командами. Каждая команда представляет себя очень кратко: название, девиз.
2. Игра по заданиям.
3. Игра с болельщиками.
4. Подведение итогов.
Заключительное слово учителя.
Слайд 4

Условия игры.
Учащиеся делятся на 2 команды, в каждой
команде определяются 5групп (2-3чел.), их очередность выполнять задания. На подготовку и выполнение задания дается не более 3 минуты.
За каждый правильный ответ группа получает 5 баллов. Если учащиеся группы не знают ответа, помогают члены команды, но при этом за правильный ответ команда получает только 3 балла.
Можно отдельных уч-ся-знатоков поощрять дополнительными баллами, наградить.
В состав жюри приглашаются 3-5 старшеклассников.
Ход игры.
1. Знакомство с командами.
Каждая команда представляет себя очень кратко:
название, девиз.
2. Игра по заданиям.
3. Игра с болельщиками
4. Подведение итогов
Слайд 5

Дайте определение химическому элементу.
Сколько химических элементов известно в настоящее время?
Кем и
когда был открыт основной закон о химических элементах?
Как называется этот закон,
как формулируется?
Слайд 6

Вспомните,
что такое
химическая реакция?
Дайте определение. Назовите
типы химических реакций
(по количеству и качественному составу исходных веществ и продуктов реакции).
Исходное и конечное
состояние химической реакции выражается
химическим уравнением.
Дайте определение понятию
«химическое уравнение».
Приведите пример уравнения.
Слайд 7

Сформулируйте понятия
«атом»,
«молекула»,
«ион» -
частиц,
из которых
состоят вещества.
Приведите формулы
этих частиц.
Слайд 8

Какие вещества называются индикаторами?
Приведите пример индикатора. Покажите его поведение в растворах
определенных веществ.
Слайд 9

Количество вещества (n) – физическая величина, характеризующая число частиц, содержащихся в
данной системе.
Рассчитайте объем кислорода, который займут
12·1024молекул.
(Не забудьте о числе Авогадро)
Слайд 10
В химии часто пользуются физической величиной «молярный объем».
Дайте определение этой
величине и рассчитайте с помощью ее объем углекислого газа массой 4,4 грамма.
Слайд 11
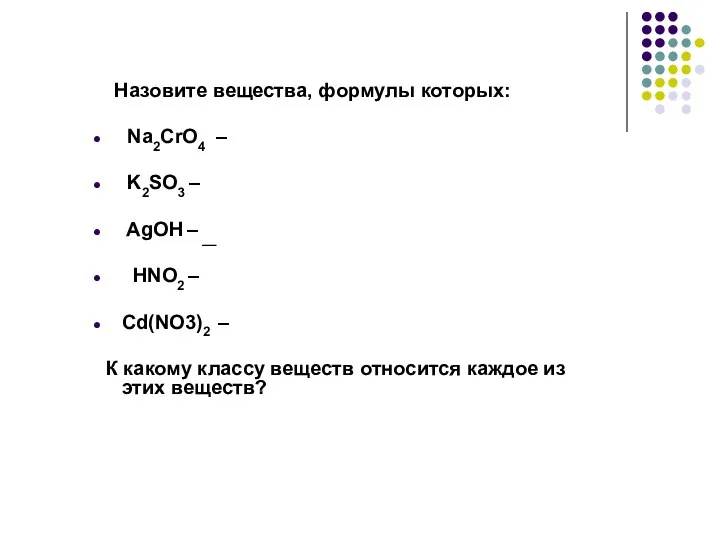
Назовите вещества, формулы которых:
Na2CrO4 –
K2SO3 –
AgOH –
__
HNO2 –
Cd(NO3)2 –
К какому классу веществ относится каждое из этих веществ?
Слайд 12

Запишите формулы веществ
по их названиям:
ортофосфат кальция,
сульфид алюминия,
угольная кислота,
гидроксид
хрома (III),
силикат натрия.
К какому классу веществ относится каждое из этих веществ?
Слайд 13
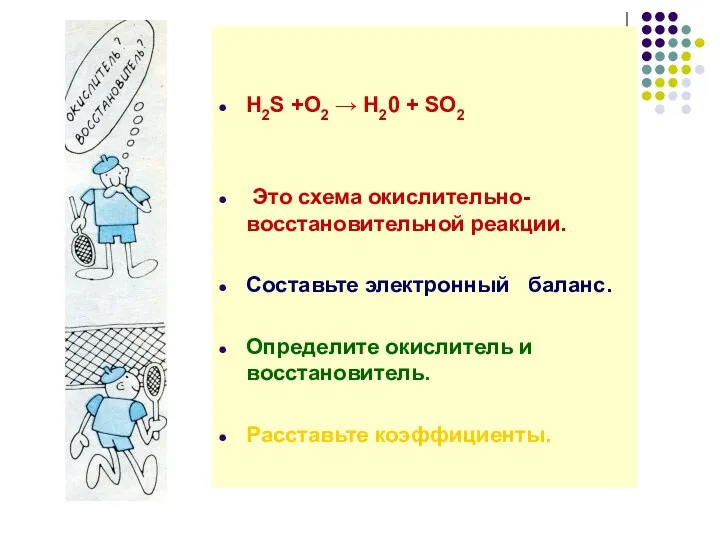
H2S +O2 → H20 + SO2
Это схема окислительно-восстановительной реакции.
Составьте
электронный баланс.
Определите окислитель и восстановитель.
Расставьте коэффициенты.
Слайд 14
Существует класс сложных веществ, получившие свое название из-за своего кислого вкуса,
который имеют большинство представителей.
Почему растворы этих веществ имеют этот вкус?
Для веществ этого класса характерна реакция нейтрализации.
Дайте определение этой реакции.
Приведите пример химической реакции нейтрализации в молекулярном, полном и кратком ионном виде.
Слайд 15

Вспомните,
какой химический процесс
называется горением.
Каковы условия, необходимые для
прекращения процесса горения ?
Слайд 16

Как в походных условиях очистить и обеззаразить мутную воду и сделать
ее пригодной для питья и приготовления пищи?















 Презентация проекта сюжетно-ролевой игры Поликлиника
Презентация проекта сюжетно-ролевой игры Поликлиника Иммунопатологиялық үрдістер
Иммунопатологиялық үрдістер Оптимизация добычи скважинной продукции путем подбора рациональной технологии и борьбы с осложнениями
Оптимизация добычи скважинной продукции путем подбора рациональной технологии и борьбы с осложнениями Региональная составляющая национального проекта Здравоохранение
Региональная составляющая национального проекта Здравоохранение Мастер-класс Ромашка. Презентация
Мастер-класс Ромашка. Презентация Безопасность жизнедеятельности в условиях социальной среды
Безопасность жизнедеятельности в условиях социальной среды Физическое воспитание детей школьного возраста. Основы юношеского спорта
Физическое воспитание детей школьного возраста. Основы юношеского спорта Замкнутые СУЭП постоянного тока. (Тема 3)
Замкнутые СУЭП постоянного тока. (Тема 3) Презентация к классному часуСимволы России.
Презентация к классному часуСимволы России. Арт - терапия и ее виды
Арт - терапия и ее виды Туберкулез костей и суставов
Туберкулез костей и суставов Программированное задание по теме Углерод и кремний. Химия - 9 класс. Диск
Программированное задание по теме Углерод и кремний. Химия - 9 класс. Диск Задания по английскому языку (вариант 1)
Задания по английскому языку (вариант 1) Механическая обработка молочного сырья
Механическая обработка молочного сырья Рок-гурт Океан Ельзи
Рок-гурт Океан Ельзи Задачи на дроби
Задачи на дроби РБФ-сети. НС Хопфилда. НС Кохонена
РБФ-сети. НС Хопфилда. НС Кохонена Дорожные знаки
Дорожные знаки Глаукома: как распознать и что делать
Глаукома: как распознать и что делать Цена и ценообразование. Тема 6
Цена и ценообразование. Тема 6 Киемнәр кибетендә. Яңа лексика
Киемнәр кибетендә. Яңа лексика Сырьевые, материальные и топливно-энергетические ресурсы
Сырьевые, материальные и топливно-энергетические ресурсы Верховный бог Олимпа Зевс
Верховный бог Олимпа Зевс Основи сіткового і календарного планування проєктів
Основи сіткового і календарного планування проєктів Хронический холецистит
Хронический холецистит Акция Птицы Кубани. Операция День птиц
Акция Птицы Кубани. Операция День птиц Инвертор сварочный IW-160/7.1ATL
Инвертор сварочный IW-160/7.1ATL ОРКСЭ Монастыри4 класс
ОРКСЭ Монастыри4 класс