Содержание
- 2. О каком элементе идёт речь? Задачи: закрепить и углубить теоретические знания учащихся о химических свойствах кислорода.
- 3. Тема урока: «Кислород» Задачи: закрепить и углубить теоретические знания учащихся о химических свойствах кислорода. Познакомить учащихся
- 4. Записываем тему и говорим о девизе урока 1. Элемент кислород находится в VI группе главной подгруппы.
- 5. Получение кислорода Имеется много способов получения кислорода, но в лаборатории его получают так: t 2KMnO4 H2MnO4
- 6. Ребята, что при этом образуется? Оксиды. S + O2 = SO2 SO2 + H20 = H2SO4
- 7. А теперь, давайте посмотрим, как же ребята приготовили опыт: Посмотрите как происходит горение угля t 2KNO3
- 8. Какими же свойствами обладает кислород? В кислороде все вещества горят или окисляются. Записываем уравнения реакций: H2S
- 9. Записываем уравнения реакций в тетрадях и на доске. 1. Проверяем правильные ответы: 2H2S + 3O2 =
- 10. А теперь ребята немного поиграем. Нужно составить формулы солей, используя кислород, комбинируя ниже приведенные составные части.
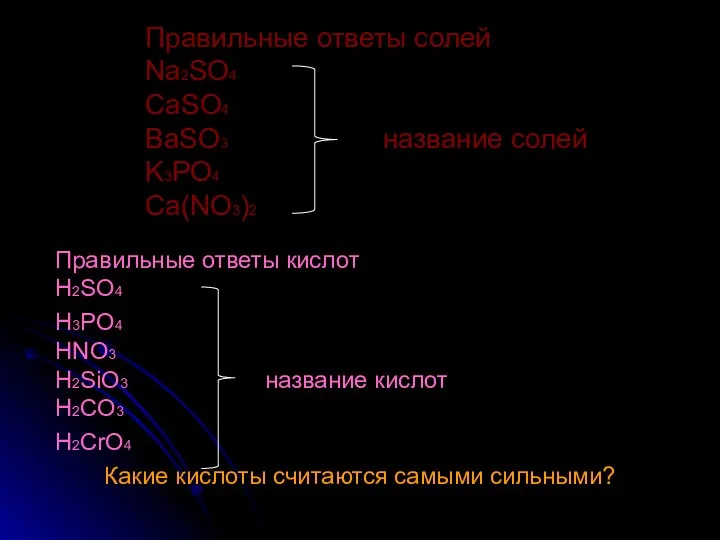
- 11. Правильные ответы солей Na2SO4 CaSO4 BaSO3 название солей K3PO4 Ca(NO3)2 Правильные ответы кислот H2SO4 H3PO4 HNO3
- 12. 1. Осуществите уравнения реакций следующих превращений: P P2O5 H3PO4 Na3PO4 S SO2 SO3 H2SO4 H3PO4. 2.
- 13. Кроссворд Единица количества вещества Русский композитор и химик Темно-бурая жидкость Химический элемент, самый легкий газ Инертный
- 14. Единица количества вещества Русский композитор и химик Темно-бурая жидкость Химический элемент, самый легкий газ Инертный газ
- 15. Единица количества вещества Русский композитор и химик Темно-бурая жидкость Химический элемент, самый легкий газ Инертный газ
- 16. Единица количества вещества Русский композитор и химик Темно-бурая жидкость Химический элемент, самый легкий газ Инертный газ
- 17. Единица количества вещества Русский композитор и химик Темно-бурая жидкость Химический элемент, самый легкий газ Инертный газ
- 18. Единица количества вещества Русский композитор и химик Темно-бурая жидкость Химический элемент, самый легкий газ Инертный газ
- 19. Единица количества вещества Русский композитор и химик Темно-бурая жидкость Химический элемент, самый легкий газ Инертный газ
- 20. Единица количества вещества Русский композитор и химик Темно-бурая жидкость Химический элемент, самый легкий газ Инертный газ
- 21. Единица количества вещества Русский композитор и химик Темно-бурая жидкость Химический элемент, самый легкий газ Инертный газ
- 22. Единица количества вещества Русский композитор и химик Темно-бурая жидкость Химический элемент, самый легкий газ Инертный газ
- 23. Применение кислорода Кислород применяют в металлургии и химической промышленности. При резке и сварке металлов. При дыхании.
- 25. Скачать презентацию





















 Компетентностный подход к решению проблем образования
Компетентностный подход к решению проблем образования Урок доброты
Урок доброты Развивающая игра Угадай эмоцию
Развивающая игра Угадай эмоцию Собрание родителей будущих первоклассников
Собрание родителей будущих первоклассников Социально-экономическая характеристика Донецкого региона в ХVІІІ веке
Социально-экономическая характеристика Донецкого региона в ХVІІІ веке Храм во имя иконы Божьей Матери Целительница
Храм во имя иконы Божьей Матери Целительница Технологія процесів первинної переробки нафти
Технологія процесів первинної переробки нафти Экспертные модели бизнес-процессов. Экспертные сравнения
Экспертные модели бизнес-процессов. Экспертные сравнения Метрополитен желілерін жобалау
Метрополитен желілерін жобалау Болгария
Болгария Общие положения ультразвуковой дефектоскопии
Общие положения ультразвуковой дефектоскопии Цифровая схемотехника. Базовые элементы цифровых интегральных схем
Цифровая схемотехника. Базовые элементы цифровых интегральных схем Сравнительный подход к оценке недвижимости. (Тема 8)
Сравнительный подход к оценке недвижимости. (Тема 8) Главные члены предложения. Подлежащее
Главные члены предложения. Подлежащее Технологический расчет участка по ремонту коробки передач
Технологический расчет участка по ремонту коробки передач Значение культурного наследия в истории человечества
Значение культурного наследия в истории человечества Специфика проверки и оценивания задач ЕГЭ по математике с развернутым ответом. Вопросы теории равносильности
Специфика проверки и оценивания задач ЕГЭ по математике с развернутым ответом. Вопросы теории равносильности Занятие по предшкольной подготовке Дикие животные
Занятие по предшкольной подготовке Дикие животные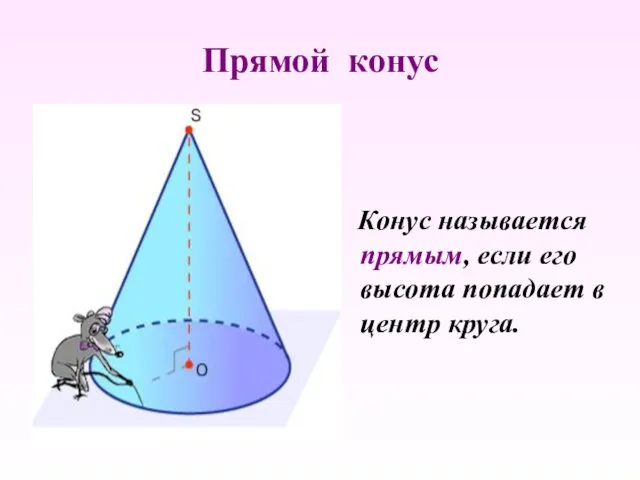 Прямой конус
Прямой конус Повторение изученного в 10 классе: Работа, мощность, законы сохранения. Тест
Повторение изученного в 10 классе: Работа, мощность, законы сохранения. Тест Особенности конструктивного мышления, как условие развития математических способностей детей старшего дошкольного возраста
Особенности конструктивного мышления, как условие развития математических способностей детей старшего дошкольного возраста гг
гг Мой класс 9 а
Мой класс 9 а Аталық жыныс мүшелері
Аталық жыныс мүшелері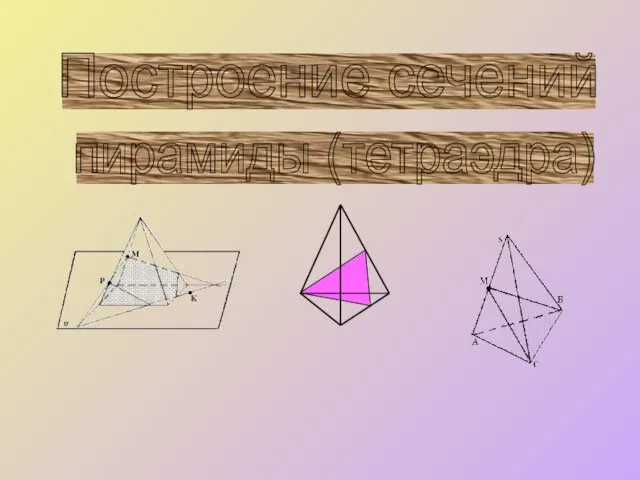 Построение сечений пирамиды (тетраэдра)
Построение сечений пирамиды (тетраэдра) Методы повышения нефтеотдачи пласта и интенсификации добычи. Цели методов повышения нефтеотдачи
Методы повышения нефтеотдачи пласта и интенсификации добычи. Цели методов повышения нефтеотдачи Личные местоимения
Личные местоимения Статическая устойчивость
Статическая устойчивость