Содержание
- 2. Общая характеристика nS2nP3 – строение внешнего энергетического уровня На внешнем уровне 5 электронов Увеличивается количество энергетических
- 3. Азот – простое вещество Молекула азота (:N N:) N2 В молекуле имеются одна σ- и две
- 4. Химические свойства азота Молекула азота очень устойчива (три ковалентные связи), поэтому обладает низкой реакционной способностью. В
- 5. Восстановительные свойства атомы проявляют при взаимодействии с кислородом при температуре электрической дуги N20 + O2 2N+2O
- 6. Получение азота Промышленный способ: Перегонка жидкого воздуха. Лабораторный способ: Разложение нитрита аммония: NH4NO2 N2 + 2H2O
- 7. А м м и а к NH3 Молекула полярная, имеет форму треугольной пирамиды с атомом азота
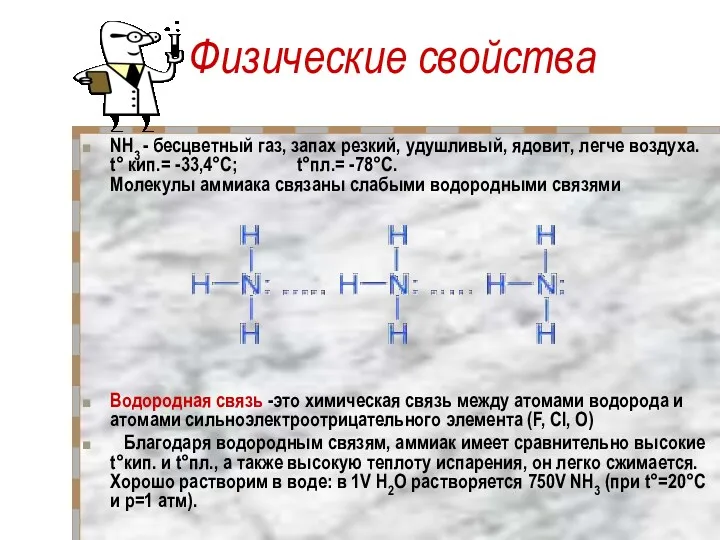
- 8. Физические свойства NH3 - бесцветный газ, запах резкий, удушливый, ядовит, легче воздуха. t° кип.= -33,4°C; t°пл.=
- 9. В хорошей растворимости аммиака можно убедиться на следующем опыте. Сухую колбу наполняют аммиаком и закрывают пробкой,
- 10. Получение Промышленный способ: N2 + 3H2 2NH3 (p=1000 атм; t°= 500°C; kat). Лабораторный способ: Нагревание солей
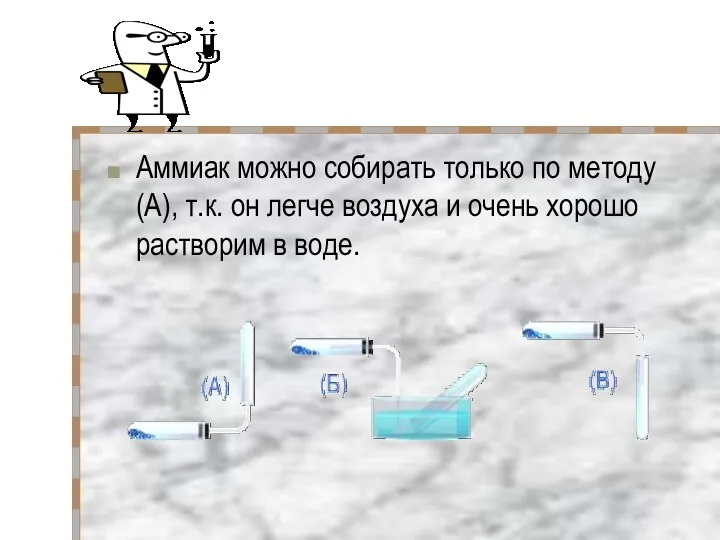
- 11. Аммиак можно собирать только по методу (А), т.к. он легче воздуха и очень хорошо растворим в
- 12. Химические свойства NH3 Образование ковалентной связи по донорно-акцепторному механизму Такой механизм образования связи, который возникает за
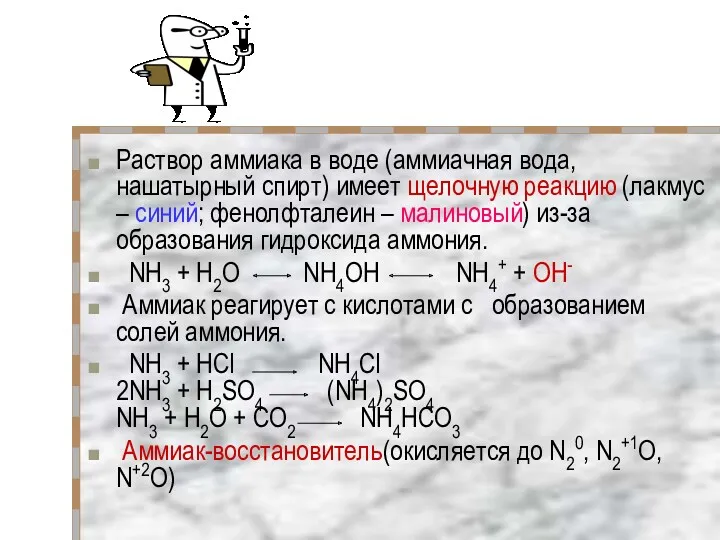
- 13. Раствор аммиака в воде (аммиачная вода, нашатырный спирт) имеет щелочную реакцию (лакмус – синий; фенолфталеин –
- 14. Горение в кислороде без катализатора 4N-3H3 + 3O2 2 N2 + 6Н2O каталитическое окисление ( kat
- 15. Соли аммония Соли аммония – сложные вещества, в состав которых входят катионы аммония NH4+, связанные с
- 16. Химические свойства солей аммония Сильные электролиты (диссоциируют в водных растворах) NH4Cl NH4+ + Cl- Разложение при
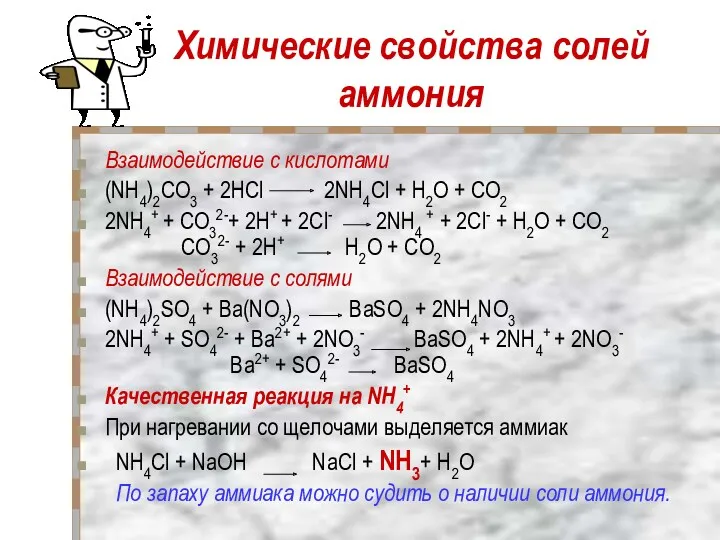
- 17. Химические свойства солей аммония Взаимодействие с кислотами (NH4)2CO3 + 2НCl 2NH4Cl + Н2O + CO2 2NH4+
- 18. Применение солей аммония Хлорид аммония NH4Cl: используют при паянии, он очищает поверхность металла от оксидной пленки,
- 19. Оксиды азота N2+1O, N+2O, N2+3O3, N+4O2 ,N2+5O5 Оксиды N2O, NO несолеобразующие, а остальные оксиды проявляют свойства
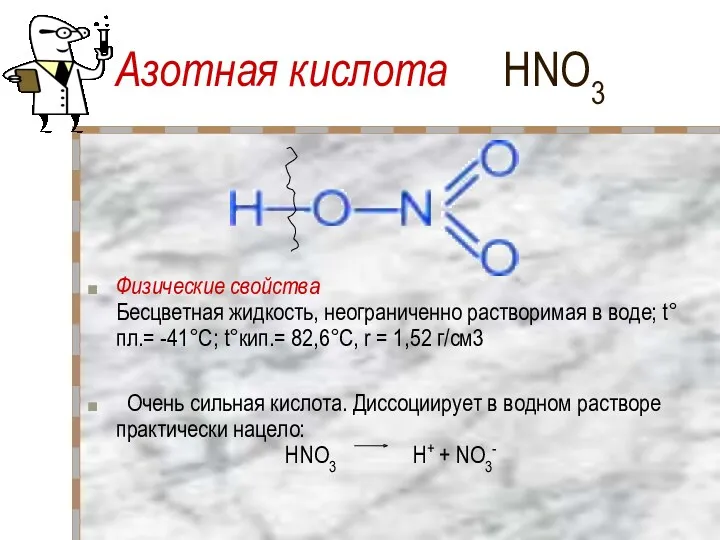
- 20. Азотная кислота HNO3 Физические свойства Бесцветная жидкость, неограниченно растворимая в воде; t°пл.= -41°C; t°кип.= 82,6°С, r
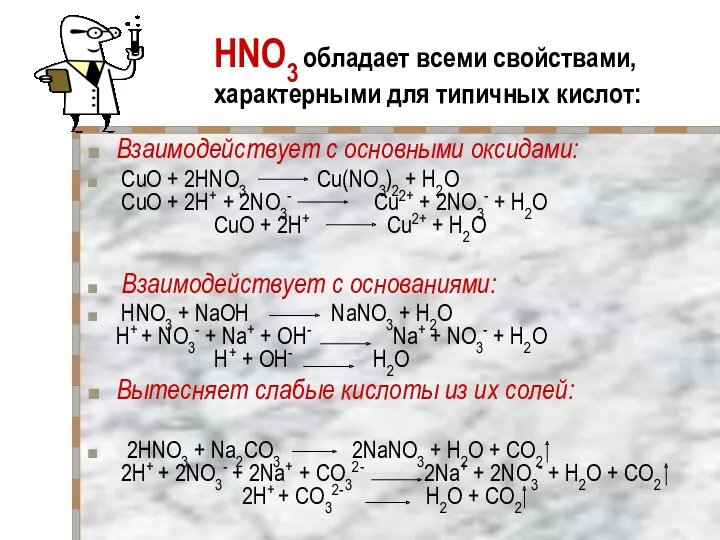
- 21. HNO3 обладает всеми свойствами, характерными для типичных кислот: Взаимодействует с основными оксидами: CuO + 2HNO3 Cu(NO3)2
- 22. Специфические свойства азотной кислоты HNO3 сильный окислитель Разлагается на свету и при нагревании 4HNO3 2H2O +
- 23. Окислительные свойства HNO3 Взаимодействие с металлами: Fe, Al, Cr, Au, Pt HNO3 пассивирует (без нагревания) Окислительные
- 24. Окислительные свойства HNO3 Взаимодействие с неметаллами: Азотная кислота превращается в NO (или в NO2); неметаллы окисляются
- 25. Соли азотной кислоты-нитраты Нитраты щелочных металлов разлагаются до нитритов: 2NaNO3 2NaNO2 + O2 Нитраты менее активных
- 26. Значение азота Азот- жизненно важный элемент. Все основные части клеток организма построены из белковых молекул, в
- 28. Скачать презентацию



















 Календари религий мира
Календари религий мира День семьи, любви и верности
День семьи, любви и верности Энергия приливов и отливов. Энергия волн океана. Малые ГЭС
Энергия приливов и отливов. Энергия волн океана. Малые ГЭС Лыжные гонки для детей старшего возраста
Лыжные гонки для детей старшего возраста Награды военных лет
Награды военных лет Теория функциональных систем П. К. Анохина
Теория функциональных систем П. К. Анохина Алексстрой. Ремонт квартир, домов и офисов в Анапе “под ключ”
Алексстрой. Ремонт квартир, домов и офисов в Анапе “под ключ” Использование мнемотехники в речевом развитии детей дошкольного возраста
Использование мнемотехники в речевом развитии детей дошкольного возраста Презентация Путешествие в музей
Презентация Путешествие в музей Типы плодов
Типы плодов The Postcrossing as motivation for studying of English
The Postcrossing as motivation for studying of English Аксиально-поршневые гидромашины
Аксиально-поршневые гидромашины Дифференциация звуков [Ч -Ть]
Дифференциация звуков [Ч -Ть] Фундаменты под оборудование
Фундаменты под оборудование Предмет и метод бухгалтерского учета
Предмет и метод бухгалтерского учета Научные школы теории организации
Научные школы теории организации Виды нивелирования
Виды нивелирования Why You Need to Measure Both BER and MER on QAM Digital Signals
Why You Need to Measure Both BER and MER on QAM Digital Signals презентация к уроку технология 1 класс УМК Гармония Учимся вырезать снежинку
презентация к уроку технология 1 класс УМК Гармония Учимся вырезать снежинку Сәламәт тәндә - сәламәт акыл
Сәламәт тәндә - сәламәт акыл Тайная вечеря Леонардо да Винчи
Тайная вечеря Леонардо да Винчи Вычисление площади плоской фигуры с помощью определенного интеграла
Вычисление площади плоской фигуры с помощью определенного интеграла Геотермалдық энергиясы
Геотермалдық энергиясы Многофункциональный жилой дом
Многофункциональный жилой дом презентация проекта Детская филармония
презентация проекта Детская филармония Предпосылки образования СССР
Предпосылки образования СССР Организация исследовательское деятельности в учебном процессе. Из опыта работы учителя географии
Организация исследовательское деятельности в учебном процессе. Из опыта работы учителя географии Как создавать газету
Как создавать газету