Слайд 2

Цель урока
повторить понятия: «химическая формула», «индекс», «коэффициент»
продолжить вычислять относительные молекулярные массы
веществ
научиться определять массовую долю химического элемента в сложном веществе.
Слайд 3
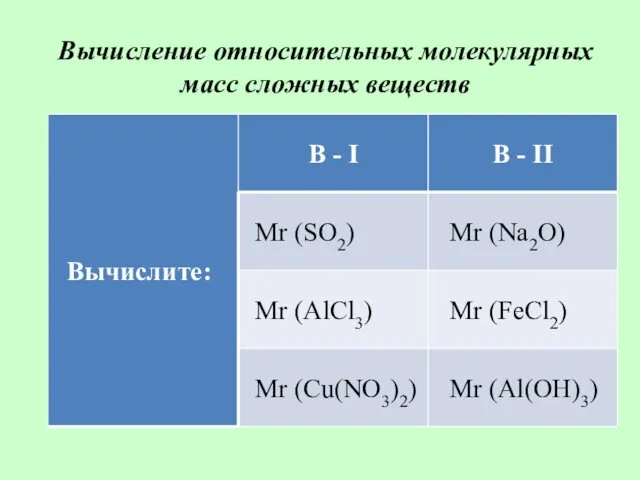
Вычисление относительных молекулярных масс сложных веществ
Слайд 4
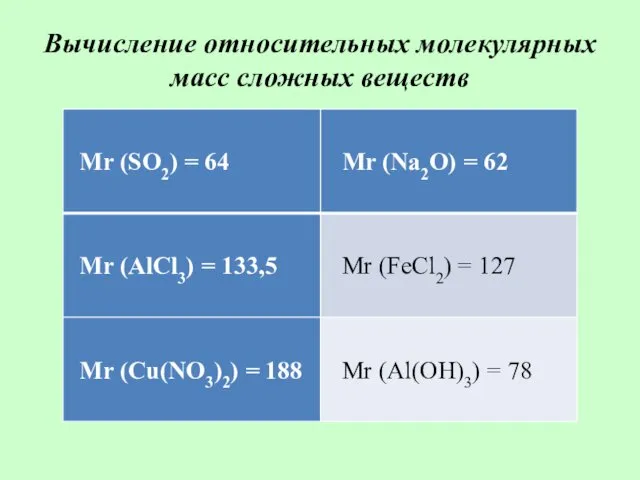
Вычисление относительных молекулярных масс сложных веществ
Слайд 5

Вычислите массовую долю каждого из элементов в сульфате меди (II) CuSO4.
Слайд 6

Массовая доля элемента
Показывает какую часть (долю) составляет масса данного элемента от
всей массы вещества
Обозначается ω (э)
Измеряется в %
ω (Э) = 100%
n – число атомов
Аr – относительная атомная масса элемента
Мr - относительная молекулярная масса вещества
Слайд 7

Задача №1. В каком из веществ больше массовая доля серы в
Na2S или в SO3?
Слайд 8

Задача №2
Относительная молекулярная масса вещества, формула которого ХNО 3 , равна
101.
Определите, атом какого элемента обозначен букой Х.
Укажите, какую информацию о веществе несет выведенная формула.
Найдите массовую долю кислорода в соединении.







 Как человек поехал по железной дороге
Как человек поехал по железной дороге Праздники в религиях мира
Праздники в религиях мира Дети моей группы Звёздочки
Дети моей группы Звёздочки Христианские представления о нравственности. Заповеди Божии
Христианские представления о нравственности. Заповеди Божии Безопасность детей в сети Интернет
Безопасность детей в сети Интернет 20231112_umniki_i_umnitsy
20231112_umniki_i_umnitsy Спальное белье. Хлопок, поплин, бязь
Спальное белье. Хлопок, поплин, бязь Химические свойства металлов
Химические свойства металлов Обеспечение химической защиты
Обеспечение химической защиты Содержание психолого-педагогической работы по физической культуре
Содержание психолого-педагогической работы по физической культуре фотоотчёт открытого занятия
фотоотчёт открытого занятия Исследовательский проект Тайны старинной книги
Исследовательский проект Тайны старинной книги Mobile Phone
Mobile Phone Не хочу делать уроки!
Не хочу делать уроки! Разработка интерактивного расписания занятий учебного учреждения
Разработка интерактивного расписания занятий учебного учреждения Технология групповой работы в начальной школе.
Технология групповой работы в начальной школе. Храмы России
Храмы России Роль драматизации в жизни дошкольника
Роль драматизации в жизни дошкольника Внесение изменений в РД и ПД. Оформление. Памятка
Внесение изменений в РД и ПД. Оформление. Памятка Средства наблюдения
Средства наблюдения My winter. Holidays were. Fantastic
My winter. Holidays were. Fantastic ОАО Судостроительный завод Северная верфь
ОАО Судостроительный завод Северная верфь Использование маркетинговых стратегий компанией ОАО РЖД
Использование маркетинговых стратегий компанией ОАО РЖД Нам нужны такие корабли на море
Нам нужны такие корабли на море Мой край . ПрезентацияЛишь в Усть-Цильме водят горку.
Мой край . ПрезентацияЛишь в Усть-Цильме водят горку. Субботники
Субботники Беспроводные технологии передачи данных
Беспроводные технологии передачи данных Комплекс решений в строительстве скважин с большим отходом от вертикали
Комплекс решений в строительстве скважин с большим отходом от вертикали