Слайд 2
Спектроскопи́я я́дерного магни́тного резона́нса, ЯМР-спектроскопия —
спектроскопический метод исследования химических объектов, использующий явлениеядерного
магнитного резонанса. Наиболее важными для химии и практических применений являются спектроскопия протонного магнитного резонанса (ПМР-спектроскопия), а также спектроскопия ЯМР на ядрах углерода-13 (13C ЯМР-спектроскопия), фтора-19 (19F ЯМР-спектроскопия), фосфора-31 (31P ЯМР-спектроскопия).
.
Слайд 3

Базовая ЯМР техника
Образец вещества для ЯМР помещается в тонкостенную стеклянную трубку
(ампулу). Когда её помещают в магнитное поле, ЯМР активные ядра (такие как 1H или 13C) поглощают электромагнитную энергию. Резонансная частота, энергия абсорбции и интенсивность испущенного сигнала пропорциональны силе магнитного поля. Так, в поле в 21 Тесла протон резонирует при частоте 900 МГц.
Слайд 4

Химический сдвиг
В зависимости от местного электронного окружения разные протоны в молекуле
резонируют на слегка отличающихся частотах. Так как и это смещение частоты, и основная резонансная частота прямо пропорциональны величине индукции магнитного поля, то это смещение преобразуется в независимую от магнитного поля безразмерную величину, известную как химический сдвиг. Химический сдвиг определяется как относительное изменение относительно некоторых эталонных образцов. Частотный сдвиг экстремально мал в сравнении с основной ЯМР частотой. Типичный сдвиг частоты равен 100 Гц, тогда как базовая ЯМР частота имеет порядок 100 МГц. Таким образом, химический сдвиг часто выражается в частях на миллион (ppm). Для того чтобы обнаружить такое маленькое различие частоты, приложенное магнитное поле должно быть постоянным внутри объёма образца.
Слайд 5

Спин-спиновое взаимодействие
Наиболее полезную информацию для определения структуры в одномерном ЯМР-спектре даёт
так называемое спин-спиновое взаимодействие между активными ЯМР ядрами. Это взаимодействие возникает в результате переходов между различными спиновыми состояниями ядер в химических молекулах, что приводит к расщеплению сигналов ЯМР. Это расщепление может быть простым и сложным и, как следствие, его либо просто интерпретировать, либо оно может запутать экспериментатора.
Это связывание обеспечивает детальную информацию о связях атомов в молекуле.
Слайд 6

Взаимодействие второго порядка (сильное)
Простое спин-спиновое взаимодействие предполагает, что константа взаимодействия мала
в сравнении с разницей в химических сдвигах между сигналами. Если разность сдвигов уменьшается (или константа взаимодействия увеличивается), интенсивность мультиплетов образцов искажается, становится более сложной для анализа (особенно если система содержит более 2 спинов). Однако в мощных ЯМР-спектрометрах искажения обычно умеренные и это позволяет легко интерпретировать связанные пик
Слайд 7

Приложение ЯМР спектроскопии к исследованию белков
Большинство последних инноваций в ЯМР спектроскопии
сделаны в так называемой ЯМР спектроскопии белков, которая становится очень важной техникой в современной биологии и медицине. Общей задачей является получение 3-мерной структуры белка в высоком разрешении, подобно изображениям, получаемым в рентгеновской кристаллографии. Из-за присутствия большего числа атомов в белковой молекулe в сравнении с простым органическим соединением, базовый 1H спектр переполнен перекрывающимися сигналами, поэтому прямой анализ спектра становится невозможным. Поэтому были разработаны многомерные техники, чтобы решить эту проблему.






 Мотивация Cash on Card
Мотивация Cash on Card Основы теории градостроительства. Понятие город. (Лекция 5)
Основы теории градостроительства. Понятие город. (Лекция 5) Изменения в деятельности учителя при переходе на ФГОС ООО
Изменения в деятельности учителя при переходе на ФГОС ООО Презентация Использование мнемотаблиц, схем, в познавательно - речевом развитии дошкольников
Презентация Использование мнемотаблиц, схем, в познавательно - речевом развитии дошкольников Christmas
Christmas Digital Systems. Chapter 5. Flip-Flops and Related Devices
Digital Systems. Chapter 5. Flip-Flops and Related Devices Magic spells from Harry Potter
Magic spells from Harry Potter презентация к статье контроль и самоконтроль учащихся ФГОС
презентация к статье контроль и самоконтроль учащихся ФГОС Фонд социального страхования
Фонд социального страхования Аналоговые электронные вольтметры
Аналоговые электронные вольтметры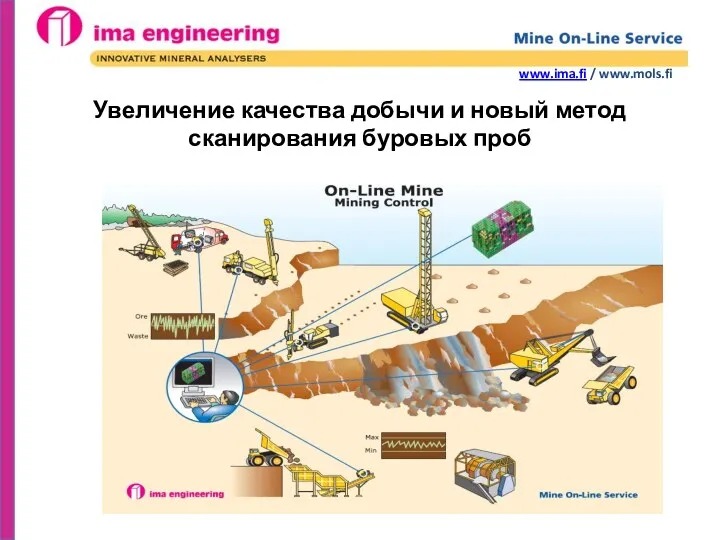 IMA Engineering. Увеличение качества добычи руды и новый метод сканирования буровых проб
IMA Engineering. Увеличение качества добычи руды и новый метод сканирования буровых проб Реформы 1990-х годов в России
Реформы 1990-х годов в России Дифференциальные уравнения и ряды. Степенные ряды
Дифференциальные уравнения и ряды. Степенные ряды Галогенпроизводные алифатических углеводородов
Галогенпроизводные алифатических углеводородов Концептуальные основы радиационной безопасности
Концептуальные основы радиационной безопасности Основной государственный экзамен по русскому языку в 9 классе. Подготовка к написанию сочинения-рассуждения (15.2)
Основной государственный экзамен по русскому языку в 9 классе. Подготовка к написанию сочинения-рассуждения (15.2) Русская культура в XVI - XVIII веках
Русская культура в XVI - XVIII веках Проект Создание коллажа
Проект Создание коллажа Презентация учителя русского языка и литературы
Презентация учителя русского языка и литературы Искусство и духовная жизнь
Искусство и духовная жизнь Образовательная область Здоровье
Образовательная область Здоровье Общеразвивающие упражнения
Общеразвивающие упражнения Формы взаимодействия детского сада с родителями
Формы взаимодействия детского сада с родителями о.ю
о.ю Как мы следы осени искали
Как мы следы осени искали Welcome to WeOptimum Customer Support Center
Welcome to WeOptimum Customer Support Center Типовые звенья
Типовые звенья Смешарики. Английский для детей
Смешарики. Английский для детей