Слайд 2

Золото (Au)
Атомный номер:79
Номер периода:9
Строение атома:)2)8)18)32)18 )1
Степень окисления:+3
Оксиды:Au2O
Взаимодействие с другими веществами:Кроме
галогенов ни с чем не взаимодействует ( неметаллами ) .
Использование:В медицине , ювелирные изделия , изготовление слитков .
В природе:В растениях , в организме человека и животных .
Слайд 3

Происхождение Золото
Зарядовое число 79 золота делает его одним из высших по
количеству протонов элементов,которые встречаются в природе.
Слайд 4

Химические свойства
Золото — один из самых инертных металлов, стоящий в ряду напряжений правее всех
других металлов. При нормальных условиях оно не взаимодействует с большинством кислот и не образует оксидов, поэтому его относят к благородным металлам, в отличие от обычных металлов, разрушающихся под действием кислот и щелочей.
Ковалентный радиус: 134 пм
Радиус иона: (-3е) 185 (+1е) 137 пм
Электро-отрицательность: 2,64 (шкала Полинга)
Электродный потенциал: Au←Au³+ 1,50 B,Au←Au+1,70B
Степени окисления: -1,1,3,5
Энергия ионизации: 889,3 (9,22) кДж/моль
Слайд 5

Физические свойства
Чистое золото — мягкий металл жёлтого цвета. Красноватый оттенок некоторым изделиям из золота,
например, монетам, придают примеси других металлов, в частности, меди. В тонких плёнках золото просвечивает зелёным. Золото обладает высокой теплопроводностью и низким электрическим сопротивлением.
Слайд 6

Добыча золота
Люди добывают золото с незапамятных времён. С золотом человечество столкнулось
уже в V тыс. до н. э. в эпоху неолита благодаря его распространению в самородном состоянии.
Слайд 7

Получение золота
Для получения золота используются его основные физические и химические свойства: присутствие в
природе в самородном состоянии, способность реагировать лишь с немногими веществами (ртуть, цианиды). С развитием современных технологий более популярными становятся химические способы






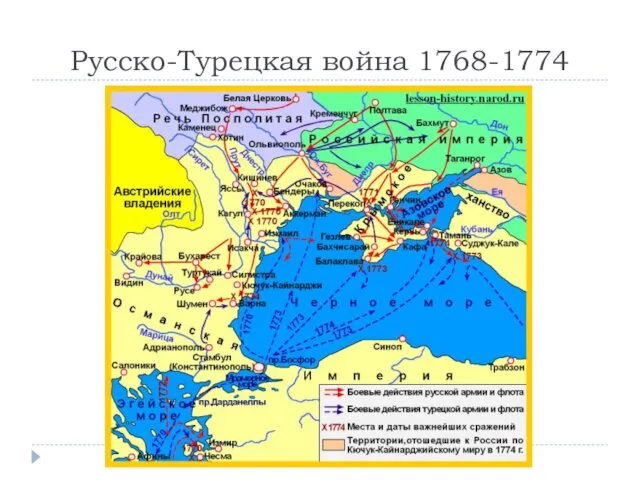 Русско-Турецкая война 1768-1774
Русско-Турецкая война 1768-1774 Виртуальный детский сад Хошенко Н.Д - мебель
Виртуальный детский сад Хошенко Н.Д - мебель Лихорадка. Типы нарушений терморегуляции
Лихорадка. Типы нарушений терморегуляции Анализ архитектуры исторического и современного города
Анализ архитектуры исторического и современного города Бакчада экологик тәрбия
Бакчада экологик тәрбия Эндогенные геологические процессы
Эндогенные геологические процессы Environnement matériel d’un système informatique
Environnement matériel d’un système informatique Сетевые проекты как интерактивное пространство взаимодействия педагога и учащихся в начальной школе.
Сетевые проекты как интерактивное пространство взаимодействия педагога и учащихся в начальной школе. Безопасность, гигиена, эргономика, ресурсосбережение. Эксплуатационные требования к компьютерному рабочему месту
Безопасность, гигиена, эргономика, ресурсосбережение. Эксплуатационные требования к компьютерному рабочему месту Новый год. Тогда и сейчас
Новый год. Тогда и сейчас Конспект и презентация к уроку Океанаия география 7 класс
Конспект и презентация к уроку Океанаия география 7 класс Технология разработки прогнозов разных уровней. Макроэкономическое прогнозирование
Технология разработки прогнозов разных уровней. Макроэкономическое прогнозирование Презентация подготовка к ЕГЭ №37 (С2) Реакции, подтверждающие взаимосвязь различных классов неорганических веществ Мысленный эксперимент Занятие №1 Ключевые слова
Презентация подготовка к ЕГЭ №37 (С2) Реакции, подтверждающие взаимосвязь различных классов неорганических веществ Мысленный эксперимент Занятие №1 Ключевые слова Рыночная экономика как система
Рыночная экономика как система Клетки, осуществляющие иммунный ответ
Клетки, осуществляющие иммунный ответ Правила написания сочетаний жи – ши
Правила написания сочетаний жи – ши Использование проекта в практике дошкольного образования.
Использование проекта в практике дошкольного образования. Дифракция и интерференция волн
Дифракция и интерференция волн Апостол Павел
Апостол Павел Система подготовки младших школьников к олимпиадам
Система подготовки младших школьников к олимпиадам Многообразие Земноводных. Amphibia
Многообразие Земноводных. Amphibia График линейной функции
График линейной функции Анализ и оценка обоснований нормативов потерь углеводородного сырья при добыче
Анализ и оценка обоснований нормативов потерь углеводородного сырья при добыче Электричество среди нас
Электричество среди нас Криминалистическая характеристика незаконного оборота наркотических средств. Этапы расследования
Криминалистическая характеристика незаконного оборота наркотических средств. Этапы расследования Бұрғылау кемелері
Бұрғылау кемелері Из опыта работы (презентация) Отчет классного руководителя
Из опыта работы (презентация) Отчет классного руководителя Системы счисления
Системы счисления