Государственный стандарт Республики Казахстан. Правовые основы стандартизации в Республике Казахстан презентация
Содержание
- 2. Государственный стандарт Республики Казахстан. Правовые основы стандартизации в Республике Казахстан впервые были установлены Законом Республики Казахстан
- 3. Основная цель закона - установление мер государственной защиты интересов потребителей и государства в вопросах качества и
- 4. Закон Республики Казахстан «О стандартизации» регламентирует: основные понятия в области стандартизации; сферу действия настоящего закона; законодательство
- 5. нормативные документы по стандартизации и требования к ним; применение нормативных документов; информацию о нормативных документах; планирование
- 6. Государственная система стандартизации Республики Казахстан В развитие Закона Республики Казахстан «О стандартизации» разработана Государственная система стандартизации
- 7. Основные задачи ГСС РК. Для достижения целей стандартизации, установленных законодательством, ГСС РК должна решать следующие основные
- 8. совершенствование действующего законодательства и переход на иные формы регулирования качества и безопасности продукции путем формирования в
- 9. Методологические вопросы организации и функционирования Государственной системы стандартизации изложены в комплексе государственных основополагающих стандартов «Государственная система
- 10. СТ РК 1.4-99 «ГСС РК. Стандарт фирмы. Основные положения». СТ РК 1.5-2000 «ГСС РК. Общие требования
- 11. Организация работ по стандартизации в Республике Казахстан Организационная структура Государственной системы стандартизации Республики Казахстан состоит из:
- 12. Комитет по стандартизации, метрологии и сертификации является государственным органом исполнительной власти, осуществляющим межотраслевую координацию, а также
- 13. участвует в работах по межгосударственной, международной, региональной стандартизации; организует и осуществляет проведение государственного надзора за соблюдением
- 14. В работах по стандартизации также участвуют органы государственною управления, юридические и физические лица, которые организуют и
- 15. Планирование работ по стандартизации Составление программ и планов государственной стандартизации находится в ведении Комитета по стандартизации,
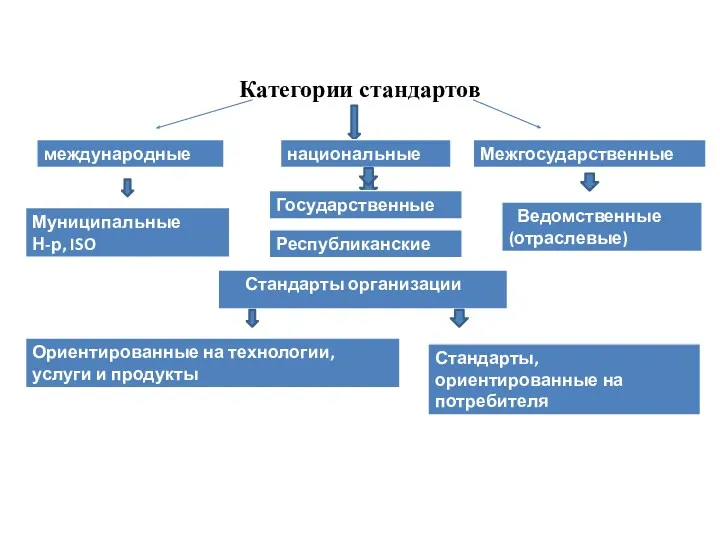
- 16. Категории стандартов
- 17. Международный стандарт – стандарт, принятый международной организацией. Национальный стандарт(государственный) стандарт - принятый национальным органом по стандартизации
- 18. Нормативные документы по стандартизации Категории нормативных документов по стандартизации Категорией нормативного документа по стандартизации называют его
- 19. МЕЖГОСУДАРСТВЕННАЯ СТАНДАРТИЗАЦИЯ В СОДРУЖЕСТВЕ НЕЗАВИСИМЫХ ГОСУДАРСТВ Межгосударственная система стандартизации (МГСС) Началом развития межгосударственной стандартизации в рамках
- 20. Для выработки согласованной политики в области стандартизации, метрологии и сертификации и определения основных направлений деятельности в
- 21. МЕЖДУНАРОДНАЯ И РЕГИОНАЛЬНАЯ СТАНДАРТИЗАЦИЯ Начало непосредственного сотрудничества различных стран в области стандартизации относится к 1921 году,
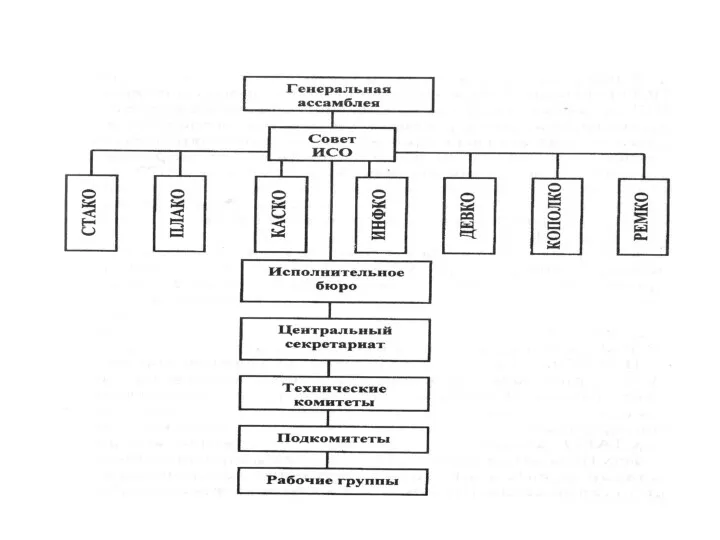
- 22. Высшим органом ИСО является Генеральная ассамблея - собрание должностных лиц и делегатов, назначенных членами. Каждый член
- 24. Международная электротехническая комиссия (МЭК) была создана в 1906 году 13 странами мира. МЭК занимается стандартизацией в
- 25. Участие международных организаций в работах по стандартизации [Из общего числа четырех с лишним тысяч международных организаций
- 26. Международная торговая палата известна работами по унификации торговой документации и сборником «ИНКОТЕРМС» - международными правилами толкования
- 27. Региональные организации по стандартизации В мире действует семь региональных организаций по стандартизации, подобных МГС, - в
- 28. Добровольности; Единства целостности национальной системы стандартизации; Обеспечения системности и комплексности стандартизации; Разработки и приятности национальных стандартов;
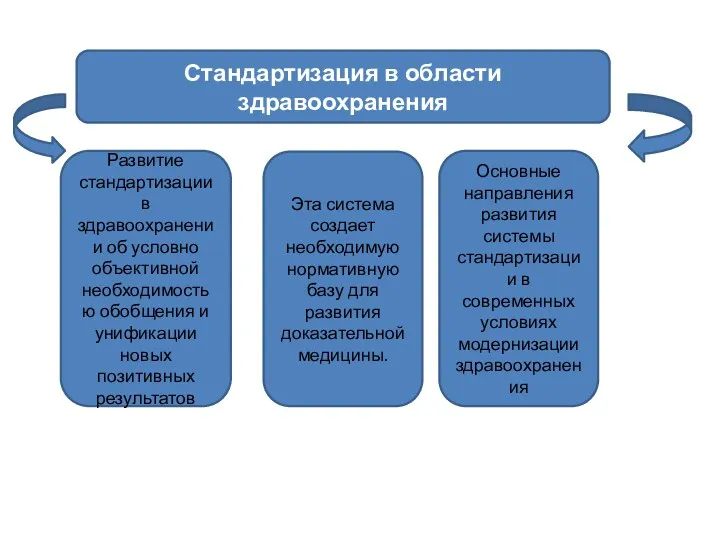
- 29. Стандартизация в области здравоохранения Развитие стандартизации в здравоохранении об условно объективной необходимостью обобщения и унификации новых
- 30. Область применения: Настоящий стандарт устанавливает общие требования к организации и выполнению научно- исследовательских работ(НИР); порядок выполнения
- 31. Надлежащая лабораторная практика / Правила лабораторной практики (Стандарт GLP — Good Laboratory Practice GLP): Система требований
- 32. Введение Надлежащая лабораторная практика (Good Laboratories Practice; GLP) устанавливает единый подход и единые требования к проведению
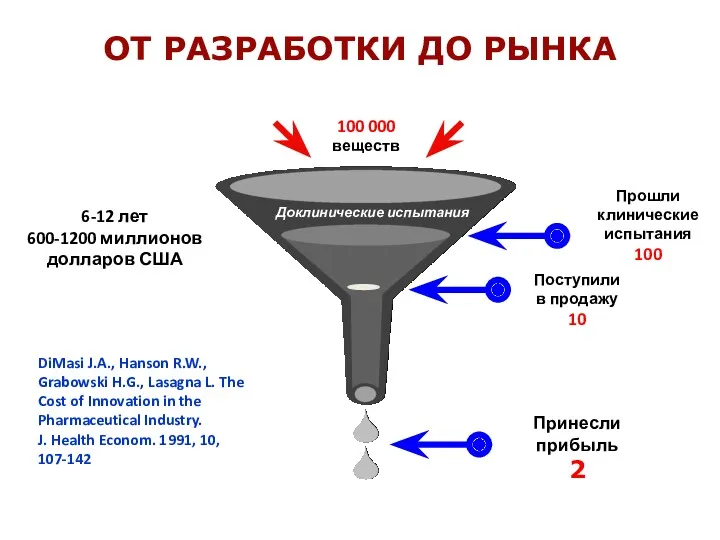
- 33. ОТ РАЗРАБОТКИ ДО РЫНКА 6-12 лет 600-1200 миллионов долларов США Прошли клинические испытания 100 100 000
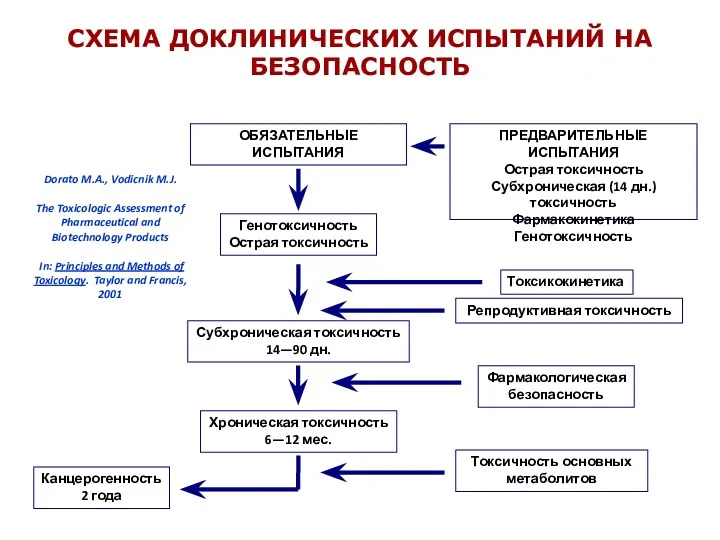
- 34. СХЕМА ДОКЛИНИЧЕСКИХ ИСПЫТАНИЙ НА БЕЗОПАСНОСТЬ
- 35. МЕЖДУНАРОДНЫЙ СТАНДАРТ «OECD Principles on Good Laboratory Practice» (OECD, ENV/MC/CHEM(98)17, 1997 г.) НАЦИОНАЛЬНЫЕ СТАНДАРТЫ «Принципы надлежащей
- 36. Организация и персонал испытательного центра Программа обеспечения качества Помещения Оборудование, материалы и реагенты Тест-системы Испытуемые и
- 37. 58.31 Руководство исследовательской организации (Testing facility management) 58.33 Руководитель исследования (Study director) 58.35 Группа обеспечения качества
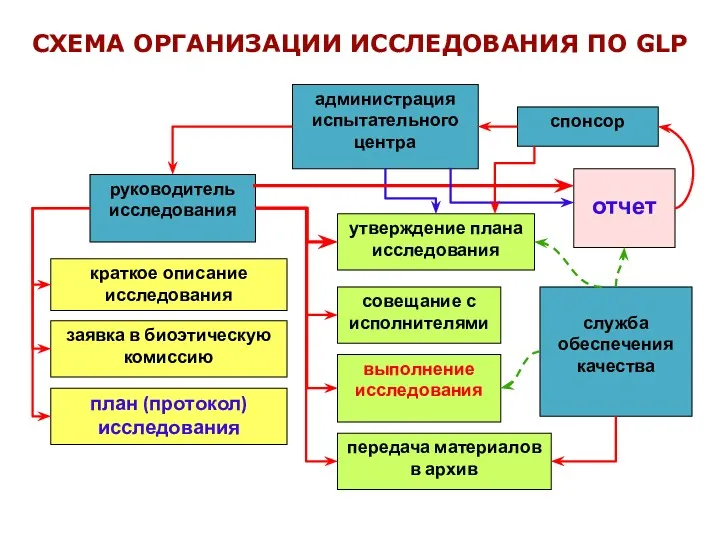
- 38. СХЕМА ОРГАНИЗАЦИИ ИССЛЕДОВАНИЯ ПО GLP руководитель исследования краткое описание исследования заявка в биоэтическую комиссию план (протокол)
- 39. ГОСУДАРСТВЕННЫЙ СТАНДАРТ РЕСПУБЛИКИ КАЗАХСТАН НАДЛЕЖАЩАЯ ЛАБОРАТОРНАЯ ПРАКТИКА. ОСНОВНЫЕ ПОЛОЖЕНИЯ СТ РК 1613-2006 Издание официальное Комитет по
- 40. Пункт 12. Руководитель организации согласовывает план доклинического исследования, организует работу по его выполнению, назначает ответственного исполнителя
- 41. Лаборатория имеет необходимое оборудование и укомплектована персоналом, имеющим соответствующее образование, квалификацию и опыт работы для выполнения
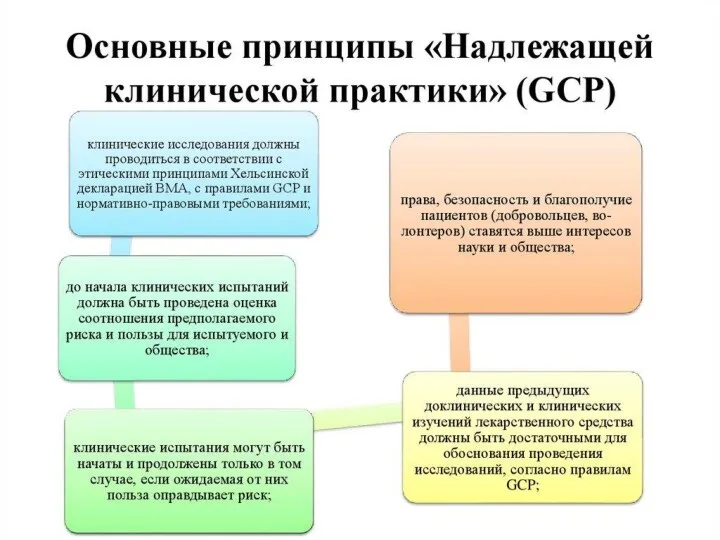
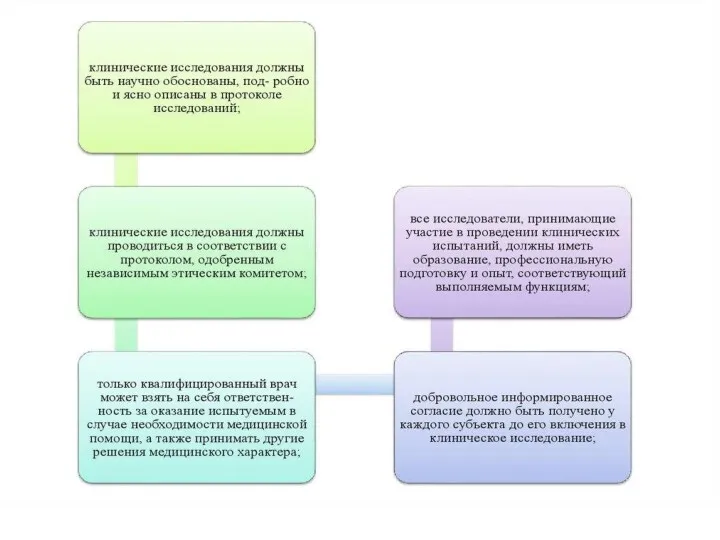
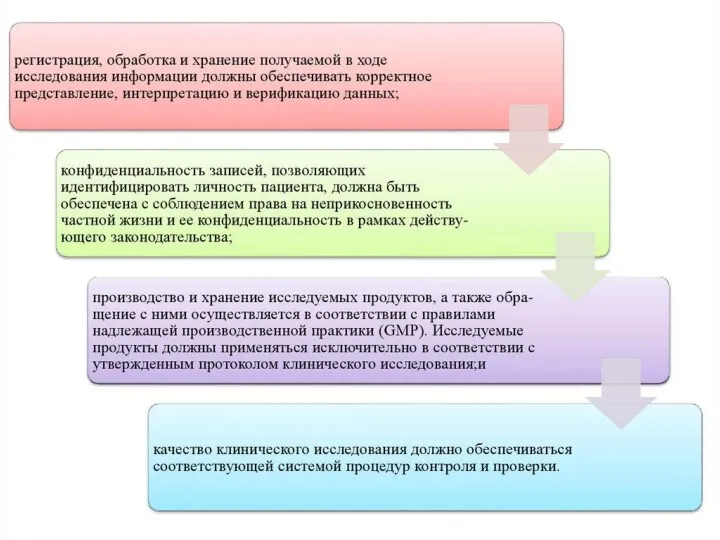
- 42. Стандарты клинических испытаний При проведении клинических испытаний исследователи всего мира руководствуются основными правилами GCP (Good Clinical
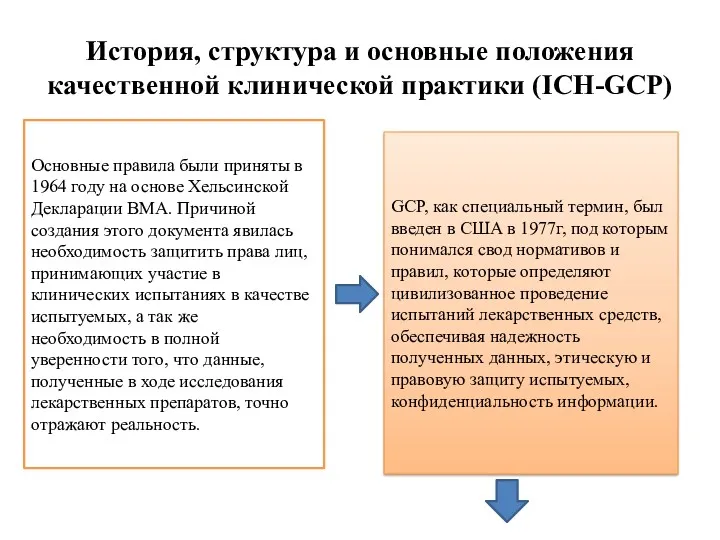
- 43. История, структура и основные положения качественной клинической практики (ICH-GCP) GCP, как специальный термин, был введен в
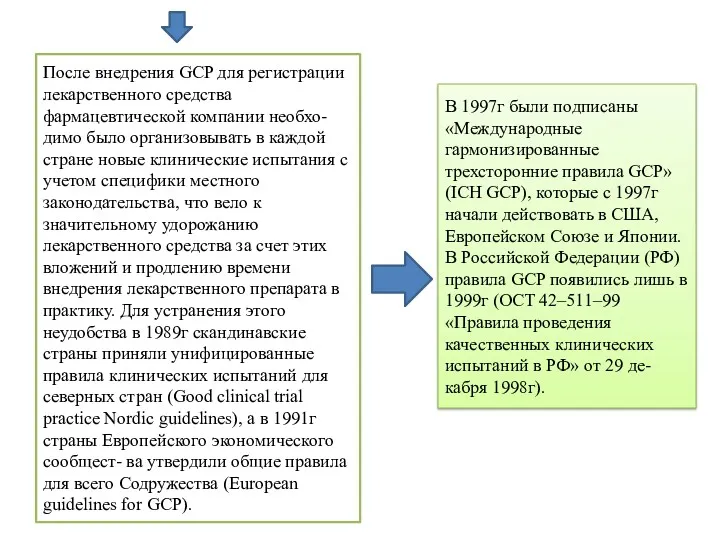
- 44. После внедрения GCP для регистрации лекарственного средства фармацевтической компании необхо- димо было организовывать в каждой стране
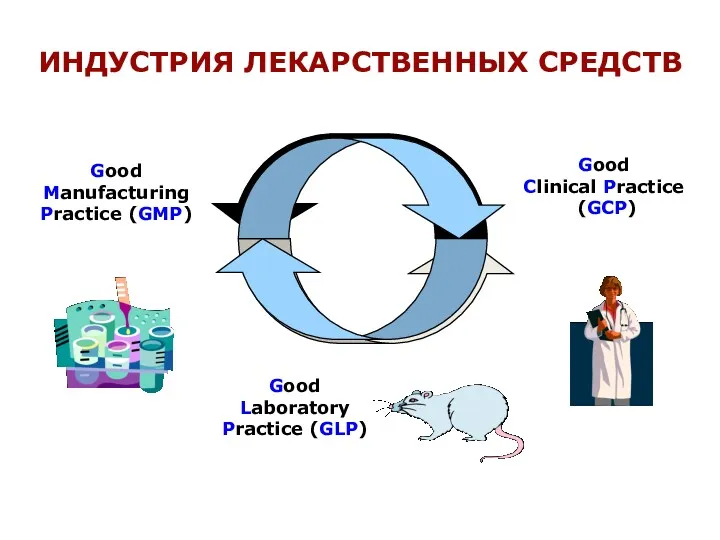
- 52. Вместе с GMP (Надлежащая производственная практика) и GLP (Надлежащая лабораторная практика ) GCP призван стандартизовать некоторые
- 53. Good Manufacturing Practice (GMP) Good Clinical Practice (GCP) Good Laboratory Practice (GLP) ИНДУСТРИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ
- 54. Нормативные ссылки В настоящем стандарте использованы ссылки на следующие нормативные документы: СТ РК 2.75-2004 Государственная система
- 56. Скачать презентацию









































 Соотношение информационного общества и государства
Соотношение информационного общества и государства Классификация прав человека
Классификация прав человека Сравнительный анализ различных контрактов
Сравнительный анализ различных контрактов Конституционный статус Президента Российской Федерации
Конституционный статус Президента Российской Федерации Конституция Российской Федерации
Конституция Российской Федерации Государственная услуга по приему от граждан анкет в целях регистрации в системе обязательного пенсионного страхования
Государственная услуга по приему от граждан анкет в целях регистрации в системе обязательного пенсионного страхования Социальное партнерство в сфере труда
Социальное партнерство в сфере труда Федеративное устройство России
Федеративное устройство России Принятие решений в процессе управления рисками. Инструментарий принятия решений в СУР
Принятие решений в процессе управления рисками. Инструментарий принятия решений в СУР Система кадровой документации
Система кадровой документации Основы теории государства и права. Правовые отношения
Основы теории государства и права. Правовые отношения О внесении изменений в ЖК РФ
О внесении изменений в ЖК РФ Логические и психологические основы судебно-экспертной деятельности
Логические и психологические основы судебно-экспертной деятельности Виды коррупции. Источники. Методы оценки
Виды коррупции. Источники. Методы оценки Рецидив преступлений
Рецидив преступлений Основные требования оформлению документа
Основные требования оформлению документа Административные наказания
Административные наказания Методика расследования вандализма
Методика расследования вандализма Этика обвинительной речи прокурора
Этика обвинительной речи прокурора Взаимодействие нарядов ППСП с гражданами. Помощь полиции. Тема № 3
Взаимодействие нарядов ППСП с гражданами. Помощь полиции. Тема № 3 Средства индивидуализации юридических лиц, товаров, работ, услуг и предприятий
Средства индивидуализации юридических лиц, товаров, работ, услуг и предприятий Предвыборная агитация
Предвыборная агитация Підстави звільнення від кримінальної відповідальності
Підстави звільнення від кримінальної відповідальності Пенсионный процесс
Пенсионный процесс Хозяйственное право
Хозяйственное право Реализация надзорной функции органами Госсанэпиднадзора. Организация проверок юридических лиц и индивидуальных предпринимателей
Реализация надзорной функции органами Госсанэпиднадзора. Организация проверок юридических лиц и индивидуальных предпринимателей Понятие документа, классификация документов
Понятие документа, классификация документов Основы квалиметрии и квалиметрия в пищевых отраслях
Основы квалиметрии и квалиметрия в пищевых отраслях