Содержание
- 2. Определение валидации По определению PIC/S - это действия, которые в соответствии с принципами GMP доказывают, что
- 3. Цель валидации Доказать, что объект валидации действительно приводит к ожидаемым результатам
- 4. Процедура процесса валидации должна быть зафиксирована в ряде протоколов и результаты валидации должны быть зафиксированы в
- 5. План мероприятий по валидации - это документ, затрагивающий производственную деятельность всего предприятия и уточняющий сроки валидации
- 6. В плане мероприятий по валидации должны быть : представлен формат составления того или иного документа по
- 7. Валидация аналитических методик Валидация аналитической методики – это процесс, посредством которого, путем лабораторных испытаний устанавливают, что
- 8. Валидация аналитической методики Валидация является документированной процедурой, дающей высокую степень уверенности в том, что конкретный процесс,
- 9. Цель аналитической валидации - гарантия, что выбранная аналитическая методика будет давать воспроизводимые и достоверные результаты, соответствующие
- 10. Валидации подвергаются аналитические методы, применяемые для: 1. Идентификации лекарственного вещества. 2. Установления пределов содержания примесей родственных
- 11. Параметры валидации аналитического метода Правильность Прецизионность Специфичность Предел обнаружения или чувствительность Предел количественного определения Линейность Аналитическая
- 12. Правильность (accuracy, trueness) аналитического метода характеризует близость результатов испытаний, полученных данным методом, к истинному значению. Показателем
- 13. Прецизионность (precision) аналитической методики выражает близость результатов (степень разброса) серий измерений, полученных на множестве проб одного
- 14. Повторяемость – мера прецизионности при одинаковых условиях эксплуатации в течение короткого промежутка времени, то есть при
- 15. Промежуточная прецизионность – вариабельность внутри одной лаборатории. Стандартными определяемыми параметрами при этом являются вариабельности по дням,
- 16. Воспроизводимость – измеряет межлабораторную прецизионность. Этот параметр рассматривается при стандартизации аналитической методики (например, при включении методики
- 17. Специфичность аналитического метода способностью достоверно определять лекарственное вещество в присутствии примесных соединений, продуктов деградации и вспомогательных
- 18. Специфичность аналитического метода В испытаниях на подлинность аналитический метод должен обеспечивать идентификацию лекарственного вещества в присутствии
- 19. Специфичность аналитического метода При количественном определении примесей специфичность метода может быть доказана добавлением к лекарственному веществу
- 20. Предел обнаружения (ПО) минимальное количество аналита в пробе, которое может быть обнаружено, но не обязательно определено
- 21. Предел обнаружения (ПО) Существует несколько подходов для определения ПО: - при валидации инструментальных методик наличие фонового
- 22. Предел количественного определения (ПКО) минимальная концентрация, при которой аналит может быть достоверно количественно определен при соотношении
- 23. Линейность аналитической методики это способность (в рамках заданного диапазоне) получать результаты испытаний в виде переменных (например,
- 24. Существует два подхода для определения линейности методики: - при первом непосредственно берутся различные навески стандартного образца
- 25. Следует использовать результаты определений по крайней мере пяти концентраций. При нормальных условиях линейность считается приемлемой при
- 26. Диапазон аналитической методики интервал между максимальной и минимальной концентрацией анализируемого вещества в образце, для которого был
- 27. Робастность (устойчивость) аналитической методики способность методики оставаться неизменной при небольших, но преднамеренных вариациях в параметрах методики;
- 28. Робастность (устойчивость) аналитической методики
- 29. Классификация методов, используемых для фармацевтической продукции Аналитические методы, используемые для контроля качества лекарственных средств, в общем
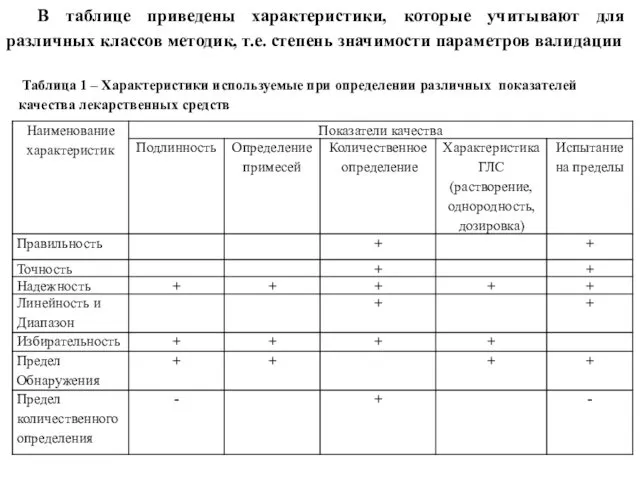
- 30. В таблице приведены характеристики, которые учитывают для различных классов методик, т.е. степень значимости параметров валидации Таблица
- 31. Так, например, при определении подлинности важны способность методики определять минимальное количество вещества и не реагировать на
- 32. Указанные общие правила могут иметь исключения, когда характеристики, отмеченные в таблице как не требуемые, могут быть
- 33. Виды валидации Валидация делится на следующие виды: - перспективная; - сопутствующая; - ретроспективная; - ревалидация.
- 34. Перспективная валидация проводится ЦЗЛ и ОКК на этапе подготовки проекта ФСП на новые ЛС или при
- 35. Сопутствующая валидация проводится в ЦЗЛ и ОКК на этапе подготовки проекта ФСП взамен существующей ФС (ВФС),
- 36. Ретроспективная валидация проводится в ОКК с использованием метода карт контроля качества. Данный тип валидации АМ используется
- 37. Ревалидация АМ (повторная валидация) осуществляется в ряде случаев, когда происходят изменения в синтезе лекарственного вещества, в
- 38. Ревалидация АМ (повторная валидация) Ревалидация проводится в случае следующих изменений: а) поставщиков исходного сырья (изменение физических
- 39. Ревалидация АМ (повторная валидация) Ревалидация должна производиться также: - при появлении отклонений, выявленных при серийном выпуске
- 40. Валидация производственных систем и оборудования В последнее время стандартной практикой стало включение процедуры «квалификация» в рамках
- 41. Требования, предъявляемые к системам и оборудованию - системы и оборудования подходят для намеченного использования в соответствии
- 42. До начала работ по валидации процесса необходимо завершить квалификацию критического оборудования и систем. Квалификацию обычно проводят
- 43. Квалификация проекта (Design Qualification - DQ) Этап включает в себя: - выбор поставщика, исходят из следующих
- 44. Квалификация монтажа (Инсталяционная квалификация – IQ) относится у установке оборудования и определяет, что полученное оборудование соответствует
- 45. Квалификация функционирования (Операционная квалификация – OQ) процесс, показывающий, что оборудование будет функционировать согласно рабочим/операционным требованиям к
- 46. Квалификация эксплуатации (Эксплуатационная квалификация – PQ) процесс, показывающий, что оборудование постоянно эксплуатируется в соответствии со спецификацией
- 47. В дальнейшем, при эксплуатации, проверка работоспособности выполняется по инструкции изготовителя с определенной периодичностью. Возможны разные варианты,
- 48. Обработка и оформление результатов валидации 1. На фармацевтическом предприятии должен быть определен сотрудник, ответственный за проведение
- 49. Обработка и оформление результатов валидации 3. Персонал, привлекаемый к работе по проведению валидации, должен пройти соответствующее
- 50. Обработка и оформление результатов валидации На основании полученных результатов руководитель рабочей группы составляет отчет о проведении
- 52. Скачать презентацию
















































 Муниципальная программа Формирование современной городской среды на территории Владивостокского городского округа
Муниципальная программа Формирование современной городской среды на территории Владивостокского городского округа Организационное обеспечение безопасности информации ограниченного доступа в РФ
Организационное обеспечение безопасности информации ограниченного доступа в РФ ФЗ №273 Об образовании в РФ. Стипендии
ФЗ №273 Об образовании в РФ. Стипендии Символы России
Символы России Гражданин Российской Федерации
Гражданин Российской Федерации Презентация к уроку Избирательный процесс Диск
Презентация к уроку Избирательный процесс Диск Определение поставщика, подрядчика, исполнителя, путем проведения запроса котировок
Определение поставщика, подрядчика, исполнителя, путем проведения запроса котировок Криминалистические версии и планирование расследования
Криминалистические версии и планирование расследования Европейская конвенция по правам человека. . Структура Статьи Конвенции
Европейская конвенция по правам человека. . Структура Статьи Конвенции Понятие, предмет принципы и источники гражданского права
Понятие, предмет принципы и источники гражданского права Понятие, содержание и значение охраны труда
Понятие, содержание и значение охраны труда Понятие и признаки несостоятельности (банкротства)
Понятие и признаки несостоятельности (банкротства) Понятие. Задачи. Источники. Система. Принципы уголовного права
Понятие. Задачи. Источники. Система. Принципы уголовного права Роль некоммерческих организаций в экономике России
Роль некоммерческих организаций в экономике России Екологічні права та обов’язки громадян
Екологічні права та обов’язки громадян Электронный сервис Росреестра Личный кабинет правообладателя
Электронный сервис Росреестра Личный кабинет правообладателя Страхование. Виды страхования
Страхование. Виды страхования Государственный портовый контроль
Государственный портовый контроль Материальная ответственность работодателя
Материальная ответственность работодателя Особенности трудоустройства иностранных граждан в России
Особенности трудоустройства иностранных граждан в России Гражданин Российской Федерации
Гражданин Российской Федерации Удержание: основания
Удержание: основания Специальные счета для участников закупок
Специальные счета для участников закупок Изменения в трудовом законодательстве 2022
Изменения в трудовом законодательстве 2022 Государственная кадастровая оценка (ФРТ-1-ЗиК 1-1м (заочно))
Государственная кадастровая оценка (ФРТ-1-ЗиК 1-1м (заочно)) Изменения трудового законодательства. Федеральный закон от 03.07.16 № 272-ФЗ
Изменения трудового законодательства. Федеральный закон от 03.07.16 № 272-ФЗ Реквизиты и бланки документов. Правила оформления реквизитов
Реквизиты и бланки документов. Правила оформления реквизитов Мемлекеттік қызметті реформалаудың сыбайлас жемқорлыққа қарсы аспектісі
Мемлекеттік қызметті реформалаудың сыбайлас жемқорлыққа қарсы аспектісі