Содержание
- 2. Белки – линейные биополимеры нерегулярной структуры, состоящие из аминокислот, соединенных пептидной связью. Насыщены азотом (16 –
- 3. Функции белков (найдите соответствие ) Пластическая Каталитическая Регуляторная Рецепторная Защитная Транспортная Механическая (опорная) Сократительная Депонирующая Энергетическая
- 4. Классификация белков По химическому строению (простые и сложные) По форме молекул (фибриллярные и глобулярные) По функциональному
- 5. Аминокислоты – азбука белка Все физико – химические свойства белков определяются их аминокислотным составом. Аминокислоты –
- 6. Классификация аминокислот По радикалу (алкильные, ароматические, имино-, амиды, серусодержащие, оксикислоты, дикарбоновые, диаминомонокарбоновые) По полярности (неполярные, полярные
- 7. Физико-химические свойства аминокислот М. масса - в среднем 100 Да Оптически активны (имеют ассиметричный атом С,
- 8. Краткое обозначение аминокислот Трехбуквенное обозначение: Гли (Gly), Ала (Ala). Однобуквенные символы: Цистеин (C), аспартат (D),метионин (M),
- 9. История открытия белков 17 -18 вв. –выделение из различных растительных и животных источников вязких, клейких, свертывающихся
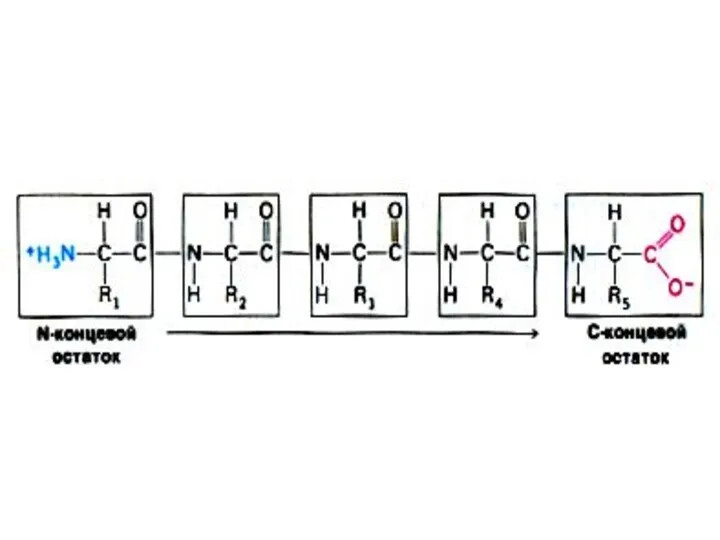
- 10. Уровни организации белковых молекул Структура белковой молекулы в первую очередь определяется последовательностью аминокислот в полипептидной цепи.
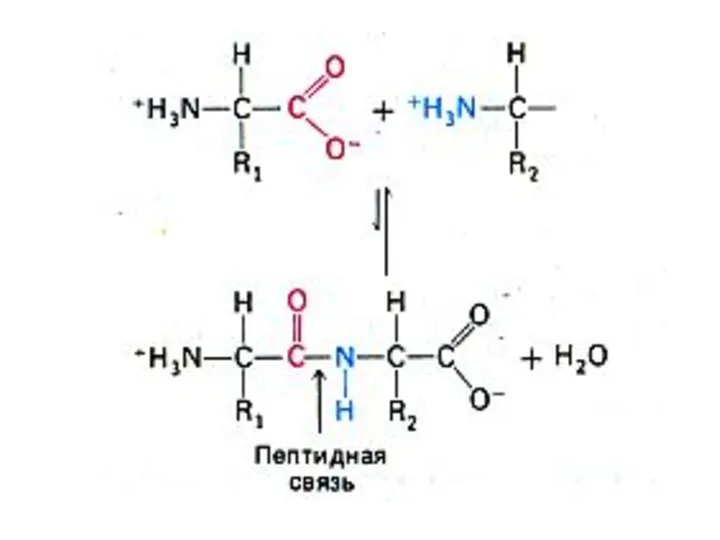
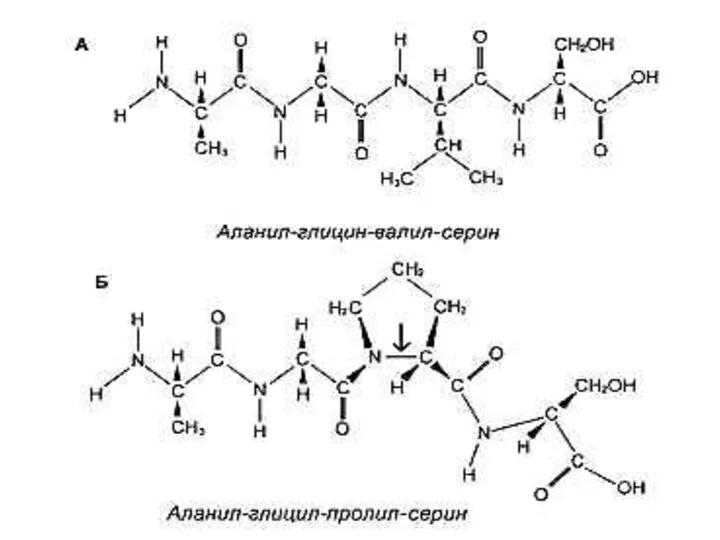
- 11. Первичная структура белка Основная связь – пептидная, прочная, ковалентная, образующая жесткий остов молекулы. Свойства пептидной связи:
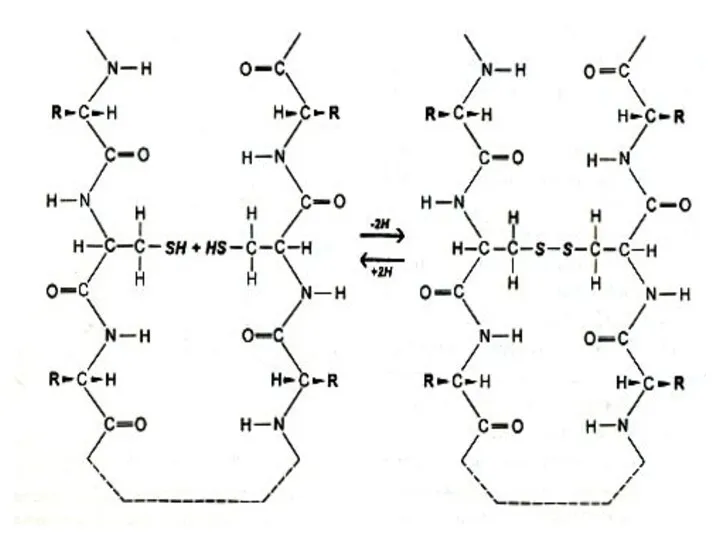
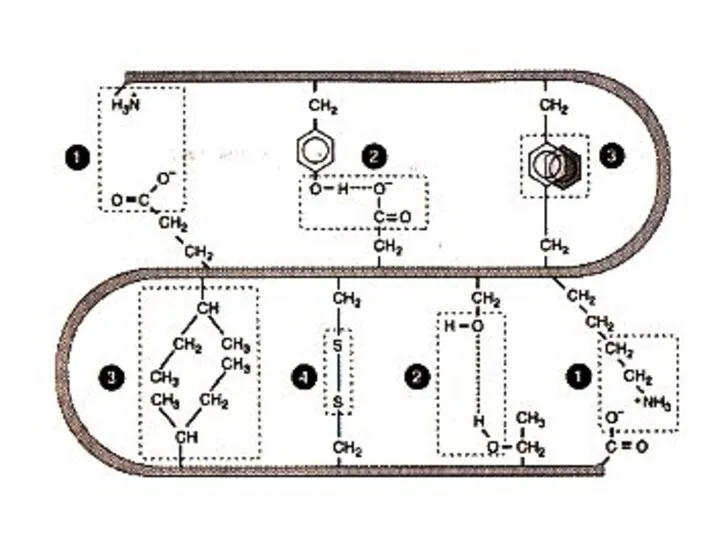
- 16. Первичная структура белка Дисульфидные связи (S – S) Образуется при спонтанном окислении SH –групп близкорасположенных остатков
- 17. Первичная структура белка Первичная последовательность аминокислот, кодируемая нуклеотидами ДНК, определяет дальнейшую укладку полипептида в пространстве. Зная
- 18. L. Pouling, P.Cory (1930-е годы) Рентгеноструктурный анализ кристаллов пептидов, определение длин и углов связей. Предсказали, а
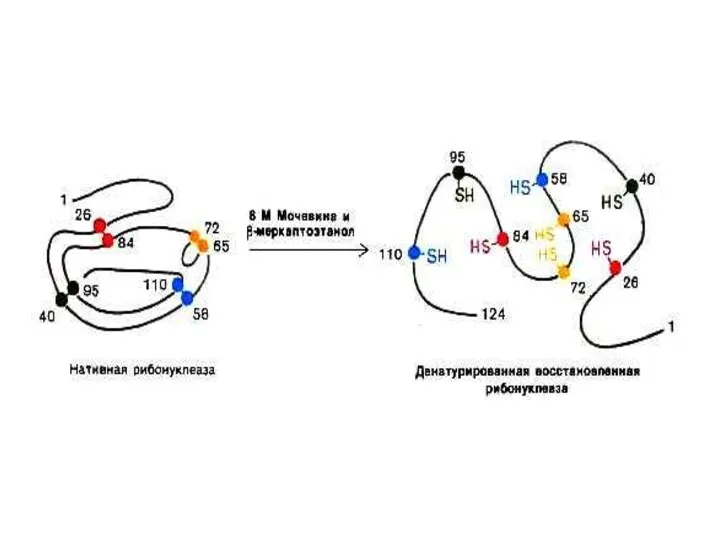
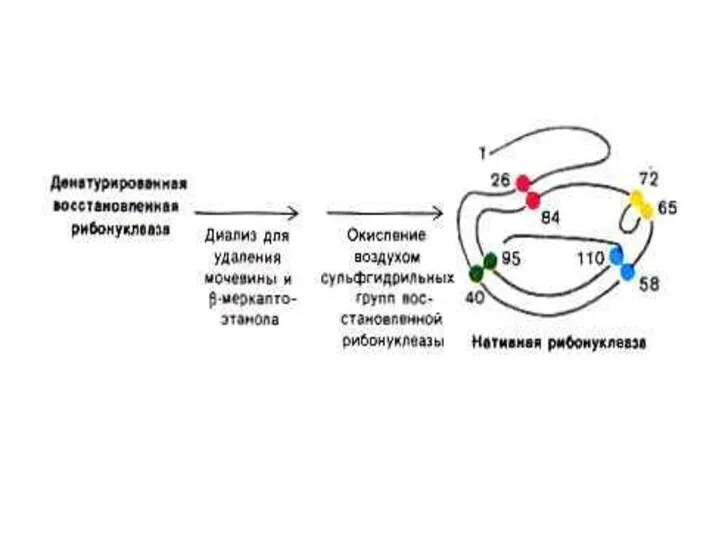
- 19. Опыты Anfinsen C.B.(1964 г.) демонстрируют связь первичной структуры белка, конформации и функциональной активности Денатурированная, раскрученная спираль
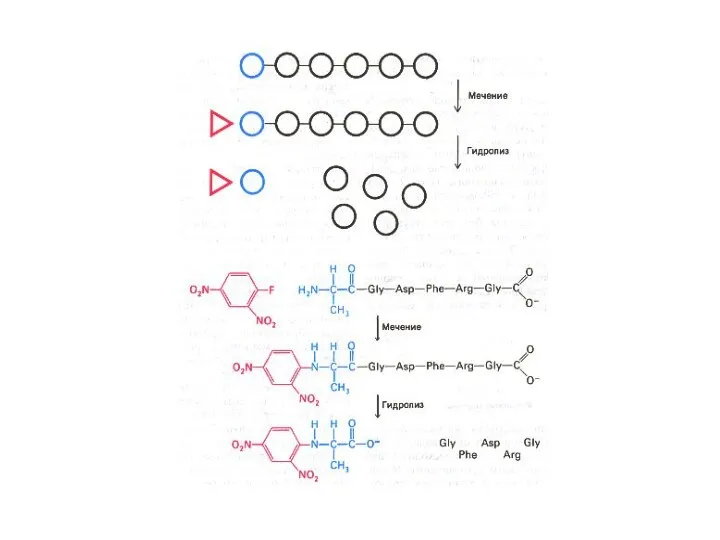
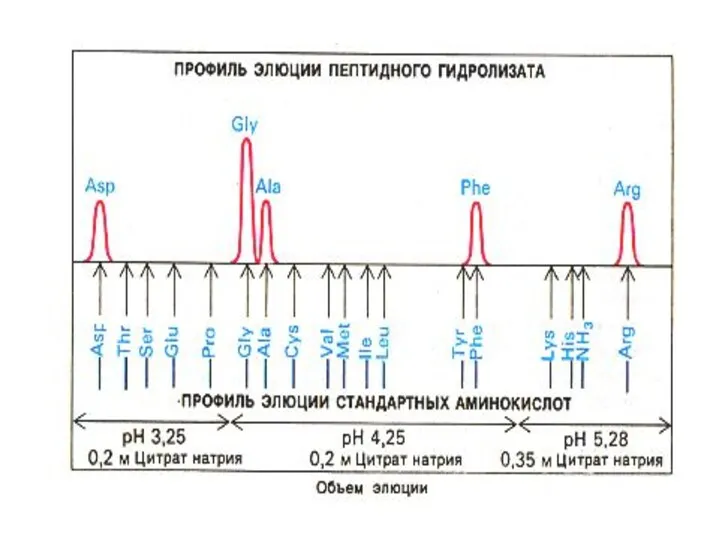
- 22. Этапы экспериментальной расшифровки первичной структуры белка Получить чистую фракцию белка Определить, сколько C- или N- концов,
- 23. Этапы экспериментальной расшифровки первичной структуры белка Специфический химический гидролиз пептидных связей (после реакции с бромцианом С
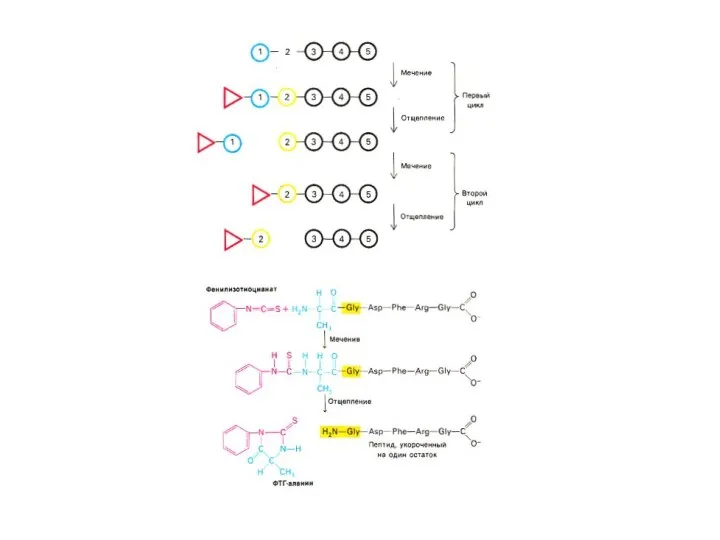
- 25. Этапы экспериментальной расшифровки первичной структуры белка Специфические реакции с N – или C-концевыми аминокислотами (реакции Сэнджера,
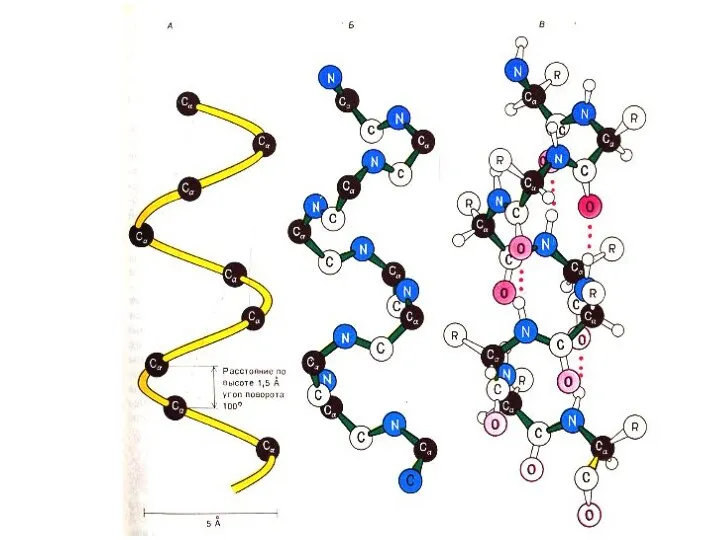
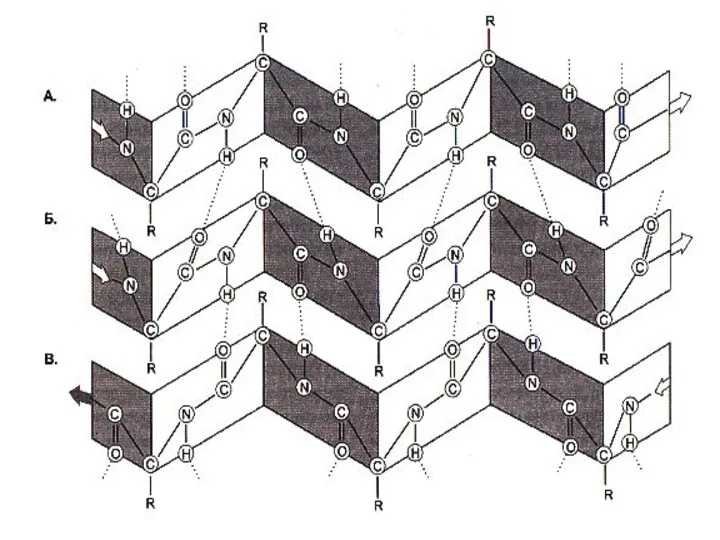
- 29. Вторичная структура белка Регулярная, периодическая структура создается вращением радикалов аминокислот вокруг α – С атома. Белки
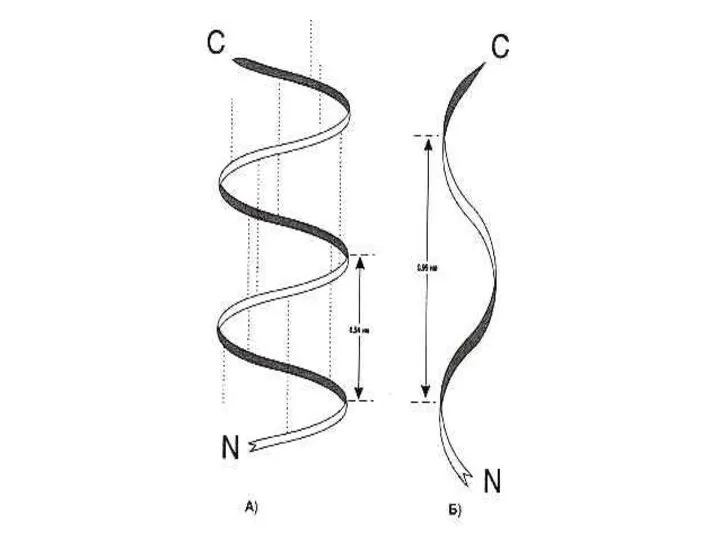
- 30. Вторичная структура белка α- спираль, право – (чаще для L- аминокислот) или левозакрученная, полный виток спирали
- 32. Вторичная структура белка Степень спирализации в полипептидах м.б. от 0 до 80 – 90%. Чем больше
- 33. Вторичная структура белка В различных белках есть разные структурные мотивы (единицы скручивания): αα − αβ −
- 36. Вторичная структура белка Коллагеновая суперспираль – фибриллярный, нерастворимый белок соединительной ткани. Субъединицей является тропоколлаген – три
- 37. Вторичная структура белка Коллаген –сложный белок (гликопротеин), остатки глюкозы или галактозы ковалентно соединены с ОН- группами
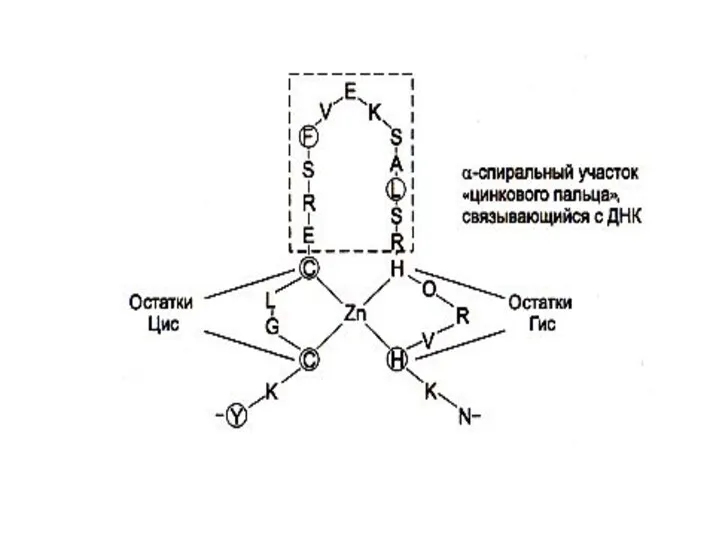
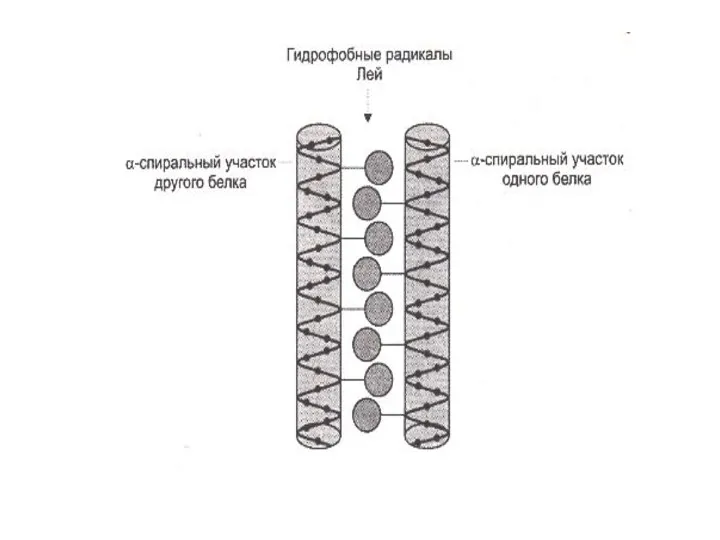
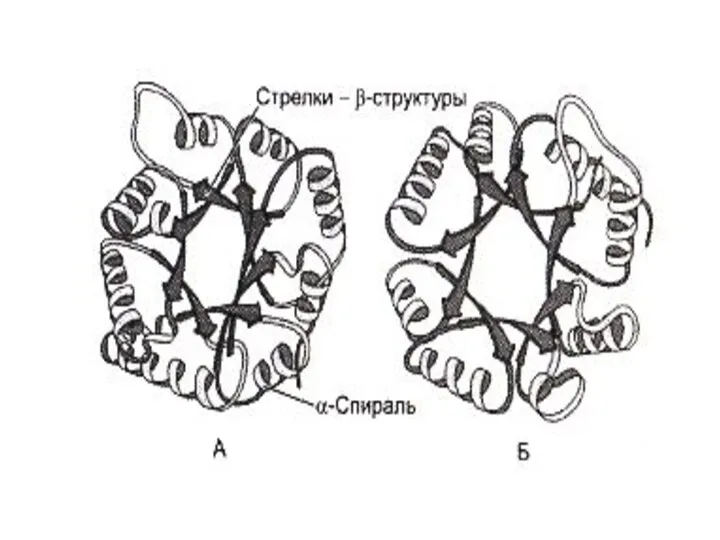
- 39. Супервторичные структуры Лейциновые застежки Цинковые пальцы В - бочонки
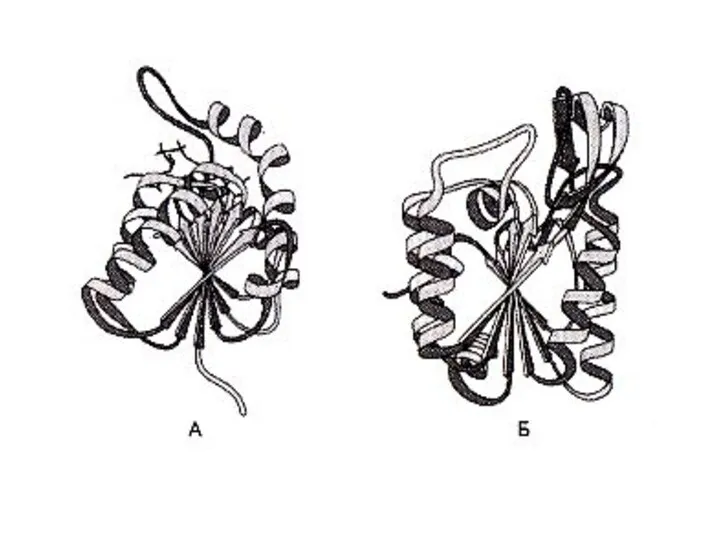
- 43. Третичная структура белка Дж. Кендрью (1956г., Кембридж) –рентгеноструктурный анализ миоглобина кашалота. Третичная структура отличается от вторичной
- 45. Третичная структура белков Именно на уровне третичной структуры большинство белков становятся функционально активными. Процесс укладки полипептида
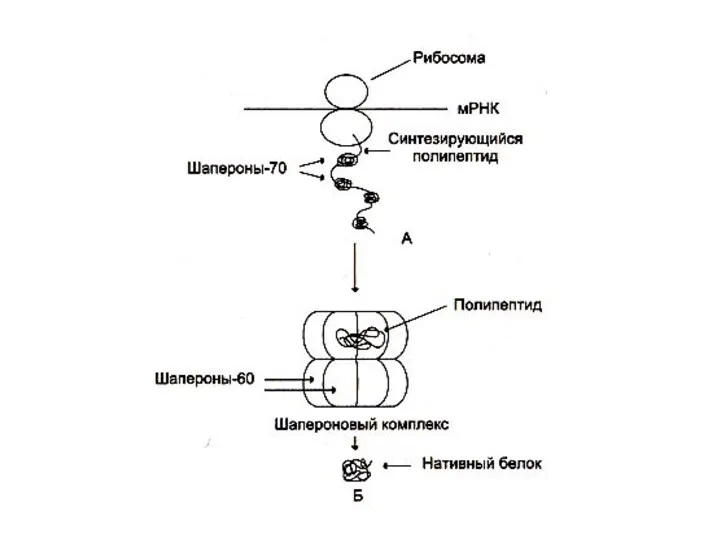
- 46. ФОЛДИНГ Условия для «правильной» укладки белковой цепи в пространстве создаются ШАПЕРОНАМИ – белками-»няньками», окружающими вновь синтезируемый
- 47. Шапероны Шапероны –комплексы из нескольких белковых субъединиц, формирующих бочонок с внутренней полостью, где происходит «перебор» всех
- 49. Четвертичная структура белка Олигомерные (состоящие из 2 –х и более субъединиц-протомеров), соединенных слабыми, нековалентными связями. М.м.
- 50. Пространственная структура белка Генетически заданная, единственно энергетически выгодная и функционально активная Пространственная конформация лабильна, подвижна в
- 51. Заметки о белках Видовая специфичность белков. Филогенетически близкие организмы имеют сходные по строению белки. Белки, выполняющие
- 52. Физико-химические свойства белков. Методы белковой химии. Белковые молекулы очень гетерогенны по всем физико-химическим свойствам: молярной массе,
- 53. Свойства белковых растворов Белковые растворы обладают свойствами истинных растворов (гомогенны, устойчивы) и свойствами коллоидных систем (обусловленных
- 54. Свойства белковых растворов, как коллоидных систем 1. Опалесценция и способность рассеивать лучи видимого света (Эффект Тиндаля)
- 55. Растворимость белков определяется главным образом двумя факторами: Зарядом молекул Способностью образовывать мицеллы, окруженные гидратной оболочкой Необходимо
- 56. Какие факторы влияют на растворимость белка? Как осадить белок из раствора? 1. Изменение рН среды. При
- 57. Центрифугирование Осадить белок из раствора можно под действием центробежной силы. Каждая частица имеет свой коэффициент седиментации.
- 58. Определение молярной массы вещества с помощью ультрацентрифугирования R x T x S M = ---------------- D
- 59. Дифференциальное центрифугирование Применяется для разделения клеток, внутриклеточных структур с разной плавучей плотностью и соответственно, разным коэффициентом
- 60. Другие методы белковой химии Структуру молекулы можно определить по результатам рентгеноструктурного анализа (кристаллы); ядерно-магнитного резонанса (растворы
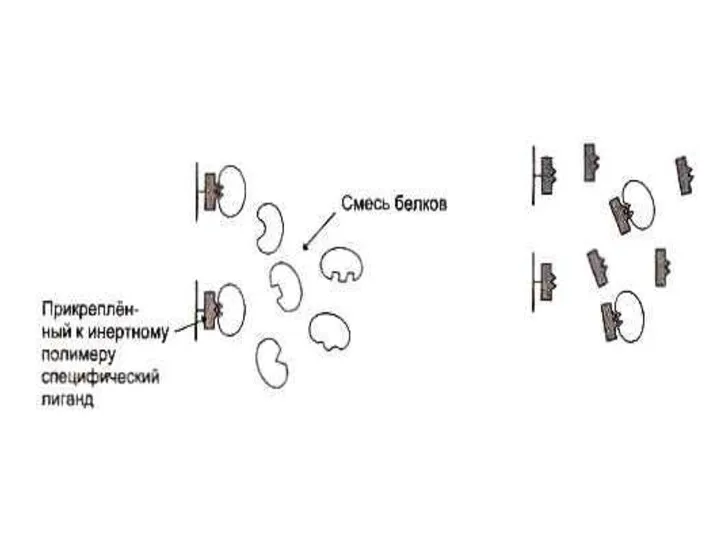
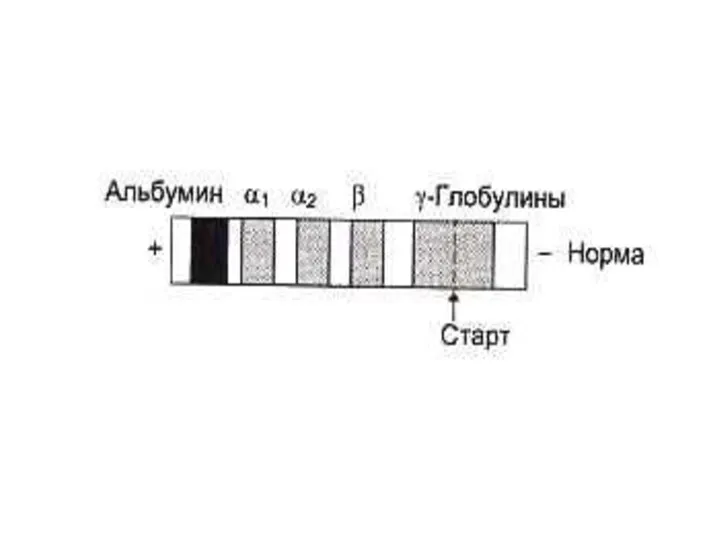
- 61. Способы разделения, идентификации и определения чистоты белковых фракций Электрофорез: Тизелиус, 1937г. Свободный э/ф по методу движущейся
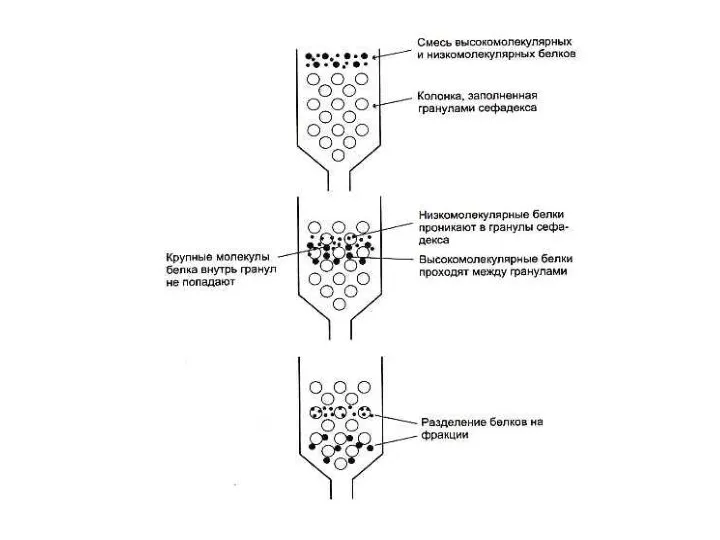
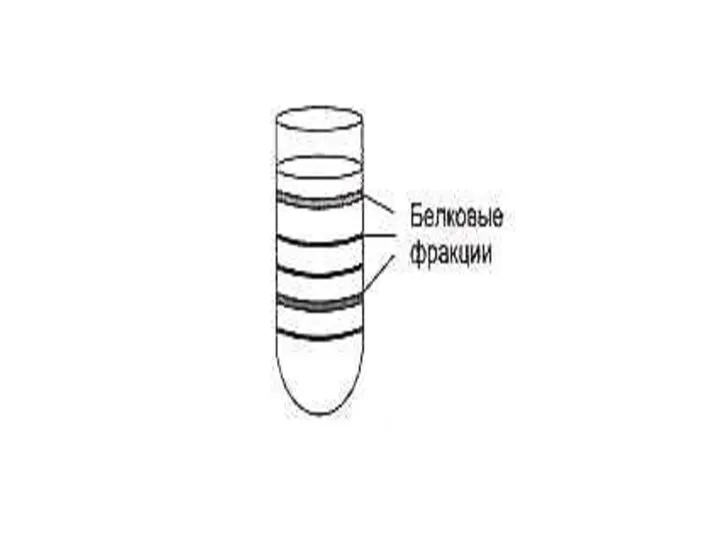
- 62. Способы разделения, идентификации и определения чистоты белковых фракций Хроматография: Ионо - обменная (по заряду) Распределительная (по
- 66. Все способы манипуляции с белками (выделение, разделение и т.д.) - это компромисс между возможностями физико-химических методов
- 68. Пептиды (условно до 5 тыс. Да) Образуются путем лимитированного протеолиза из крупных белков –предшественников или внерибосомальным
- 69. Пептиды Эндорфины, энкефалины Тафтсины Кейлоны Вазопрессин, окситоцин Ангиотензин Кинины Гастрин, секретин
- 70. Простые белки. Альбумин. Сывороточный белок (более половины всех белков плазмы), неспецифическая транспортная система плазмы, обеспечивает онкотическое
- 71. Сложные белки (имеют небелковые включения органической или неорганической природы. Типы связей между апо-частью и простетической группой
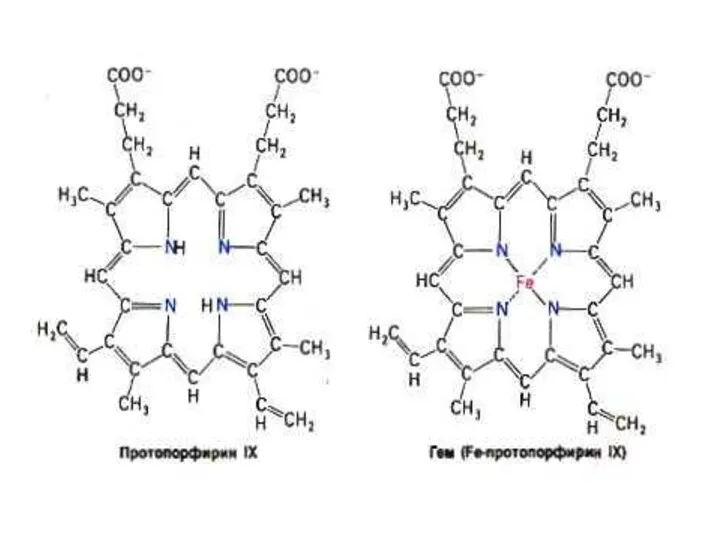
- 72. МИОГЛОБИН и ГЕМОГЛОБИН Результат эволюции механизмов переноса и депонирования кислорода. О2 может растворяться в плазме, связываться
- 74. Гем- содержащие белки Нb Миоглобин Цитохромы митохондрий и микросом Каталаза Пероксидаза Функция гема различна. Зависит от
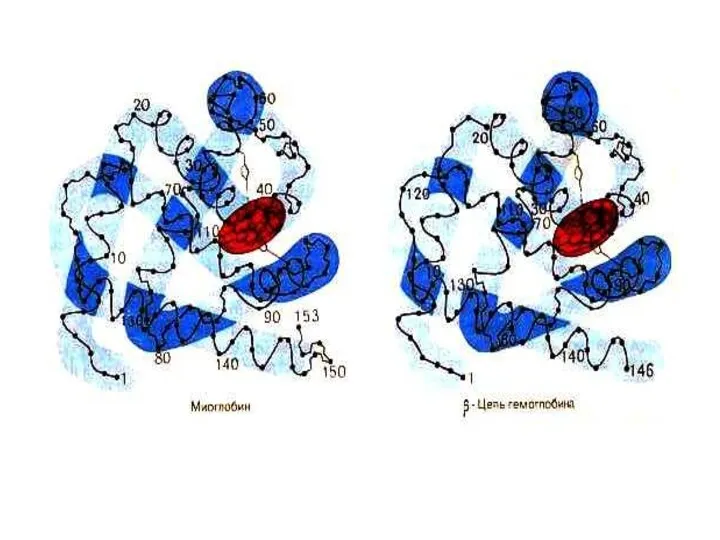
- 75. Миоглобин Гем +апобелок (1 полипептидная цепь, 150 аминокислот). М.м.=17,8 кДа, 75% α − спирализации. Плотная глобула
- 78. Гемоглобин 4 гема + 2 α− и 2 β− полипептидных цепи. М.м. 66 кДа. Белок четвертичной
- 80. Скачать презентацию





















































 Оси и плоскости в анатомии
Оси и плоскости в анатомии Отряд млекопитающие
Отряд млекопитающие Родина Пасльонові
Родина Пасльонові Гербициды. (Лекция 8)
Гербициды. (Лекция 8) Методы исследования биологии
Методы исследования биологии Углеводы. Классификация углеводов
Углеводы. Классификация углеводов Удаление продуктов обмена. Обмен веществ
Удаление продуктов обмена. Обмен веществ Необычный живой мир континента
Необычный живой мир континента Жиры (липиды)
Жиры (липиды) Поле чудес
Поле чудес Предмет и задачи зоопсихологии и сравнительной психологии
Предмет и задачи зоопсихологии и сравнительной психологии В тесном сотрудничестве: лингвистика - нейропсихология - нейролингвистика
В тесном сотрудничестве: лингвистика - нейропсихология - нейролингвистика Многообразие микробного мира
Многообразие микробного мира Методологическая роль лабораторных и практических работ по биологии в рамках ФГОС.
Методологическая роль лабораторных и практических работ по биологии в рамках ФГОС. Осенние явления в жизни растений
Осенние явления в жизни растений Митохондрии, пластиды, клеточный центр, органоиды движения, клеточные включения
Митохондрии, пластиды, клеточный центр, органоиды движения, клеточные включения Семейство крестоцветные растения
Семейство крестоцветные растения Биотехнологии. Значение биотехнологий
Биотехнологии. Значение биотехнологий Многоствольные формы
Многоствольные формы Рысь
Рысь Классификация и характеристика промысловых рыб
Классификация и характеристика промысловых рыб Состав и свойства помидоров
Состав и свойства помидоров Мониезиоз жвачных животных. Разработка мер борьбы и профилактики
Мониезиоз жвачных животных. Разработка мер борьбы и профилактики Ағзалардың көбею формалары
Ағзалардың көбею формалары Передвижение воды и минеральных веществ в растениях
Передвижение воды и минеральных веществ в растениях Общее строение клетки
Общее строение клетки Среды обитания живых организмов
Среды обитания живых организмов Зелёная аптека
Зелёная аптека