Содержание
- 2. Содержание лекции 1.Основные реакции обмена аминокислот -реакции по радикалу -реакции на карбоксильную группу -реакции на аминогруппу
- 5. Пути утилизации Аминокислот: 1.Биосинтез белка 2.Синтез олигопептидов (либеринов, статинов ) 3.Биогенных аминов 4.Мочевины 5.Креатина, креатинфосфата 6.Азотистые
- 6. Кроме индивидуальных путей обмена, известен ряд превращений, общий почти для всех аминокислот. Это реакции: 1.по радикалу
- 9. Трансаминирование аминокислот окислительное дезаминирование- прямое
- 10. Первая стадия яв-ся ферментативной с образованием промежуточного продукта- иминокислоты, которая спонтанно, без участия фермента, распадается на
- 11. ГЛУ+NAD+---?иминоглут кислота + НОН-? ---?α- кетоглутарат+NADH+H+ + NH3 Первая стадия катализируется ГДГ (анаэробный фермент). Вторая стадия
- 12. ГДГ- состоит из 6 субъединиц и проявляет свою активность только в мультимерной форме. При диссоциации ГДГ
- 13. Все остальные аминокислоты могут окисляться и дезаминироваться только непрямым путем ( т.е. через дополнительную стадию трансаминирования).
- 15. Это главный путь удаления азота у аминокислот. Выделены трансаминазы, катализирующие переаминирование большинства аминокислот. После поступления пищевых
- 16. Исключением являются аминокислоты с разветвленным углеводородным радикалом, для которых в печени нет соответствующих трансаминаз, о чем
- 17. Непрямое окислительное дезаминирование. Почти все природные а/к сначала реагируют с α-КГК в реакции трансаминирования с образованием
- 18. Любая а/к α- КГК NADH2 +NН3 Любая кето ГЛУ NADH+ + HOH кислота трансаминазы ГДГ
- 19. Поскольку обе эти реакции – и трансаминирование, и прямое дезаминирование- обратимы, то создаются условия для синтеза
- 20. Т.о. можно сказать, что путь синтеза заменимых а/к в организме- это непрямое окислительное дезаминирование, которое запущеное
- 23. Существует еще один механизм непрямого дезаминирования α- а/к, при которм ГЛУ, АСП, и АМФ выполняют роль
- 24. О2---? малат ЩУК фумарат АК ГЛУ АСП АМФ NH3 α- кетоглу ИМФ Н2О
- 25. ГДГ выполняет следующие функции: 1.Осуществляет связь обмена а/к с ЦТК через α-кетоГЛУ 2.Обеспечивает связывание аммиака 3.Обеспечивает
- 27. Трансаминирование-это главный путь удаления азота у аминокислот. Выделены трансаминазы, катализирующие переаминирование большинства аминокислот. После поступления пищевых
- 29. Исключением являются аминокислоты с разветвленным углеводородным радикалом, для которых в печени нет соответствующих трансаминаз, о чем
- 30. Клиническое значение определения активности трансаминаз Для клинических целей наибольшее значение имеют 2 трансаминазы- АсАТ и АлАТ
- 31. В сыворотке крови здоровых людей активность этих трансаминаз в среднем составляет-15-20 Е., по сравнению с десятками
- 32. Наибольшая активность АлАТ приходится на печень, а АсАТ на миокард. Поэтому определение активности АсАТ в сыворотке
- 33. Определение активностиАсАТ используется для ранней диагностики ИМ. Причем увеличение активности наблюдается через 24-36 час. И снижается
- 34. Токсичность аммиака и пути его обезвреживания 1.Аммиак в тканях протонирован ( NH4+), т.е он связывает Н+,
- 35. 3.Аммиак изменяет соотношение ионов натрия и калия т.к. близок к ним по физико- химическим свойствам: следовательно
- 36. Пути обезвреживания аммиака В плазме крови содержится 25-40 мМ/л аммиака. При накоплении последнего возникает тремор, нечленораздельная
- 37. 1.Восстановительное аминирование α-КГК + NH3+ NADFH2----------? Глутамат ЦТК ГДГ
- 39. 2.Образование амидов дикарбоновых кислот Т.к. ГЛН и АСН выделяются с мочой, то они являются транспортной формой
- 41. 3. Основная масса ГЛН и АСН захватывается почками, где под действием глутаминазы от них отщепляется аммиак..
- 42. Кроме того при ацидозе происходит потеря Na+ и K+ с мочой. Это приводит к снижению осмотического
- 43. 4. Амидирование свободных карбоксильных групп белков (амидированные формы белков устойчивы к протеазам)
- 44. Биосинтез мочевины Это основной механизм обезвреживания аммиака. 90% азота организма выводится в виде мочевины (М)., причем
- 45. Орнитиновый цикл синтеза мочевины (ОЦСМ) протекает в гепатоцитах,т.к. них наиболее высокая активность ферментов азотного обмена. Первая
- 46. Это еще один путь детоксикации аммиака- синтез пиримидиновых оснований. Первая и вторая р-ции ЦСМ протекают в
- 49. Мочевина- природный антиоксидант, радиопротектор,который взаимодействует с Fe+2, и останавливает перекисные процессы. Мочевина изменяет структуру воды, как
- 50. Энергетическая стоимость ЦСМ ЦСМ « стоит» 3 молекулы АТФ: 2 АТФ на стадии синтеза карбомоилфосфата и
- 51. 2- когда синтез-ся карбомоилфосфат ( АТФ—АДФ- 1 макроэр. связь) АТФ—АДФ- 1 макроэр. связь И 2 при
- 54. Биологическая роль ЦСМ Механизм детоксикации аммиака Механизм регуляции КЩС( т.к. поставляет СО2. ЦСМ поставляет орнитин Имея
- 56. Врожденные дефекты ЦСМ Врожденные дефекты ферментов с 1 по 5. Чем ближе ферментный блок к аммиаку,
- 60. Регуляция ЦСМ Краткосрочная: на уровень 1-го ферменты, который направляет азот ГЛУ( а значит и всех а/к)
- 62. Пути вступления аминокислот в ЦТК В процессе детоксикации амиака , образующиес углеродные скелеты могут использоваться в
- 63. Но в экстремальных ситуациях (диабет, голод, алкогольная интоксикация) роль аминокислот резко возрастает. На первых этапах главным
- 64. Дальше, после истощения запасов гликогена, происходит переключение метаболизма на утилизацию липидов (10-15 дней), с одновременным включением
- 65. После истощения запасов липидов наступает терминальная стадия- утилизация а/к--?увеличение аммиака в крови----? увеличению интоксикации----? кома-----? смерть.
- 68. Реакции декарбоксилирования аминокислот лежат в основе образования биогенных аминов. Продукты декарбоксилирования ароматических аминокислот и глутаминовой кислоты
- 69. и психических заболеваний оказывают влияние на метаболизм указанных соединений. Активная форма витамина В6 является коферментом декарбоксилаз,
- 73. Норадреналин - основной нейромедиатор симпатических постганглионарных окончаний. И норадреналин и его метилированное производное, адреналин накапливаются в
- 74. Обмен катехоламинов происходит при участии катехоламин-O-метилтрансферазы, (КOMT) и тираминазы, (MAO). Оба эти фермента широко распространены в
- 75. Нарушения метаболизма дофамина служат причиной болезни Паркинсона. Из триптофана через промежуточный 5-гидрокситриптофан образуется серотонин, соединение с
- 76. Из триптофана через промежуточный 5-гидрокситриптофан образуется серотонин, соединение с широким спектром действием
- 77. Синтез серотонина, мелатонина
- 78. Серотонин присутствует в самых высоких концентрациях в тромбоцитах и в желудочно-кишечном тракте. Меньшие количества найдены в
- 79. После высвобождения из серотонинергических нейронов, большая часть высвобождаемого серотонина возвращается активно секретируемыми клетками. Некоторые антидепрессанты ингибируют
- 80. Мелатонин образуется из серотонина в эпифизе и сетчатке, в которых находится N-ацетилтрансфераза. Парехиматозные клетки эпифиза секретирует
- 81. Синтез и секреция мелатонина увеличиваются в течение темнового периода дня и поддерживаются в низком уровне в
- 82. Эти суточные колебания синтеза мелатонина регулируются с участием норадреналина, секретируемого постганглионарными симпатическими нервами, иннервирующими эпифиз. Мелатонин
- 84. Гистамин образуется путем декарбоксилирования гистидина. Гистамин играет важную роль в о многих патологических процессах. Он образуется
- 85. Эту реакцию катализирует декарбоксилаза ароматических L-аминокислот. Этот фермент не обладает выраженной субстратной специфичностью и катализирует также
- 86. Декарбоксилаза in vitro и in vivo ингибируется а-метиламинокислотами, применяемыми в клинике в качестве гипотензивных средств. В
- 87. На первом этапе амин окисляется с передачей водородов на ФАД и образованием аммиака и соответствующего альдегида,
- 89. Ингибиторы МАО находят применение при лечении гипертонической болезни, депрессивных состояний и т.д.
- 90. Подобно другим биогенным аминам, гистамин разрушается путем окислительного дезаминирования при помощи моноаминоксидаз- флавинзависимых ферментов, локализованных преимущественно
- 91. В головном мозге концентрация аминокислот почти в 8 раз выше, чем в плазме крови, и существенно
- 92. В тканях мозга интенсивно протекают метаболические превращения аминокислот, такие, как окислительное дезаминирование, трансаминирование, модификация боковой цепи
- 93. g аминомасляная кислота образуется путем декарбоксилирования L-глутамата. Эта реакция катализируется пиридоксальфосфат-зависимым ферментом L-глутамат-декарбоксилазой.
- 94. Она локализована главным образом в нейронах центральной нервной системы, преимущественно в сером веществе головного мозга.
- 95. В особенности важной для нормального функционирования головного мозга является реакция декарбоксилирования, в результате которой образуется γ-аминомасляная
- 96. Биосинтез и деградацию глутамата можно рассматривать, как побочный путь цитратного цикла (ГАМК-шунт), который в отличие от
- 98. ГАМК-шунт характерен для клеток центральной нервной системы, но не играет существенной роли в других тканях.
- 99. Декарбоксилирование L- глутамата - это основной путь биосинтеза g-аминомасляной кислоты. Возможно также ее образованием из путресцина
- 100. Катаболизм g-аминобутирата начинается с потери аминогруппы и образования янтарного полуальдегида. Последний может быть восстановлен в g-гидроксибутират
- 101. ГАМК оказывает тормозящий эффект на деятельность ЦНС. Ее препараты используют при лечении заболеваний , сопровождающихся возбуждением
- 102. Глутамат, ГАМК, выполняют в нейронах функцию медиаторов. Они хранятся в синапсах и выделяются при поступлении нервного
- 103. Эти аминокислоты образуются в реакции трансаминирования из промежуточных метаболитов цитратного цикла, 2-оксоглутарата и оксалоацетата
- 104. Многие моноамины и катехоламины инактивируются аминоксидазой (моноаминоксидазой, "МАО") путем дезаминирования с одновременным окислением в альдегиды. Следовательно,
- 106. Скачать презентацию
 Отряд Чешуйчатые. Подотряд Ящерицы
Отряд Чешуйчатые. Подотряд Ящерицы Белки, их свойства
Белки, их свойства Основы газоноводства. (Лекция 13)
Основы газоноводства. (Лекция 13) Слои кожи
Слои кожи Биология развития
Биология развития Где больше витамина С
Где больше витамина С Цианобактерии. Отличия от бактерий
Цианобактерии. Отличия от бактерий Простейшие
Простейшие Изменчивость
Изменчивость Остеология. Анатомия человека
Остеология. Анатомия человека Дәрумендер және олардың пайдасы
Дәрумендер және олардың пайдасы Семейство Розоцветные
Семейство Розоцветные Rare images from Wildlife Photography
Rare images from Wildlife Photography Клеточный уровень организации живого
Клеточный уровень организации живого Отряд китообразные
Отряд китообразные Органы чувств
Органы чувств Презентация к уроку по биологии по теме: Эволюция органического мира. Антропогенез. 11-й класс. Тема урока: Митохондриальная Ева и генетическое разнообразие современного человечества
Презентация к уроку по биологии по теме: Эволюция органического мира. Антропогенез. 11-й класс. Тема урока: Митохондриальная Ева и генетическое разнообразие современного человечества Проектирование условий и механизмов гражданского становления личности в контексте перехода на Федеральные государственные образовательные стандарты
Проектирование условий и механизмов гражданского становления личности в контексте перехода на Федеральные государственные образовательные стандарты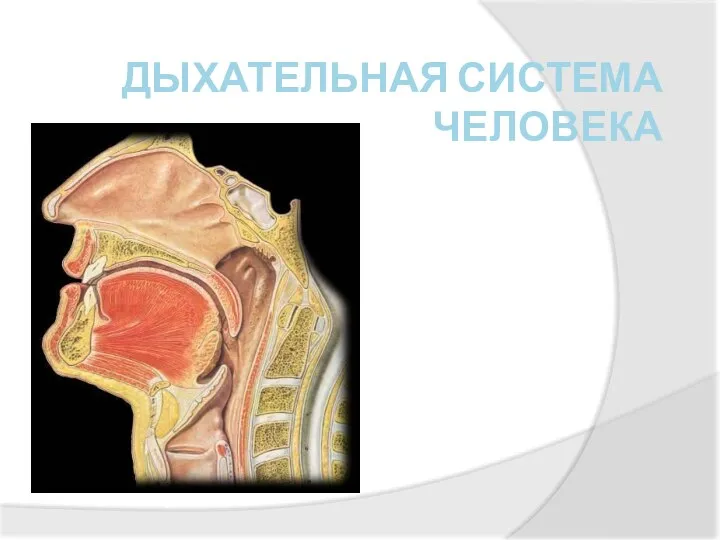 Строение органов дыхания человека
Строение органов дыхания человека Виртуальная экскурсия в природную экосистему Пионерского озера и прибрежных территорий часть2
Виртуальная экскурсия в природную экосистему Пионерского озера и прибрежных территорий часть2 Основные положения клеточной теории
Основные положения клеточной теории Класс Птицы. Многообразие, среда обитания. Биологические ососбенности
Класс Птицы. Многообразие, среда обитания. Биологические ососбенности Обмен аминокислот и белков
Обмен аминокислот и белков Разноцветные жуки. 1 класс
Разноцветные жуки. 1 класс Принципы анатомического строения и функционирования анализаторов. Антиноцицептивная система. Стресс, его механизмы
Принципы анатомического строения и функционирования анализаторов. Антиноцицептивная система. Стресс, его механизмы Вегетативное размножение растений
Вегетативное размножение растений Ведущие принципы для объяснения причин развития
Ведущие принципы для объяснения причин развития Наследственная изменчивость
Наследственная изменчивость