Содержание
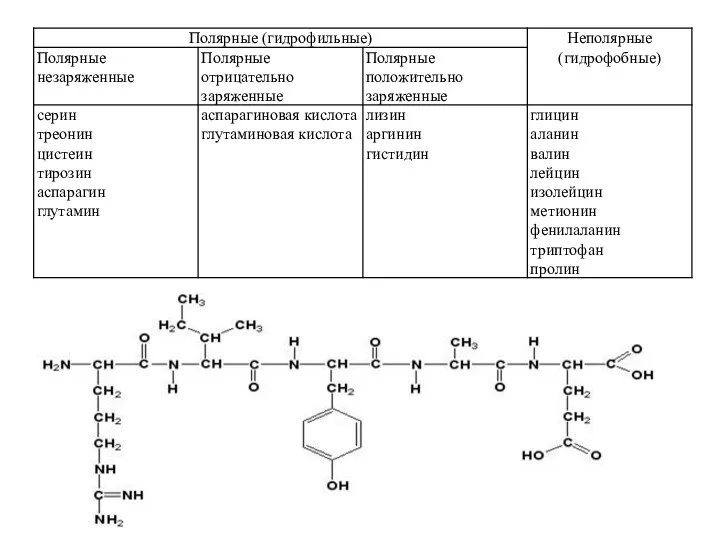
- 2. Белки – высокомолекулярные биологически активные азотсодержащие соединения, структурными компонентами которых являются аминокислоты. Функции белков: 1. Каталитическая
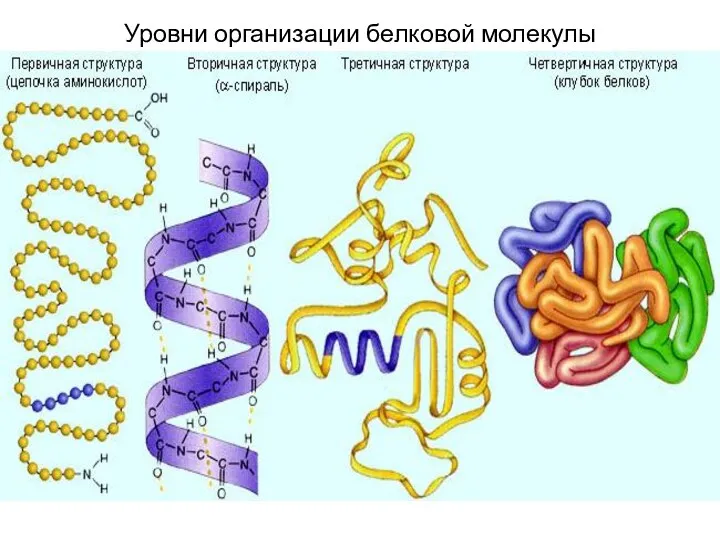
- 4. Уровни организации белковой молекулы
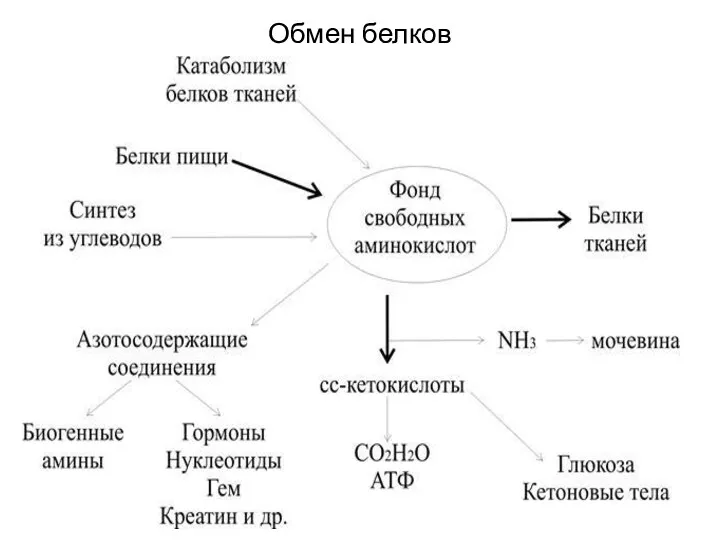
- 5. Обмен белков
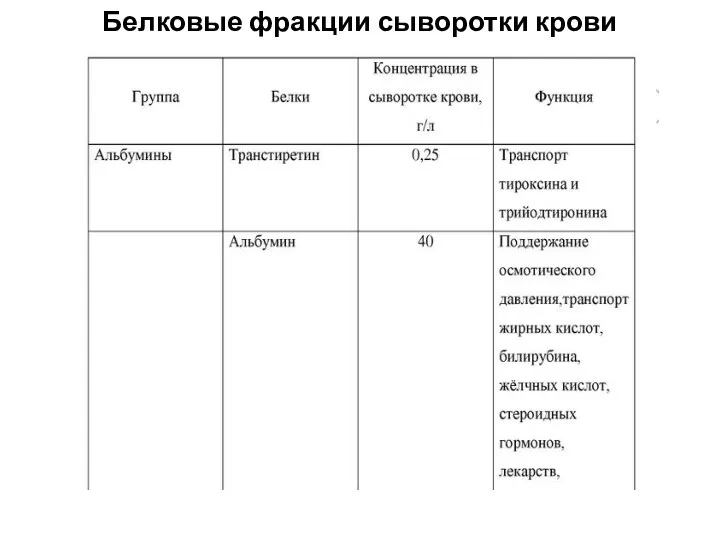
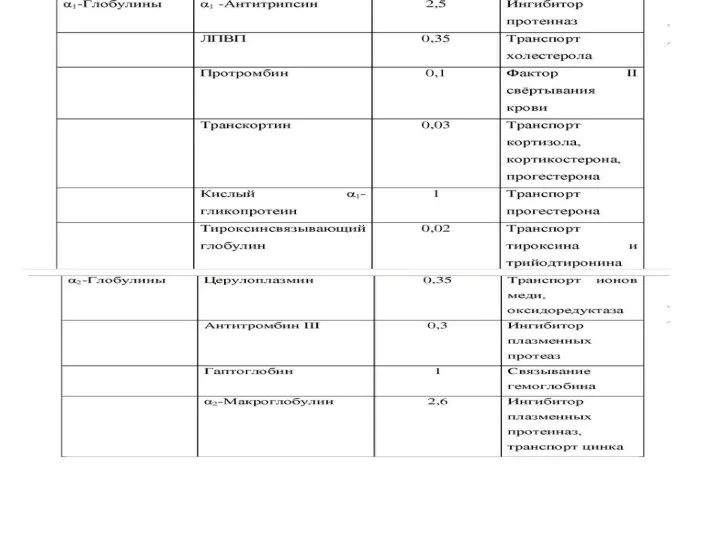
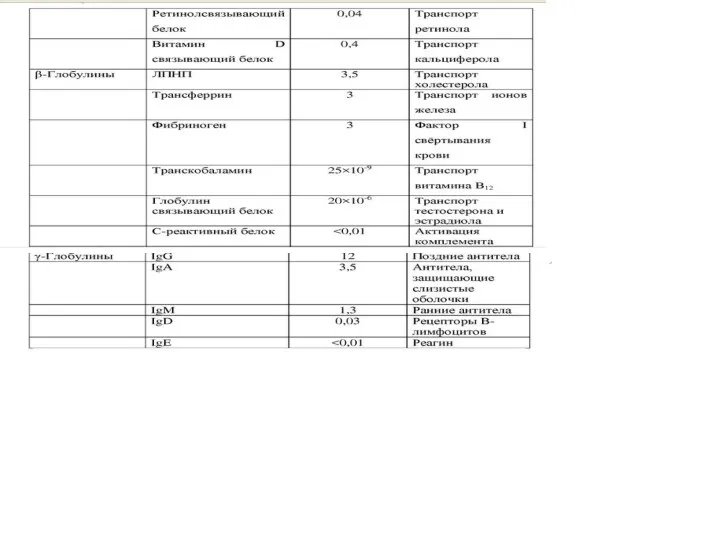
- 6. Белковые фракции сыворотки крови
- 9. Исследование общего белка Материал – сыворотка крови без гемолиза и примеси фибриногена (до исследования можно хранить
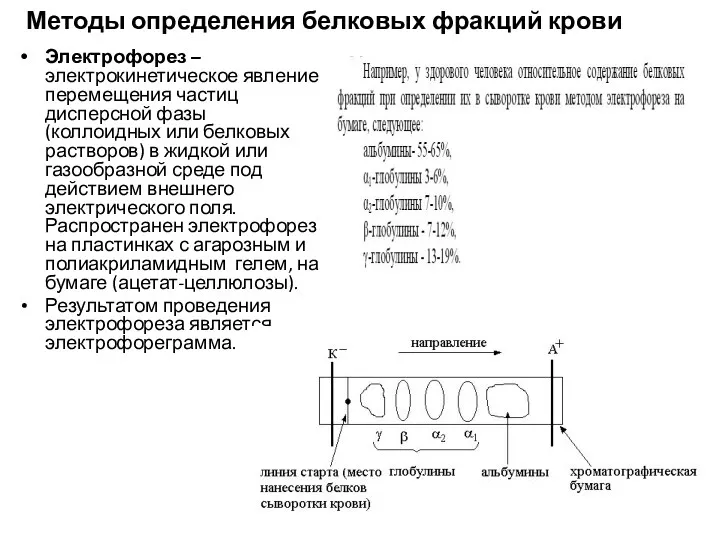
- 10. Методы определения белковых фракций крови Электрофорез – электрокинетическое явление перемещения частиц дисперсной фазы (коллоидных или белковых
- 11. Пример электрофореграмы
- 12. Определение специфических белков. Турбидиметрия - Принцип метода основан на измерении интенсивности света определённой длины волны, прошедшего
- 13. Определение специфических белков ИММУНОКОЛОРИМЕТРИЯ Принцип метода Определение белка иммуноколориметрическим методом основано на его взаимодействии с IgG,
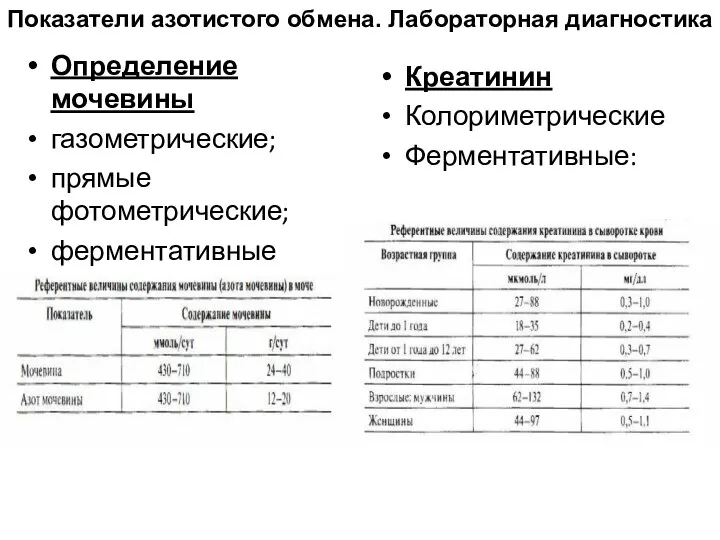
- 14. Определение мочевины газометрические; прямые фотометрические; ферментативные Креатинин Колориметрические Ферментативные: Показатели азотистого обмена. Лабораторная диагностика
- 15. Мочевая кислота Колориметрические — все эти методы недостаточно специфичны и основаны на: способности мочевой кислоты восстанавливать
- 17. Скачать презентацию






 Квітка. Будова та різноманітність квіток
Квітка. Будова та різноманітність квіток Рынок биотехнологий и государственные программы развития биотехнологий в РФ
Рынок биотехнологий и государственные программы развития биотехнологий в РФ Мир комнатных растений. Окружающий мир 2 класс
Мир комнатных растений. Окружающий мир 2 класс Кости нижней конечности
Кости нижней конечности Введение в клеточную биологию. Свойства живого. Клеточная теория
Введение в клеточную биологию. Свойства живого. Клеточная теория Макроэволюция: направления и пути эволюции
Макроэволюция: направления и пути эволюции Вода как фактор роста и развития растений
Вода как фактор роста и развития растений Огляд відділів хромофітових водоростей (Stramenopiles)
Огляд відділів хромофітових водоростей (Stramenopiles) Клеточное строение живых организмов
Клеточное строение живых организмов Майстерність маскування
Майстерність маскування Комнатные растения. Агапантус
Комнатные растения. Агапантус Клас Ракоподібні
Клас Ракоподібні Презентация Пресмыкающиеся
Презентация Пресмыкающиеся Строение головного мозга
Строение головного мозга Витамин В1 – тиамин
Витамин В1 – тиамин Anthocerotopsida (Отдел Антоцеротовые)
Anthocerotopsida (Отдел Антоцеротовые) Обмен углеводов
Обмен углеводов Вымирающие виды животных
Вымирающие виды животных Сүйектің байланысу түрлері
Сүйектің байланысу түрлері Форма костей скелета человека и виды их соединения
Форма костей скелета человека и виды их соединения Лекция. Систематика растений
Лекция. Систематика растений Мочевыделительная система человека
Мочевыделительная система человека Интерактивная игра Кто? Как? Почему? Играя, вспоминаем для 7 класса (по материалу I полугодия)
Интерактивная игра Кто? Как? Почему? Играя, вспоминаем для 7 класса (по материалу I полугодия) Хромосомная теория наследственности. Законы сцепления признаков
Хромосомная теория наследственности. Законы сцепления признаков Синичкин день
Синичкин день Методы оценки белковой экспрессии. ИФАанализ, Вестерн блоттинг, иммуноприципитация, иммуногистохимия
Методы оценки белковой экспрессии. ИФАанализ, Вестерн блоттинг, иммуноприципитация, иммуногистохимия Жүйке жүйесі
Жүйке жүйесі Тип: моллюски. Класс: брюхоногие. Виноградная улитка
Тип: моллюски. Класс: брюхоногие. Виноградная улитка