Содержание
- 2. Кафедра биохимии, 2006 (C) Пептиды и белки: общие сведения Белки При соединении аминокислот в цепочку образуется
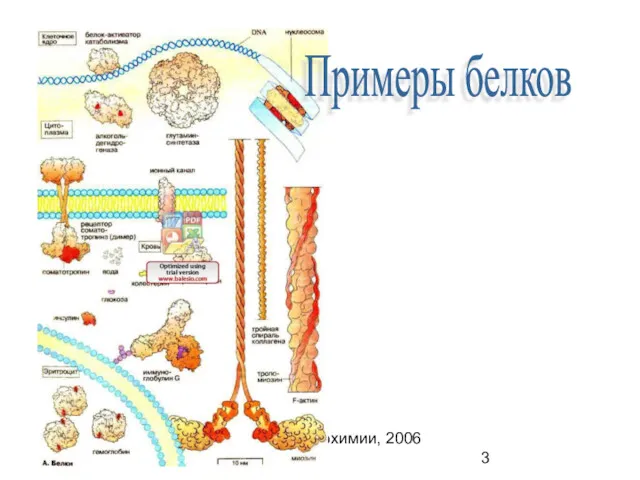
- 3. Кафедра биохимии, 2006 (C) Примеры белков
- 4. Кафедра биохимии, 2006 (C) Структурообразующие функции Структурные белки отвечают за поддержание формы и стабильности клеток и
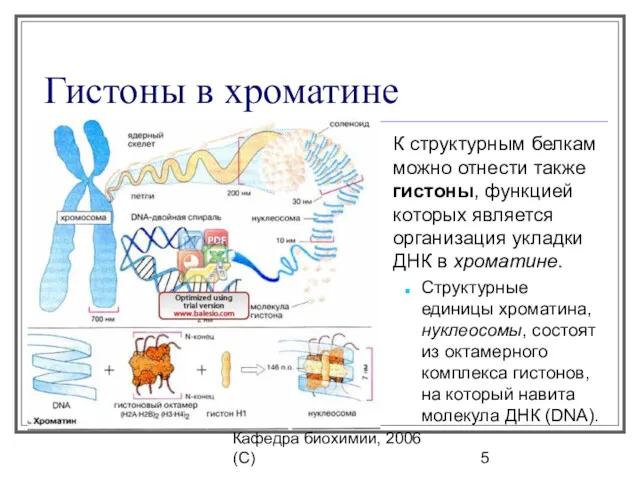
- 5. Кафедра биохимии, 2006 (C) Гистоны в хроматине К структурным белкам можно отнести также гистоны, функцией которых
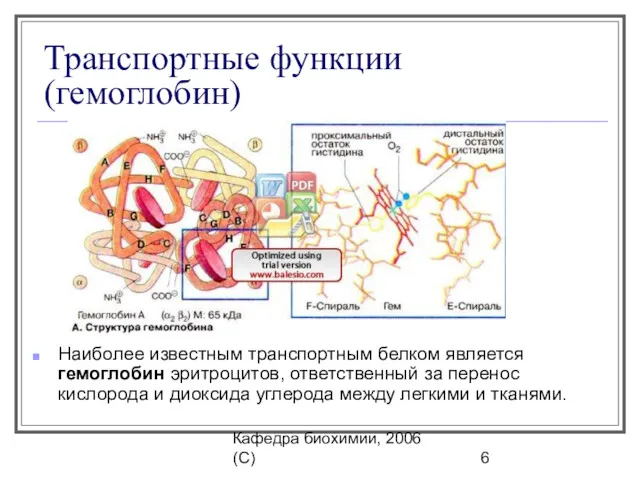
- 6. Кафедра биохимии, 2006 (C) Транспортные функции (гемоглобин) Наиболее известным транспортным белком является гемоглобин эритроцитов, ответственный за
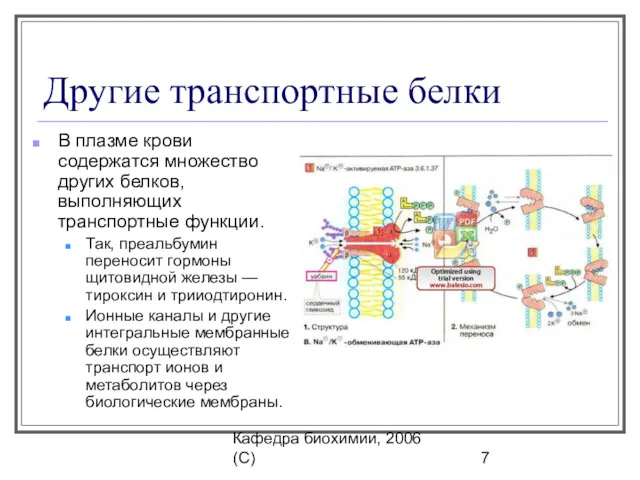
- 7. Кафедра биохимии, 2006 (C) Другие транспортные белки В плазме крови содержатся множество других белков, выполняющих транспортные
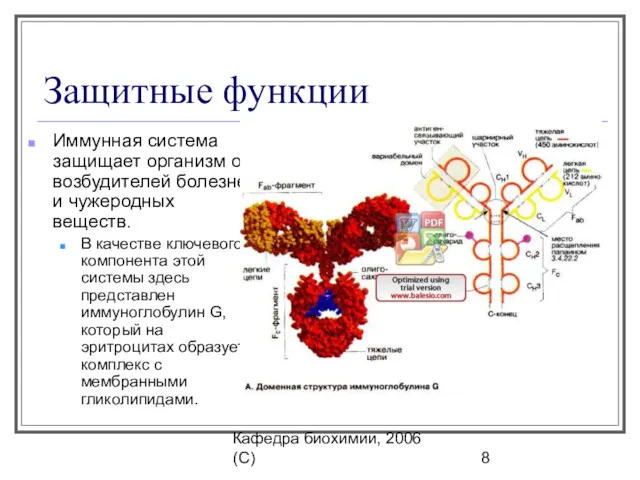
- 8. Кафедра биохимии, 2006 (C) Защитные функции Иммунная система защищает организм от возбудителей болезней и чужеродных веществ.
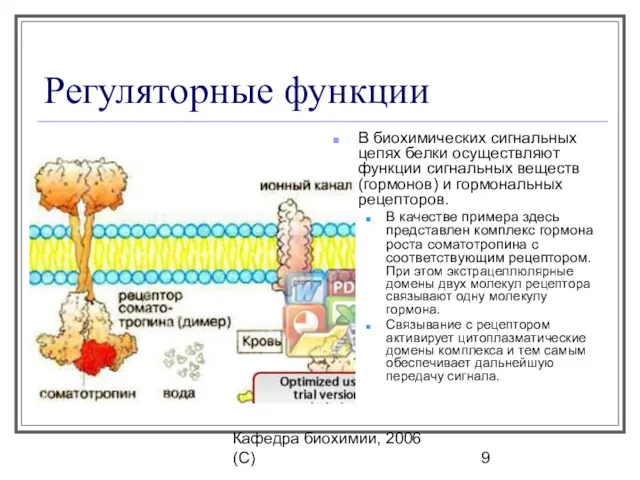
- 9. Кафедра биохимии, 2006 (C) Регуляторные функции В биохимических сигнальных цепях белки осуществляют функции сигнальных веществ (гормонов)
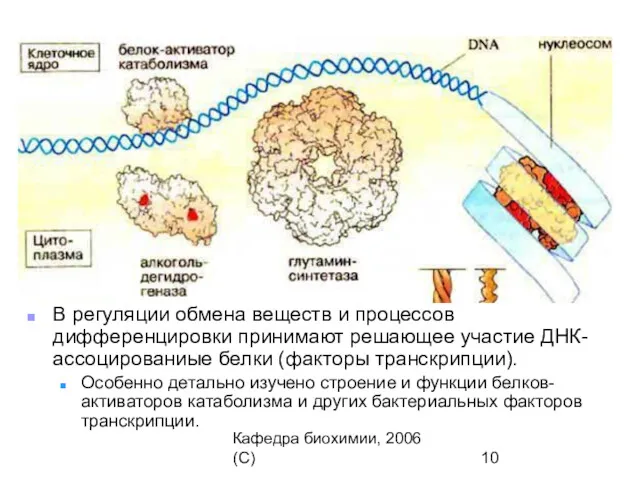
- 10. Кафедра биохимии, 2006 (C) В регуляции обмена веществ и процессов дифференцировки принимают решающее участие ДНК-ассоцированиые белки
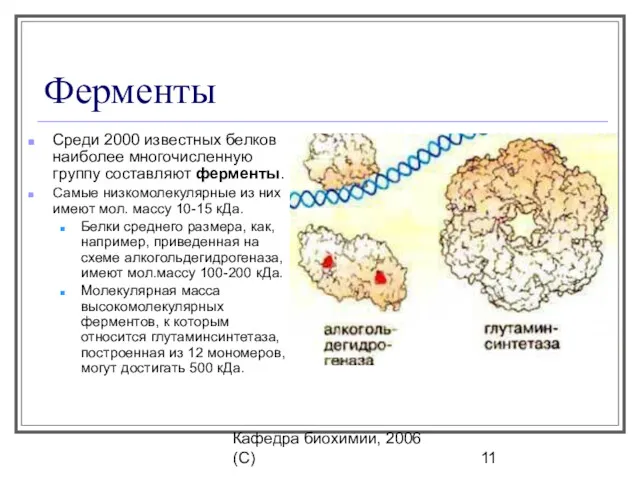
- 11. Кафедра биохимии, 2006 (C) Ферменты Среди 2000 известных белков наиболее многочисленную группу составляют ферменты. Самые низкомолекулярные
- 12. Кафедра биохимии, 2006 (C) Двигательные функции Взаимодействие актина с миозином ответственно за мышечное сокращение и другие
- 13. Кафедра биохимии, 2006 (C) Запасные функции В растениях содержатся запасные белки, являющиеся ценными пищевыми веществами. В
- 14. Кафедра биохимии, 2006 (C) Пептидная связь Главными структурными единицами белкой и пептидов являются остатки аминокислот, связанные
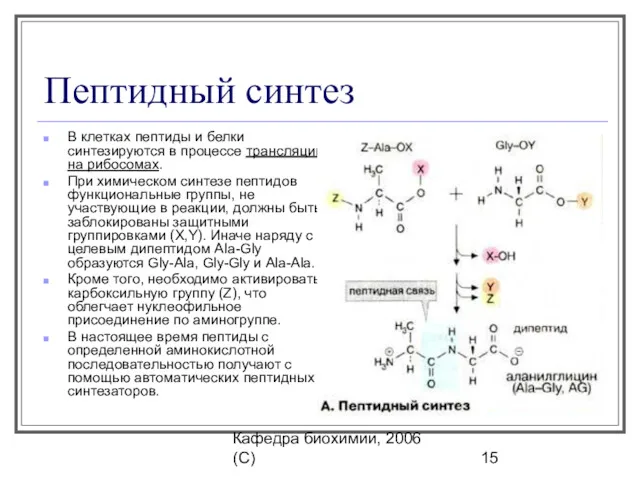
- 15. Кафедра биохимии, 2006 (C) Пептидный синтез В клетках пептиды и белки синтезируются в процессе трансляции на
- 16. Кафедра биохимии, 2006 (C) Мезомерия пептидной связи Как всякая карбоксамидная связь, пептидная связь стабилизирована за счет
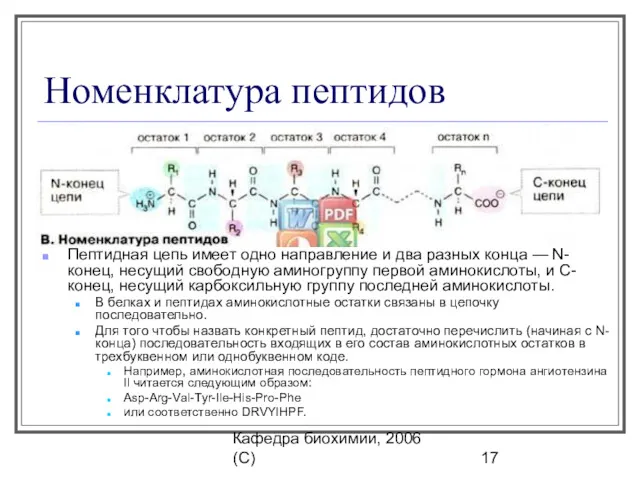
- 17. Кафедра биохимии, 2006 (C) Номенклатура пептидов Пептидная цепь имеет одно направление и два разных конца —
- 18. Кафедра биохимии, 2006 (C) Конформация полипептидной цепи Каждый аминокислотный остаток, за исключением концевых, принимает участие в
- 19. Кафедра биохимии, 2006 (C) Вторичные структуры белков Вторичные структуры стабилизированы водородными мостиками в пределах одной пептидной
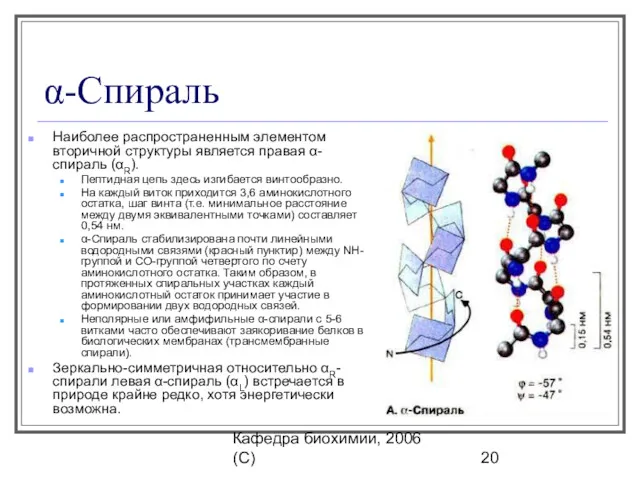
- 20. Кафедра биохимии, 2006 (C) α-Спираль Наиболее распространенным элементом вторичной структуры является правая α-спираль (αR). Пептидная цепь
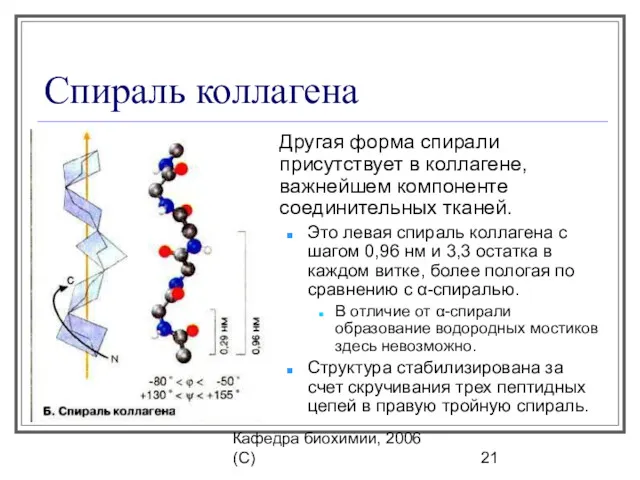
- 21. Кафедра биохимии, 2006 (C) Спираль коллагена Другая форма спирали присутствует в коллагене, важнейшем компоненте соединительных тканей.
- 22. Кафедра биохимии, 2006 (C) Складчатые структуры Две следующие почти вытянутые конформации пептидной цепи называются "β-складчатым листом",
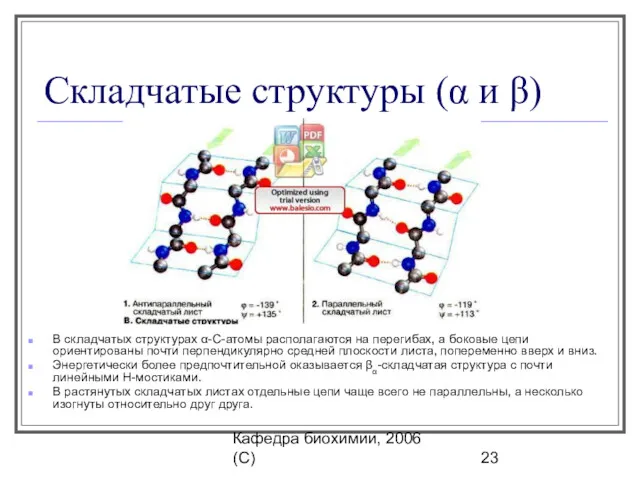
- 23. Кафедра биохимии, 2006 (C) Складчатые структуры (α и β) В складчатых структурах α-С-атомы располагаются на перегибах,
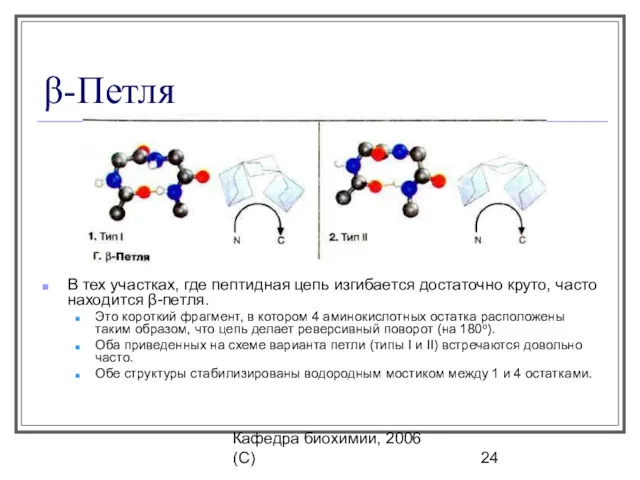
- 24. Кафедра биохимии, 2006 (C) β-Петля В тех участках, где пептидная цепь изгибается достаточно круто, часто находится
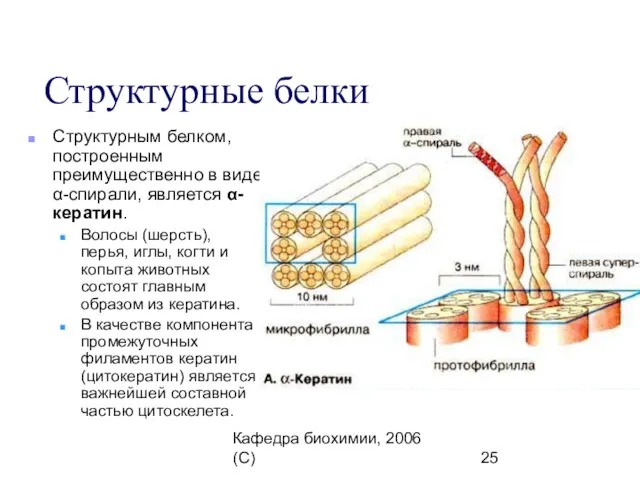
- 25. Кафедра биохимии, 2006 (C) Структурные белки Структурным белком, построенным преимущественно в виде α-спирали, является α-кератин. Волосы
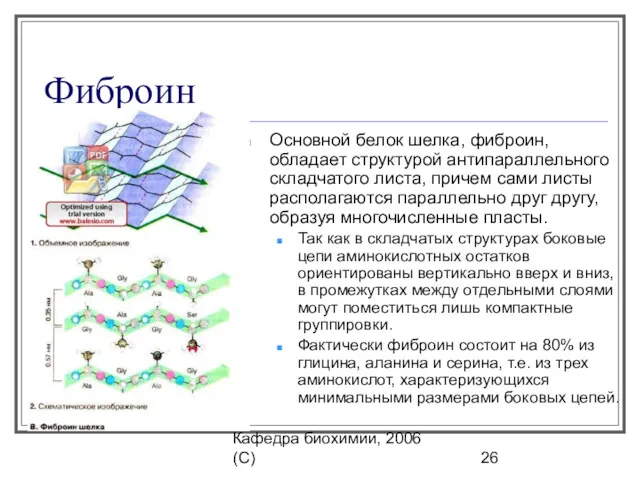
- 26. Кафедра биохимии, 2006 (C) Фиброин Ocновной белок шелка, фиброин, обладает структурой антипараллельного складчатого листа, причем сами
- 27. Кафедра биохимии, 2006 (C) Коллаген В организме млекопитающих коллаген — преобладающий в количественном отношении белок: он
- 28. Кафедра биохимии, 2006 (C) Глобулярные белки В отличие от нерастворимых фибриллярных белков растворимые белки имеют почти
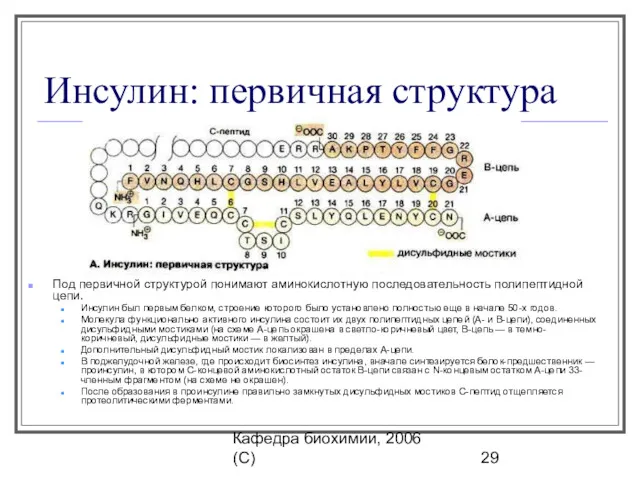
- 29. Кафедра биохимии, 2006 (C) Инсулин: первичная структура Под первичной структурой понимают аминокислотную последовательность полипептидной цепи. Инсулин
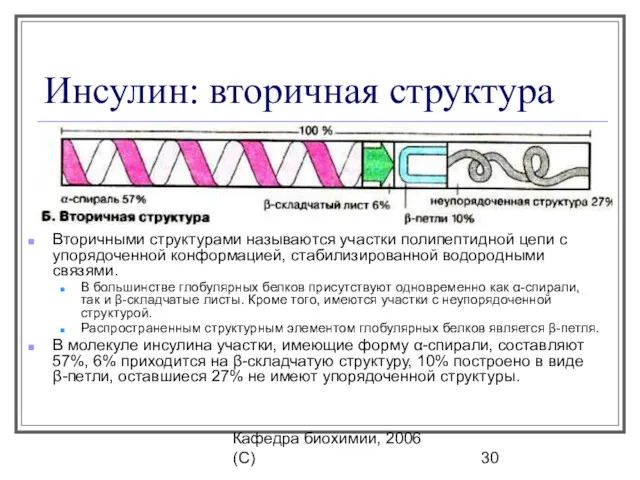
- 30. Кафедра биохимии, 2006 (C) Инсулин: вторичная структура Вторичными структурами называются участки полипептидной цепи с упорядоченной конформацией,
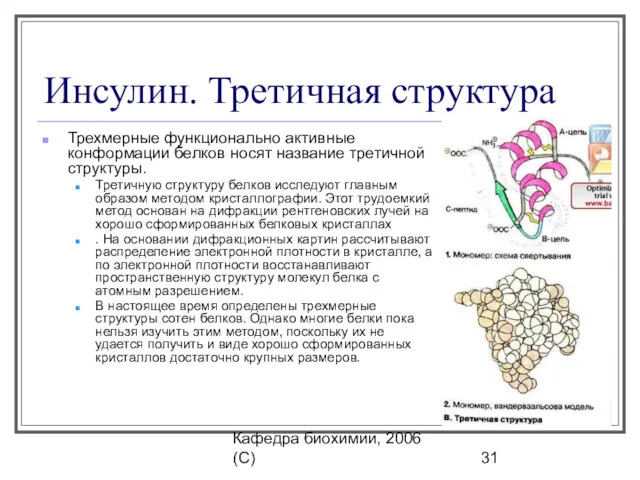
- 31. Кафедра биохимии, 2006 (C) Инсулин. Третичная структура Трехмерные функционально активные конформации белков носят название третичной структуры.
- 32. Кафедра биохимии, 2006 (C) Инсулин: анализ третичной структуры Анализ третичной структуры инсулина показал, что в Α-цепи
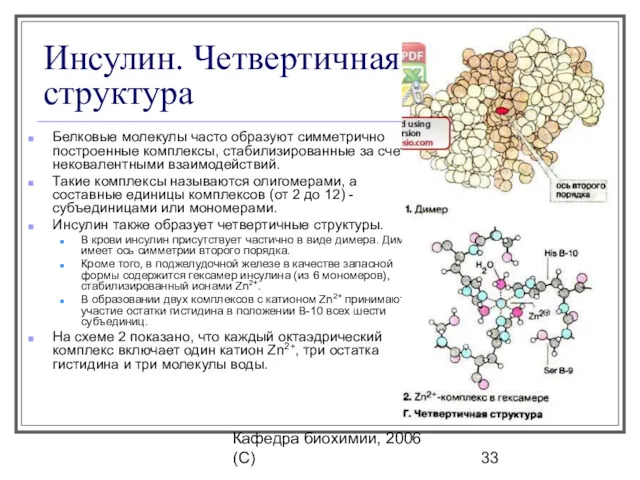
- 33. Кафедра биохимии, 2006 (C) Инсулин. Четвертичная структура Белковые молекулы часто образуют симметрично построенные комплексы, стабилизированные за
- 34. Кафедра биохимии, 2006 (C) Свертывание белков При сравнении наиболее крупных глобулярных белков становится очевидным, что существует
- 35. Кафедра биохимии, 2006 (C) Свертывание белков: примеры Рассмотрим ряд примеров (α-спирали выделены красным цветом, плоскости складчатого
- 36. Кафедра биохимии, 2006 (C) Методы выделения и анализа белков Препараты высокоочищенных белков находят разнообразное применение в
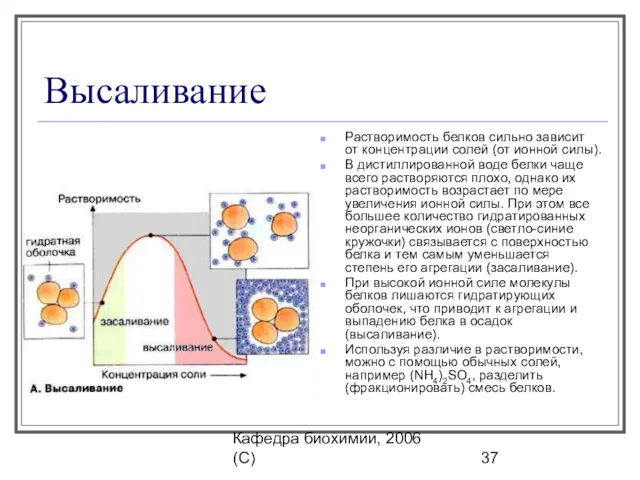
- 37. Кафедра биохимии, 2006 (C) Высаливание Растворимость белков сильно зависит от концентрации солей (от ионной силы). В
- 38. Кафедра биохимии, 2006 (C) Диализ Для отделения низкомолекулярных примесей или замены состава среды используют диализ. Метод
- 39. Кафедра биохимии, 2006 (C) Гель-фильтрация Гель-проникающая хроматография (гель-фильтрация) позволяет разделять белки по величине и форме молекул.
- 40. Кафедра биохимии, 2006 (C) Электрофорез в полиакриламидном геле в присутствии додецилсульфата натрия Метод основан на свойстве
- 41. Кафедра биохимии, 2006 (C) Под действием ДСН олигомерные белки диссоциируют на субъединицы и денатурируют. Развернутые полипептидные
- 43. Скачать презентацию



















 Звери и птицы весной
Звери и птицы весной Большой (конечный) мозг
Большой (конечный) мозг Исследовательская работа по биологии
Исследовательская работа по биологии Протеомика. Методы молекулярной биологии и биинформатики в изучении белков
Протеомика. Методы молекулярной биологии и биинформатики в изучении белков Investigate DNA Extraction
Investigate DNA Extraction Строение цветка. Соцветия
Строение цветка. Соцветия Réserves Naturelles De Russie
Réserves Naturelles De Russie Нейромедиаторы. Критерии нейромедиатора
Нейромедиаторы. Критерии нейромедиатора Царство животные. Тип губки
Царство животные. Тип губки Северцов Николай Алексеевич. Биография.
Северцов Николай Алексеевич. Биография. Лекарственные растения
Лекарственные растения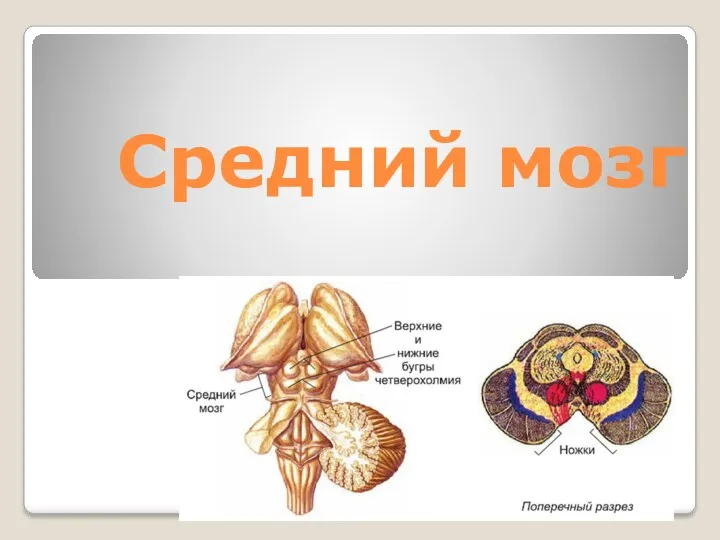 Средний мозг. Строение
Средний мозг. Строение Применение дрожжей для снижения стоимости и улучшения качества молока
Применение дрожжей для снижения стоимости и улучшения качества молока Каталитическая функция белков и синтетическая теория эволюции
Каталитическая функция белков и синтетическая теория эволюции Анатомия зрительного анализатора
Анатомия зрительного анализатора Царство Растения. Высшие семенные растения. Покрытосеменные ( = цветковые)
Царство Растения. Высшие семенные растения. Покрытосеменные ( = цветковые) Минеральное питание растений
Минеральное питание растений Органы ротовой полости у животных
Органы ротовой полости у животных Теория Чарльза Дарвина. Искусственный отбор
Теория Чарльза Дарвина. Искусственный отбор Регуляция пищеварения. Гигиена питания
Регуляция пищеварения. Гигиена питания Изучение биоритмов человека – их влияние на жизнедеятельность
Изучение биоритмов человека – их влияние на жизнедеятельность Отряд Черепахи
Отряд Черепахи Наука биология
Наука биология История развития анатомии, физиологии и медицины
История развития анатомии, физиологии и медицины Орган слуха и равновесия
Орган слуха и равновесия Движение крови по сосудам. Кровяное давление. Регуляция кровообращения
Движение крови по сосудам. Кровяное давление. Регуляция кровообращения Человек как уникальный вид живой природы
Человек как уникальный вид живой природы Бейімделу физиологиясы
Бейімделу физиологиясы