Содержание
- 2. Биофизика - наука о физико-химических явлениях в живых системах, находящихся в неразрывной связи с окружающей средой
- 3. Основные признаки живой материи Питание. Пища – источник энергии и веществ, необходимых для роста и других
- 4. Задачи биофизики: Раскрытие общих закономерностей поведения открытых неравновесных систем. Теоретическое обоснование термодинамических основ жизни. Научное объяснение
- 5. Биофизика подразделяется на такие области: Молекулярная биофизика изучает строение и физико-химические свойства, биофизику молекул. Биофизика клетки
- 6. Молекулярная биофизика – часть биологической физики, основными объектами изучения которой являются биологические полимеры – белки, нуклеиновые
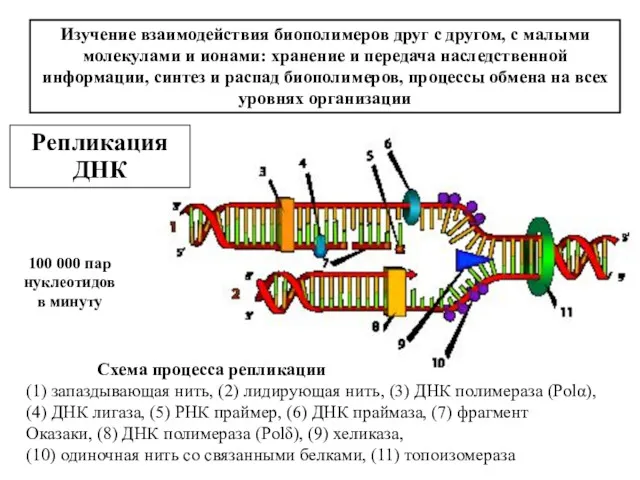
- 7. Изучение взаимодействия биополимеров друг с другом, с малыми молекулами и ионами: хранение и передача наследственной информации,
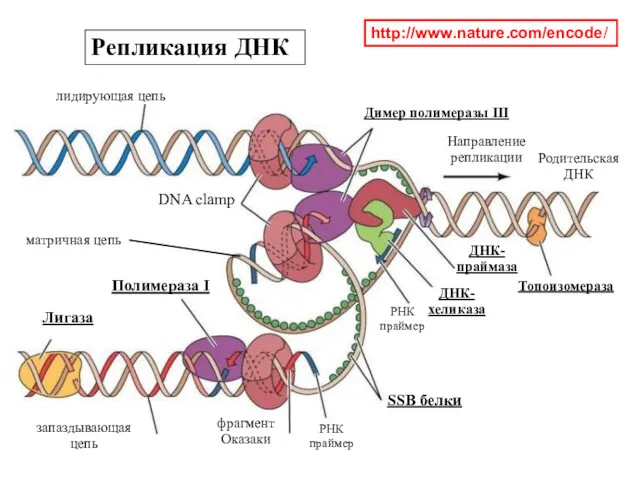
- 8. http://www.nature.com/encode/
- 9. Для осуществления всех перечисленных процессов необходимо создание определенных, биологически функциональных или нативных структур биополимеров, устойчивость нативных
- 10. Эрвин Шредингер «Что такое жизнь? Физический аспект живой клетки» «Большой, важный и очень часто обсуждаемый вопрос
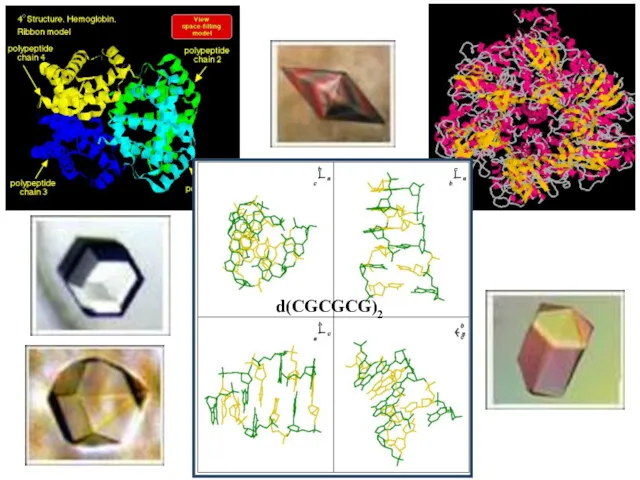
- 11. d(CGCGCG)2
- 12. Все своеобразие живых организмов, отличающее их от тел неживой природы, возникает в результате особой организации сложных
- 13. Молекулярная физика Основные задачи: Определение строения вещества на атомном и молекулярном уровнях 2. Исследование равновесных систем
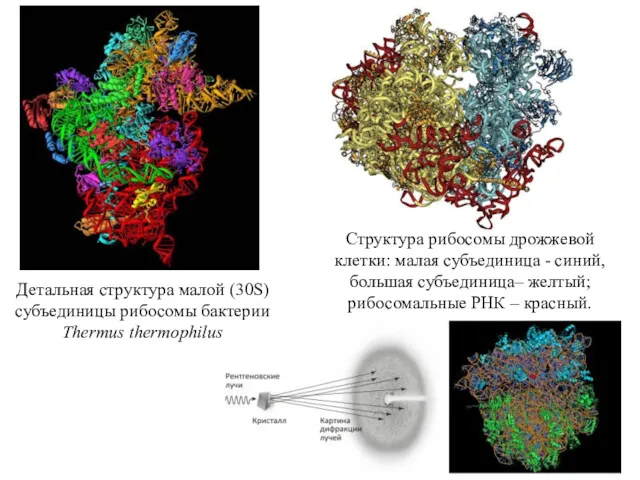
- 14. Детальная структура малой (30S) субъединицы рибосомы бактерии Thermus thermophilus Структура рибосомы дрожжевой клетки: малая субъединица -
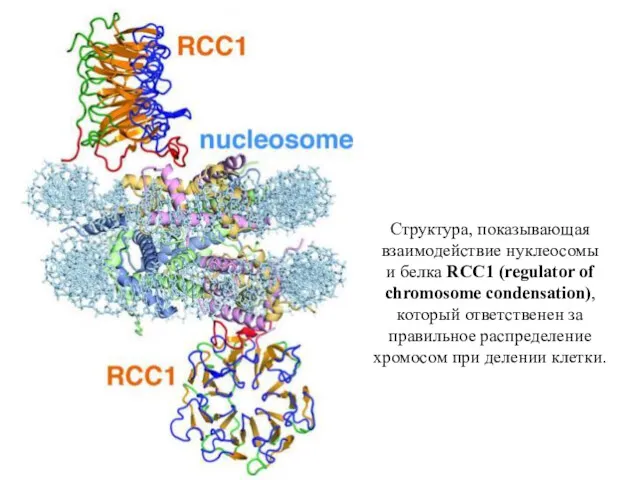
- 15. Структура, показывающая взаимодействие нуклеосомы и белка RCC1 (regulator of chromosome condensation), который ответственен за правильное распределение
- 16. Система - это совокупность материальных объектов, ограниченных каким-либо образом от окружающей среды. В зависимости от характера
- 17. Энергия (U, E, F, G, ΔU, dU, ΔE, dE, ΔF, dF, ΔG, dG) – количественная мера
- 18. Механическая энергия – форма энергии, характеризующая движения макротел и способность совершать механическую работу по перемещению макротел.
- 19. Первый закон термодинамики Общая сумма энергии материальной системы остается постоянной величиной независимо от изменений, происходящих в
- 20. Внутренняя энергия (U, ΔU, dU) – это общая сумма всех видов энергии в данной системе (тепловой,
- 21. Первый закон термодинамики: Изменение внутренней энергии системы ΔU равно алгебраической сумме тепла, переданного в процессе ΔQ,
- 22. Полное теплосодержание системы – энтальпия (H, ΔH, dH) – мера изменения теплоты системы, соответствует теплообмену при
- 23. Формулировка первого закона термодинамики для живых систем Все виды работы, совершаемые в живом организме, совершаются за
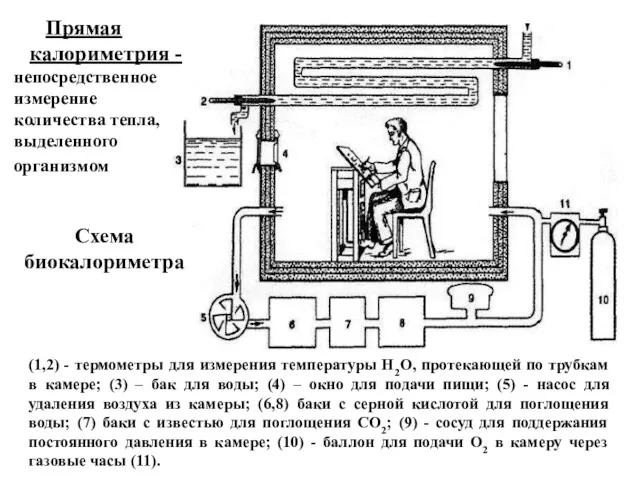
- 24. Опытная проверка применимости первого закона для живых систем проводилась в специальных биокалориметрах, где измерялась теплота, выделенная
- 25. (1,2) - термометры для измерения температуры Н2О, протекающей по трубкам в камере; (3) – бак для
- 26. К – камера; Б – баллон с кислородом; Н – мотор, выкачивающий воздух из камеры; З
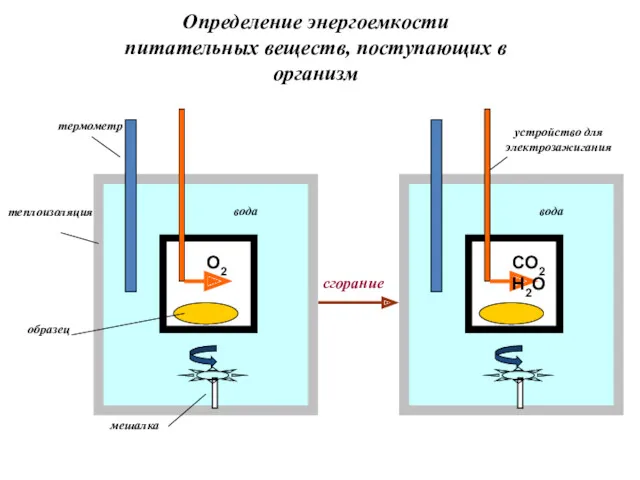
- 27. Определение энергоемкости питательных веществ, поступающих в организм
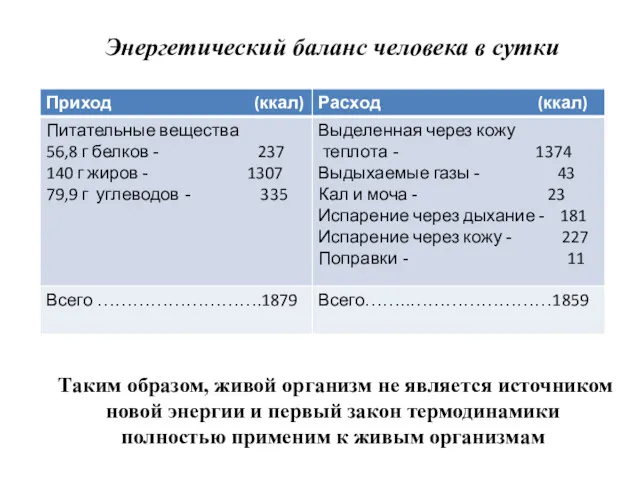
- 28. Энергетический баланс человека в сутки Таким образом, живой организм не является источником новой энергии и первый
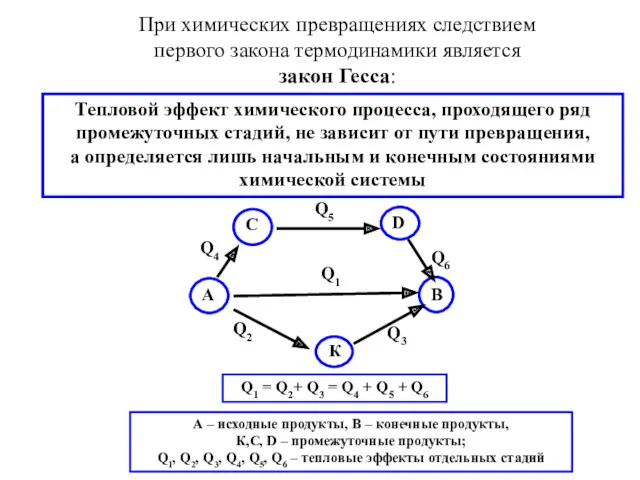
- 29. При химических превращениях следствием первого закона термодинамики является закон Гесса: Тепловой эффект химического процесса, проходящего ряд
- 30. Первый закон термодинамики Общая сумма энергии материальной системы остается постоянной величиной независимо от изменений, происходящих в
- 31. Лекция 2. Обратимые и необратимые процессы. Свободная энергия, энтропия. Второй закон термодинамики. Стационарное состояние. Теорема Пригожина.
- 32. Свободная энергия, энтропия. Термодинамическое равновесие - такое состояние системы, когда изменения различных видов энергии выровнены, и
- 33. Свободная энергия G – это способность системы совершать работу Свободная энергия определяется как G = U
- 34. Градиент Г какого-либо параметра представляет собой отношение разности его значений в двух точках ΔI к расстоянию
- 35. Второй закон термодинамики устанавливает критерий, отражающий одностороннюю направленность необратимых (неравновесных) процессов не зависимо от их конкретной
- 36. Согласно второму закону термодинамики, состояние системы может быть описано особой функцией – энтропией S. Энтропия определяет
- 37. То есть, при обратимых процессах изменение энтропии равно нулю ΔS = 0, а при необратимых оно
- 38. Общая формулировка второго закона термодинамики: Любой самопроизвольный процесс в изолированной системе приводит к уменьшению свободной энергии,
- 39. Роль энтропии 1. Энтропия как мера рассеяния энергии при необратимых процессах Чем больше возрастание энтропии при
- 40. 3. Энтропия - мера упорядоченности системы S=klnW - уравнение Планка-Больцмана где S - энтропия, k -
- 41. 4. Связь между энтропией и информацией Макроскопическое состояние некоторой системы: с определенной степенью точности указаны значения
- 42. Термодинамическая вероятность W – это количество микросостояний, возможных в пределах данного макросостояния. Величина W непосредственно связана
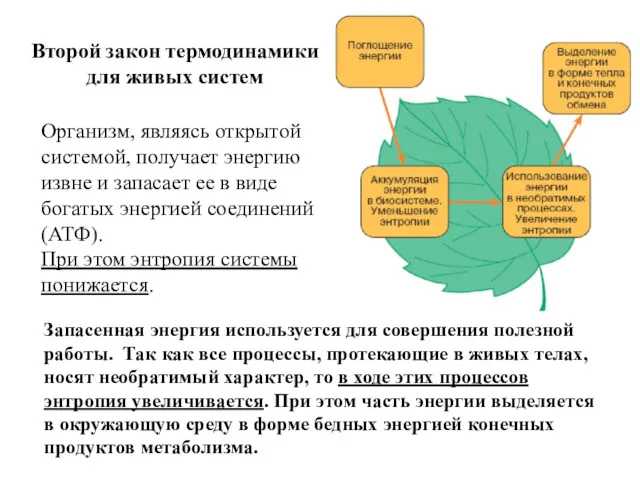
- 43. Организм, являясь открытой системой, получает энергию извне и запасает ее в виде богатых энергией соединений (АТФ).
- 44. Общее изменение энтропии dS открытой системы может происходить независимо либо за счет процессов обмена с внешней
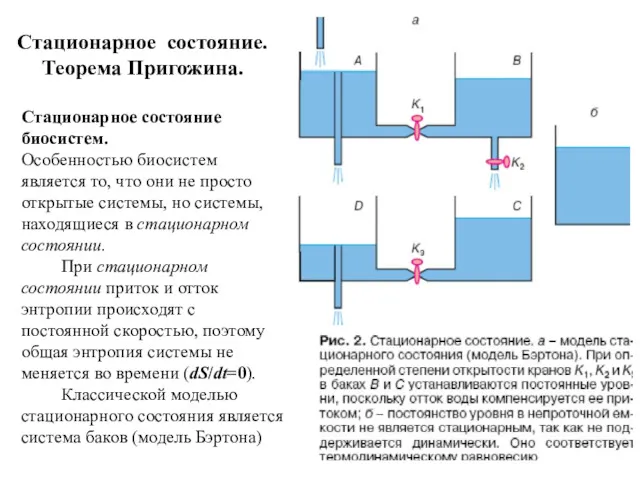
- 45. Стационарное состояние. Теорема Пригожина. Стационарное состояние биосистем. Особенностью биосистем является то, что они не просто открытые
- 46. В стационарном состоянии скорость возрастания энтропии, обусловленного протеканием необратимых процессов, имеет положительное и минимальное из возможных
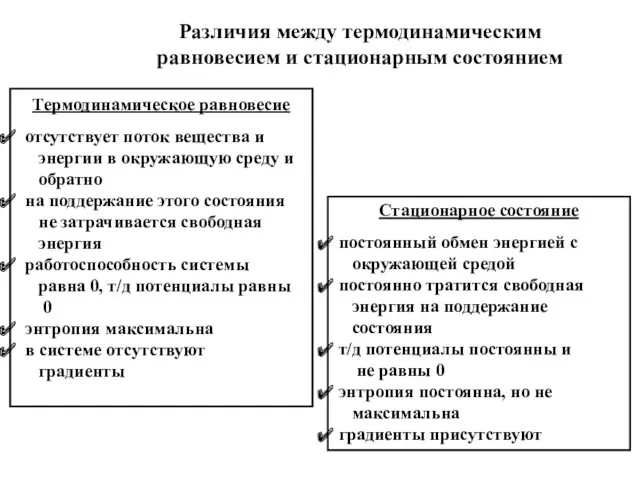
- 47. Термодинамическое равновесие отсутствует поток вещества и энергии в окружающую среду и обратно на поддержание этого состояния
- 49. Скачать презентацию


































 Паразитические плоские черви
Паразитические плоские черви Амурский тигр
Амурский тигр Роль жирів в організмі людини
Роль жирів в організмі людини Дүниежүзілік мұхит
Дүниежүзілік мұхит Приспособительные формы организмов
Приспособительные формы организмов Царство Бактерии
Царство Бактерии Алтайский заповедник
Алтайский заповедник Урок по биологии в 5 классе Жизнь в мировом океане
Урок по биологии в 5 классе Жизнь в мировом океане Первичные и вторичные метаболиты
Первичные и вторичные метаболиты Транскрипция и трансляция
Транскрипция и трансляция Esophagus. Esophageal Structure
Esophagus. Esophageal Structure Клетка. Растительная клетка
Клетка. Растительная клетка Строение амёбоидной клетки, на примере Amoeba proteus и Arcella sp
Строение амёбоидной клетки, на примере Amoeba proteus и Arcella sp Анатомия, физиология, патология зрительного анализатора
Анатомия, физиология, патология зрительного анализатора Болезни цветочных культур защищенного грунта. (Лекция 18)
Болезни цветочных культур защищенного грунта. (Лекция 18) Презентация по биологии Бесполое размножение организмов
Презентация по биологии Бесполое размножение организмов Развитие эмбриологии в XVI—XVIII и начале XIX века. (Лекция 10)
Развитие эмбриологии в XVI—XVIII и начале XIX века. (Лекция 10) Механізм скорочення м’язового волокна. (Лекція 6)
Механізм скорочення м’язового волокна. (Лекція 6) Химический состав клеток. Углеводы. Липиды
Химический состав клеток. Углеводы. Липиды Особливості будови дощового черв’яка
Особливості будови дощового черв’яка Урок 8 класса с учетом новых ФГОС
Урок 8 класса с учетом новых ФГОС Индивидуальные и групповые особенности моторики (дифференциальная биомеханика)
Индивидуальные и групповые особенности моторики (дифференциальная биомеханика) Клиническая анатомия, физиология среднего уха. Особенности строения у детей
Клиническая анатомия, физиология среднего уха. Особенности строения у детей Строение клетки. Основные органоиды (9 класс)
Строение клетки. Основные органоиды (9 класс) Человек как фактор развития природы: ноосфера vs антропоцен
Человек как фактор развития природы: ноосфера vs антропоцен Высшая нервная деятельность и ее возрастные особенности. Часть 1
Высшая нервная деятельность и ее возрастные особенности. Часть 1 Многообразие Кишечнополостных
Многообразие Кишечнополостных Биология. Ребусы и загадки
Биология. Ребусы и загадки