Биологически активные гетероциклические соединения. Нуклеотиды. Нуклеиновые кислоты. (Лекция 4) презентация
Содержание
- 2. Гетероциклическими называют соединения, молекулы которых содержат циклы, включающие наряду с атомами углерода один или несколько гетероатомов.
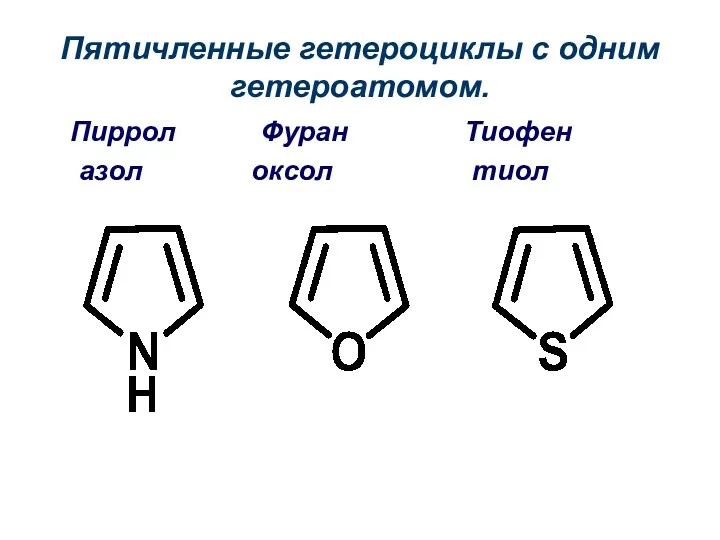
- 3. Пятичленные гетероциклы с одним гетероатомом. Пиррол Фуран Тиофен азол оксол тиол
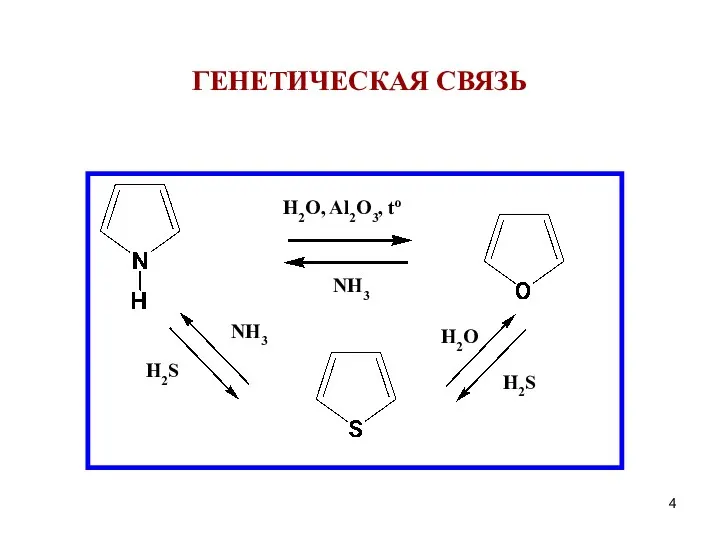
- 4. H2O, Al2O3, to NH3 H2S H2O H2S NH3 ГЕНЕТИЧЕСКАЯ СВЯЗЬ
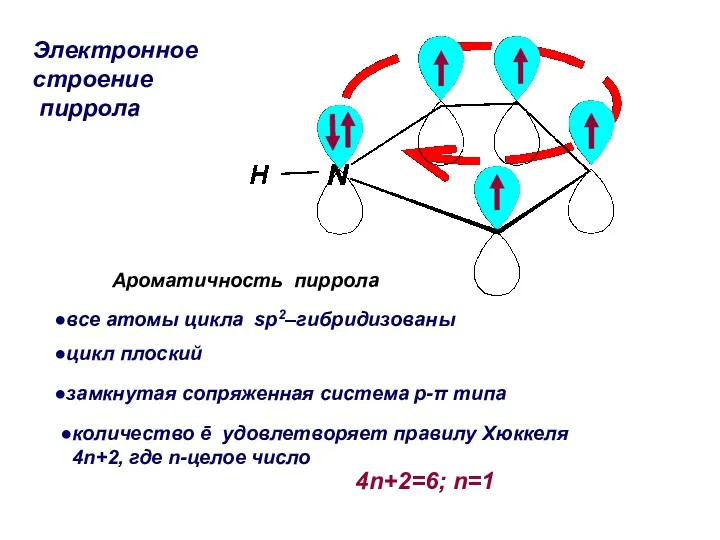
- 5. 4n+2=6; n=1 все атомы цикла sp2–гибридизованы цикл плоский замкнутая сопряженная система p-π типа количество ē удовлетворяет
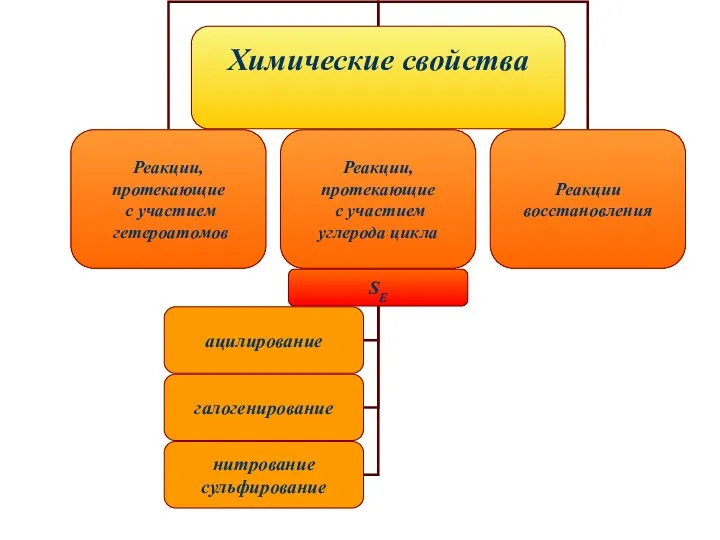
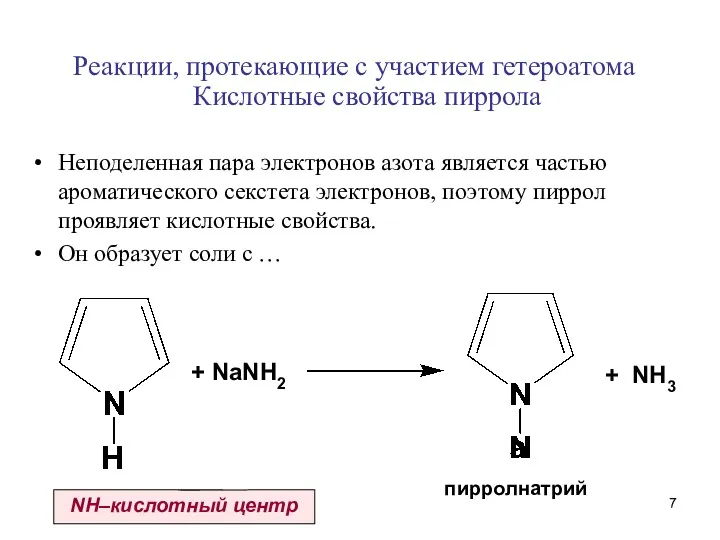
- 7. Реакции, протекающие с участием гетероатома Кислотные свойства пиррола Неподеленная пара электронов азота является частью ароматического секстета
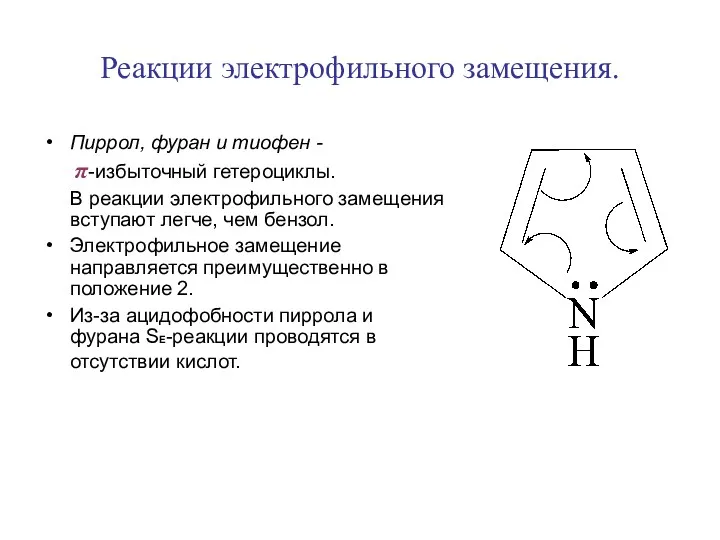
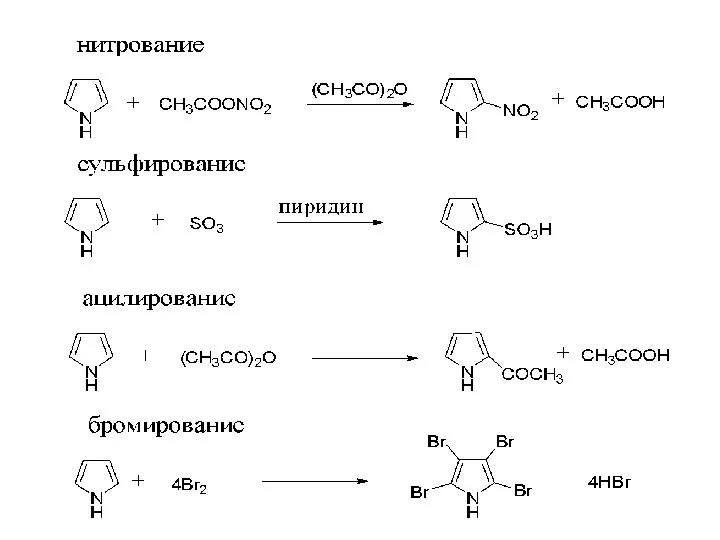
- 8. Реакции электрофильного замещения. Пиррол, фуран и тиофен - π-избыточный гетероциклы. В реакции электрофильного замещения вступают легче,
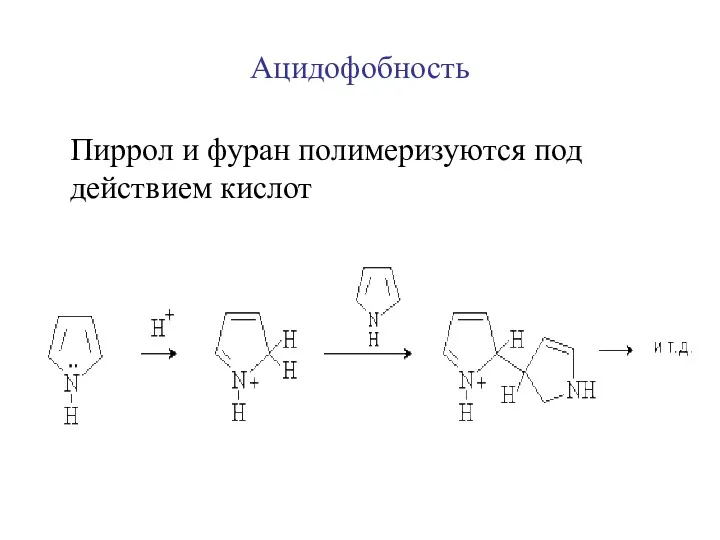
- 9. Ацидофобность Пиррол и фуран полимеризуются под действием кислот
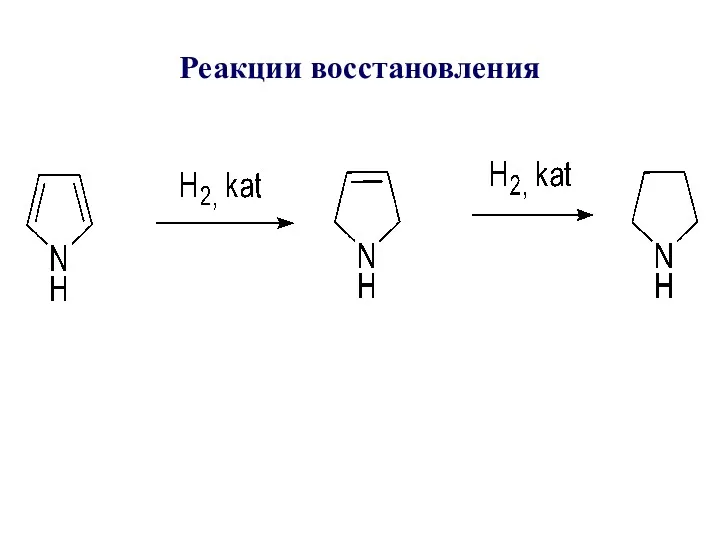
- 11. Реакции восстановления
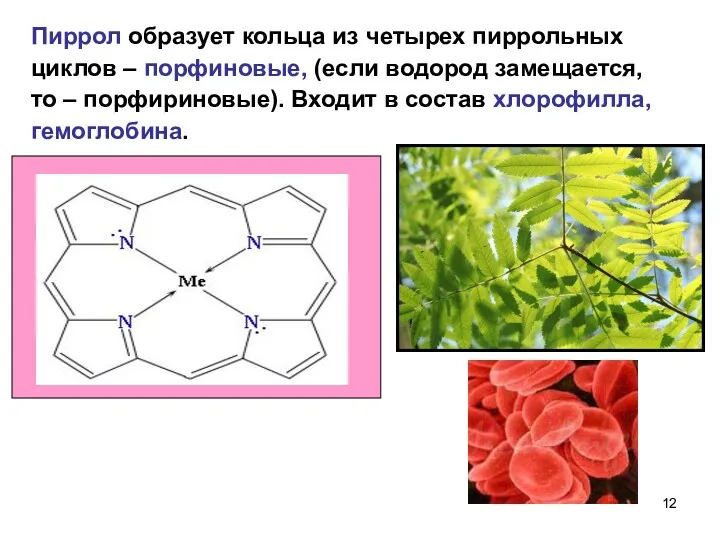
- 12. Пиррол образует кольца из четырех пиррольных циклов – порфиновые, (если водород замещается, то – порфириновые). Входит
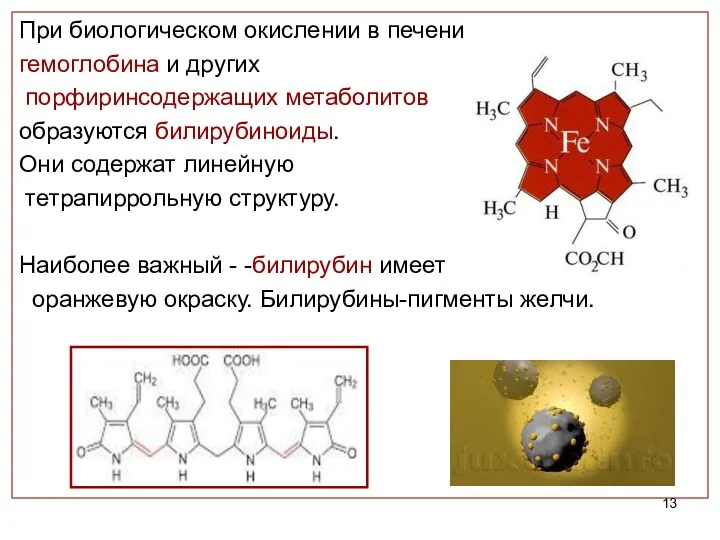
- 13. При биологическом окислении в печени гемоглобина и других порфиринсодержащих метаболитов образуются билирубиноиды. Они содержат линейную тетрапиррольную
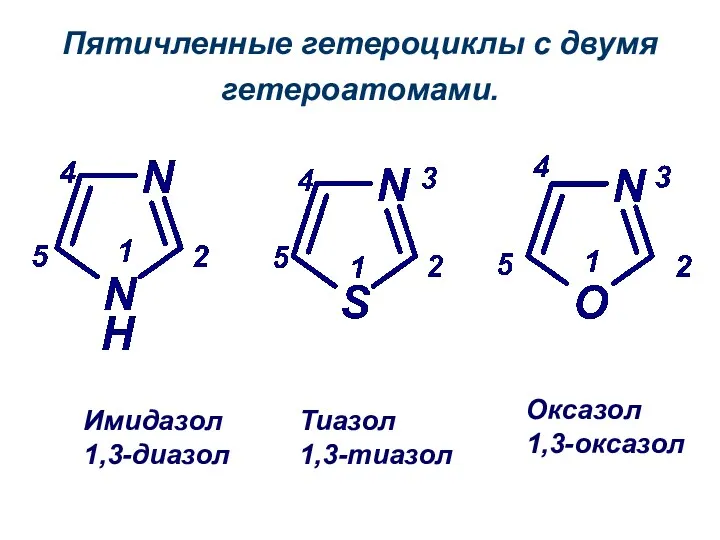
- 14. Имидазол 1,3-диазол Тиазол 1,3-тиазол Оксазол 1,3-оксазол Пятичленные гетероциклы с двумя гетероатомами.
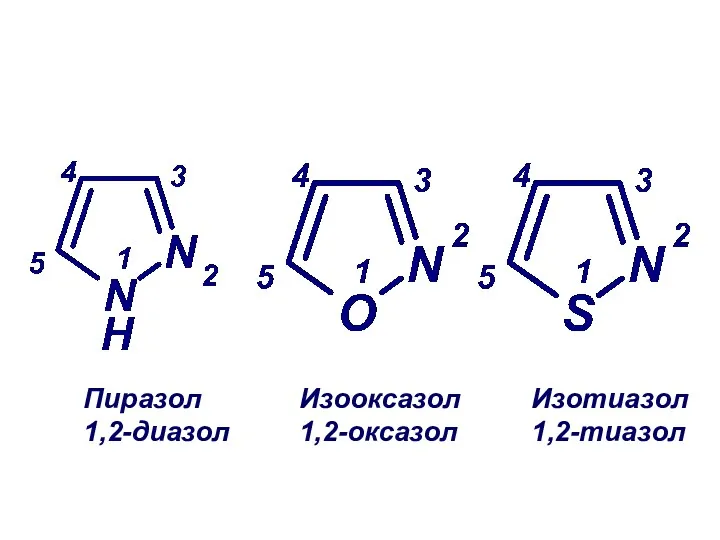
- 15. Пиразол 1,2-диазол Изооксазол 1,2-оксазол Изотиазол 1,2-тиазол
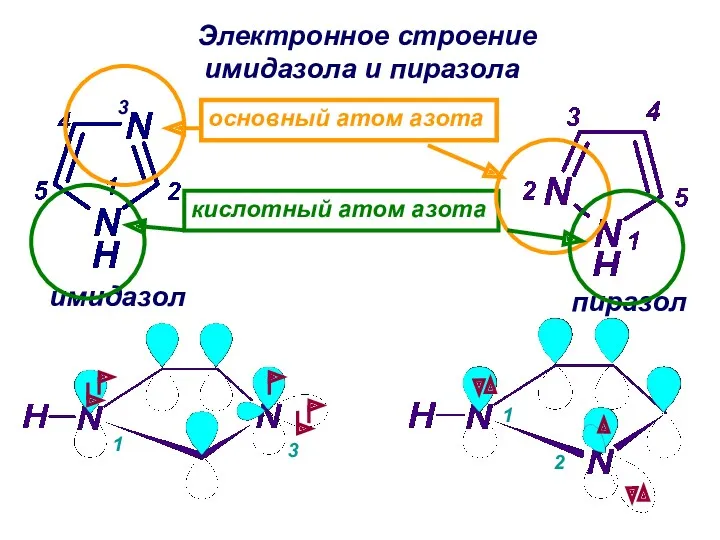
- 16. имидазол пиразол Электронное строение имидазола и пиразола кислотный атом азота основный атом азота 3 1 1
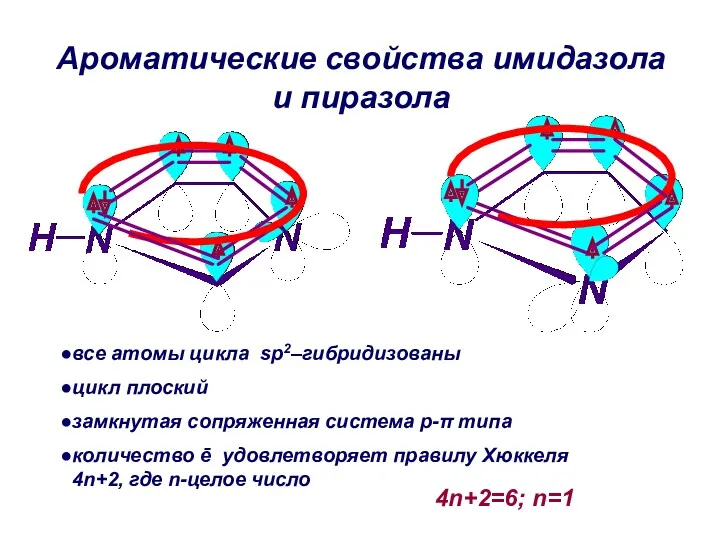
- 17. Ароматические свойства имидазола и пиразола все атомы цикла sp2–гибридизованы цикл плоский замкнутая сопряженная система p-π типа
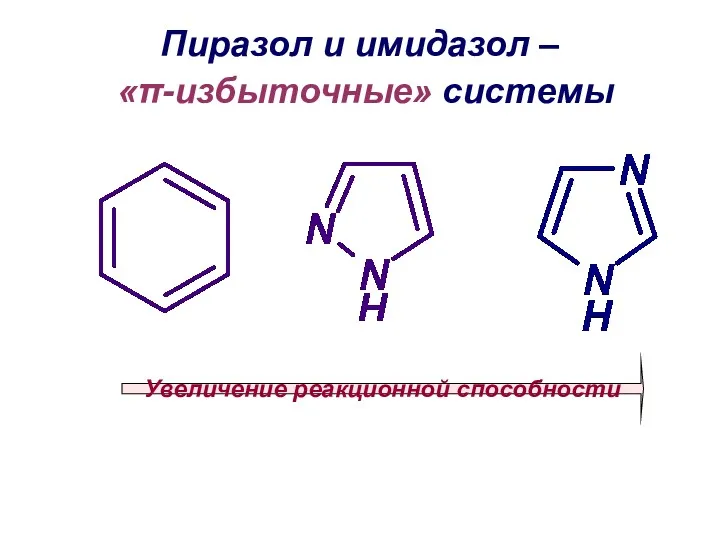
- 18. Пиразол и имидазол – «π-избыточные» системы Увеличение реакционной способности
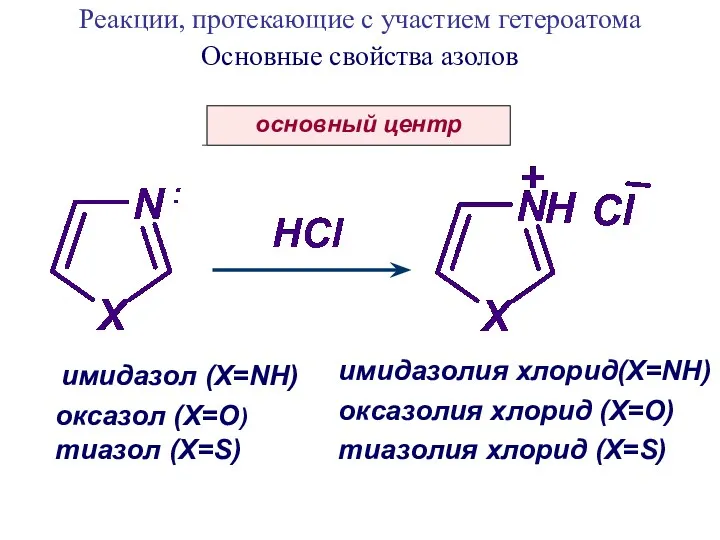
- 19. Реакции, протекающие с участием гетероатома Основные свойства азолов основный центр имидазолия хлорид(X=NH) имидазол (X=NH) оксазол (X=O)
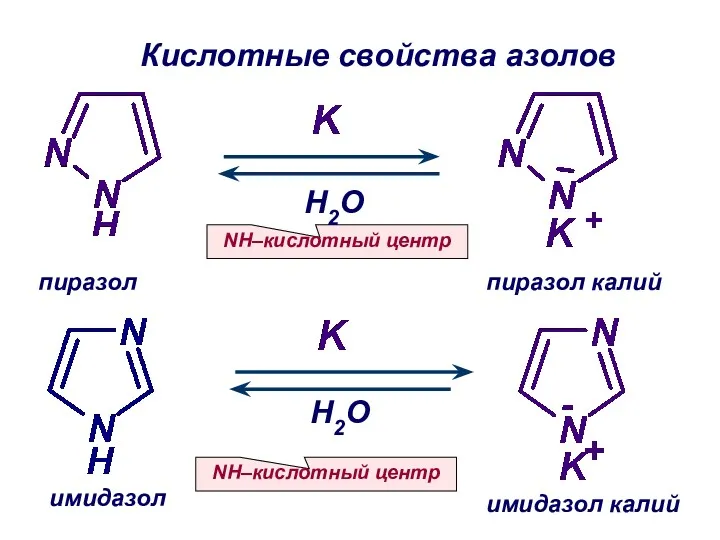
- 20. NH–кислотный центр имидазол калий Кислотные свойства азолов NH–кислотный центр имидазол пиразол калий пиразол H2O H2O
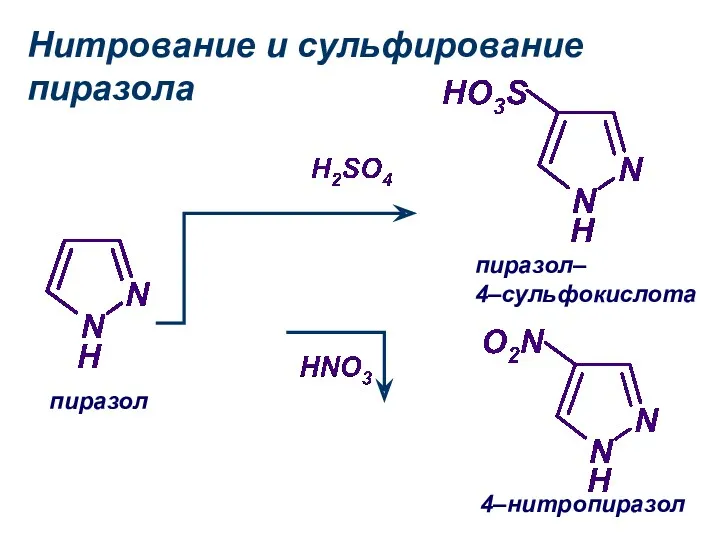
- 21. Нитрование и сульфирование пиразола пиразол 4–нитропиразол пиразол– 4–сульфокислота
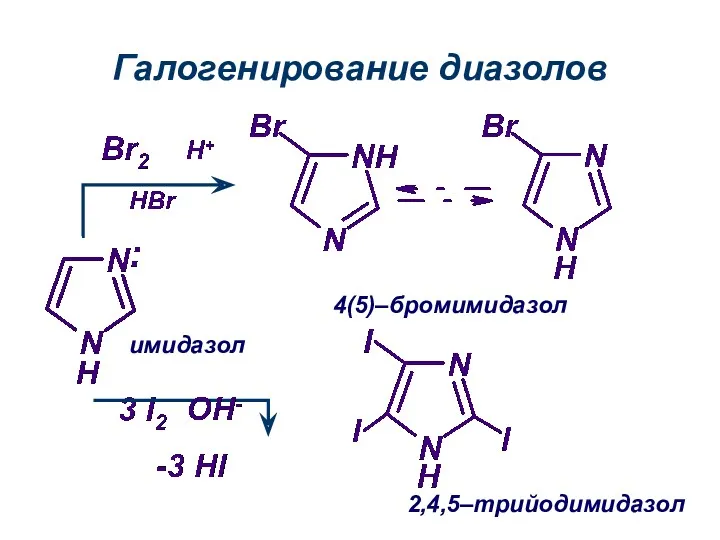
- 22. Галогенирование диазолов имидазол 2,4,5–трийодимидазол 4(5)–бромимидазол
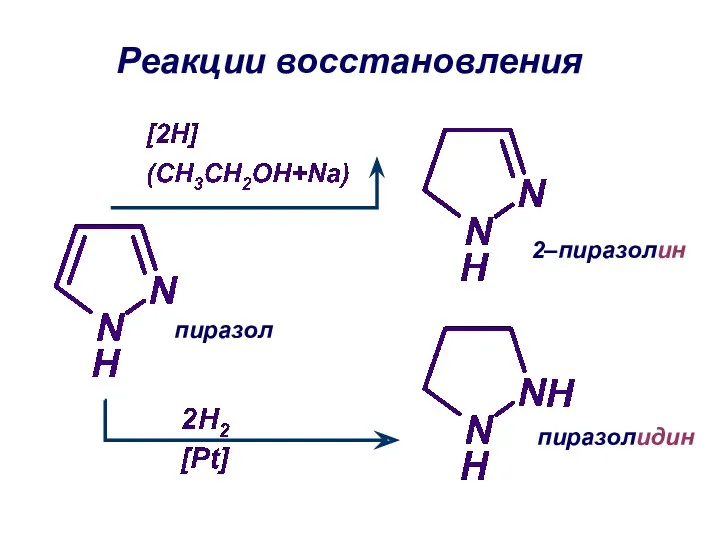
- 23. Реакции восстановления пиразол 2–пиразолин пиразолидин
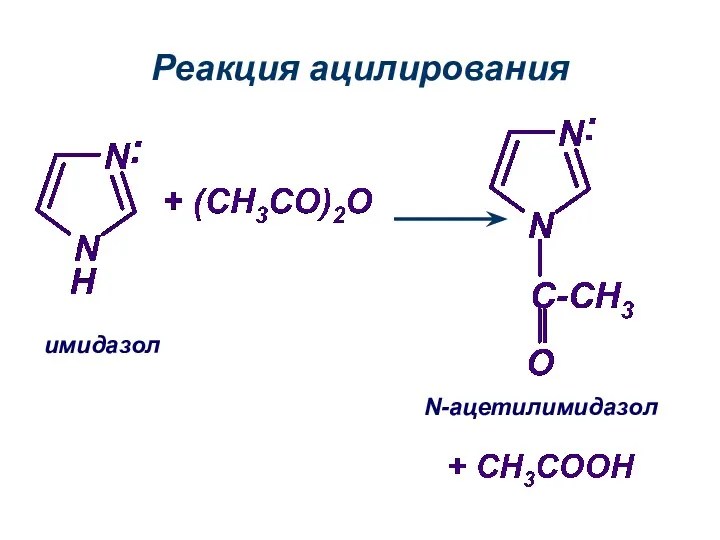
- 24. Реакция ацилирования имидазол N-ацетилимидазол
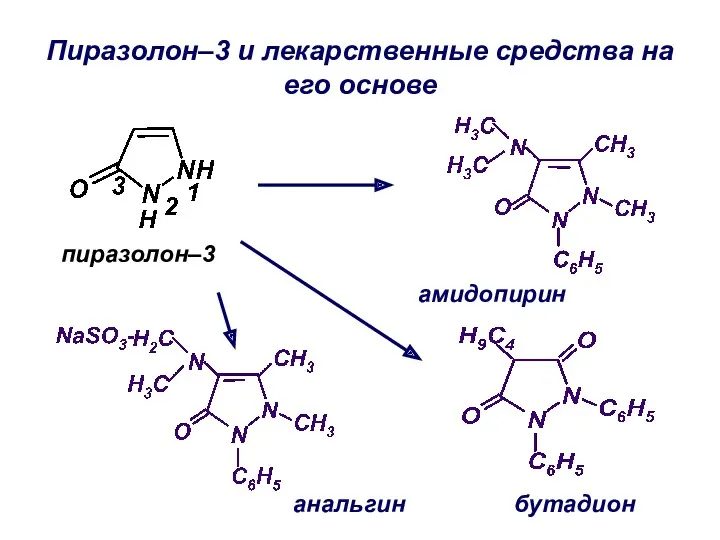
- 25. Пиразолон–3 и лекарственные средства на его основе пиразолон–3 анальгин бутадион амидопирин
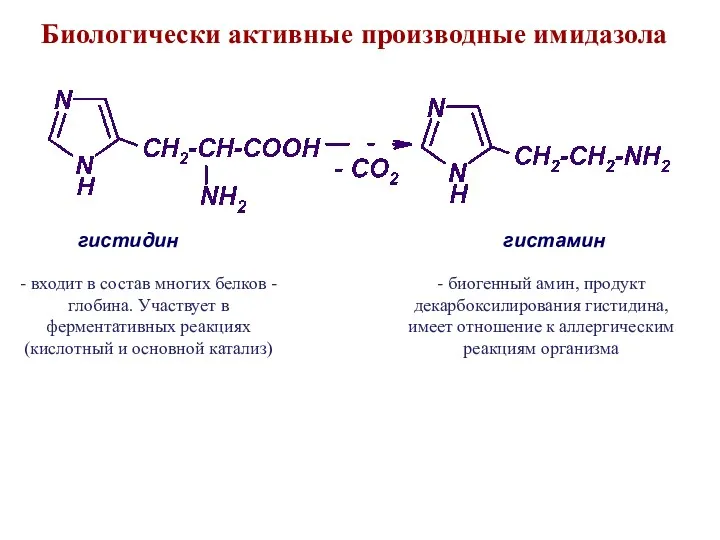
- 26. гистидин гистамин Биологически активные производные имидазола - входит в состав многих белков -глобина. Участвует в ферментативных
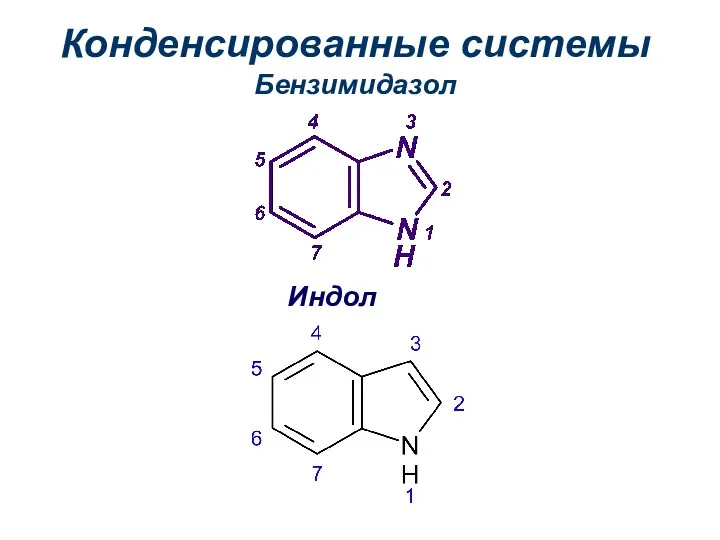
- 27. Конденсированные системы Бензимидазол Индол
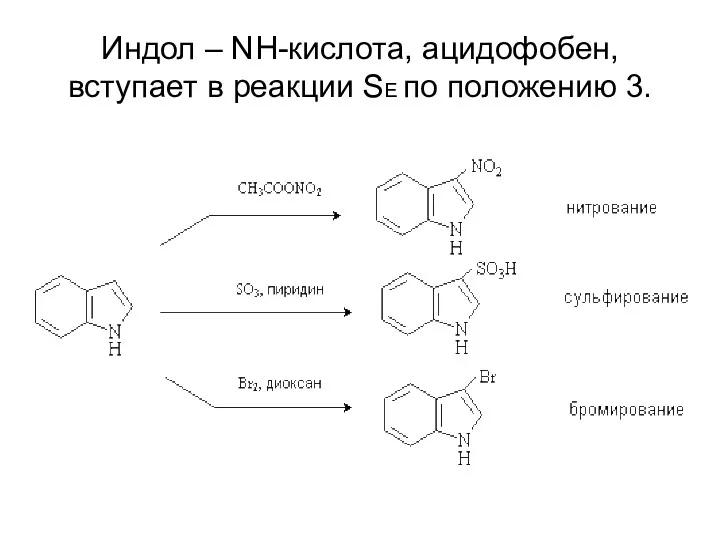
- 28. Индол – NH-кислота, ацидофобен, вступает в реакции SЕ по положению 3.
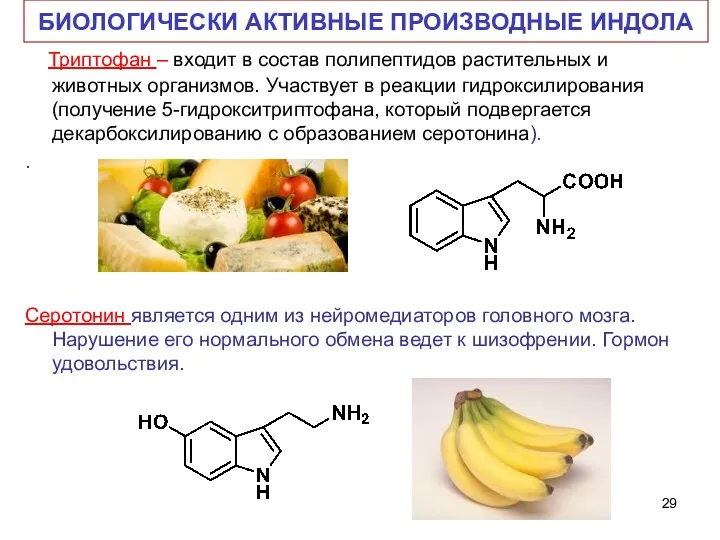
- 29. БИОЛОГИЧЕСКИ АКТИВНЫЕ ПРОИЗВОДНЫЕ ИНДОЛА Триптофан – входит в состав полипептидов растительных и животных организмов. Участвует в
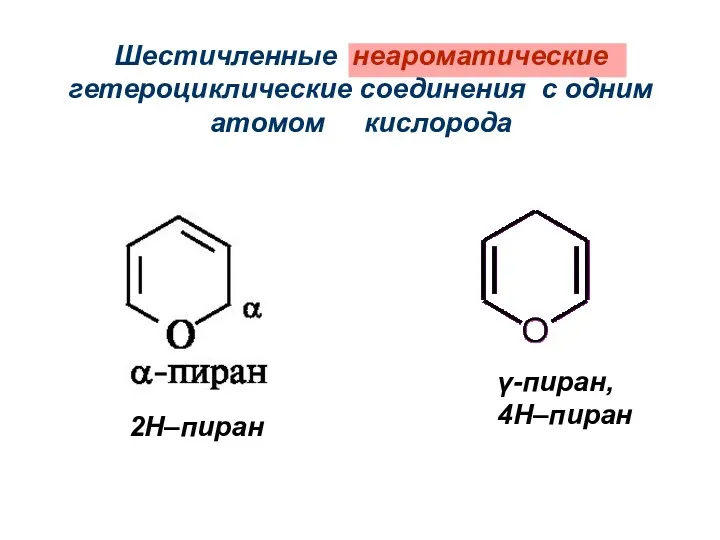
- 30. Шестичленные неароматические гетероциклические соединения с одним атомом кислорода 2Н–пиран γ-пиран, 4Н–пиран
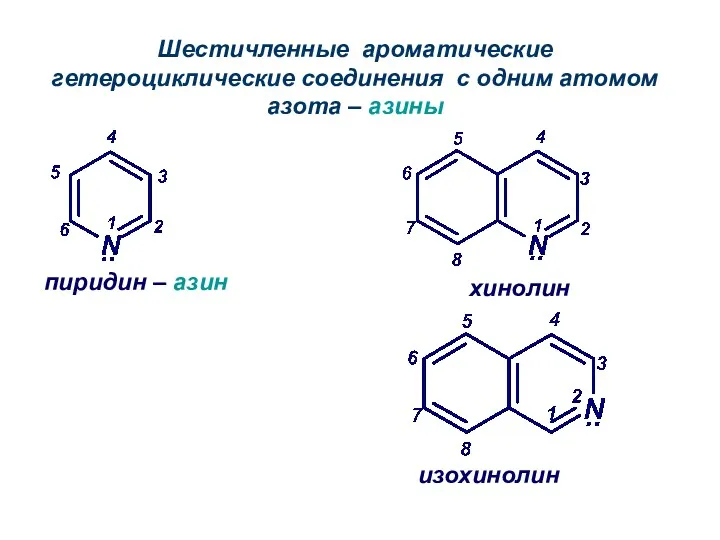
- 31. Шестичленные ароматические гетероциклические соединения с одним атомом азота – азины пиридин – азин хинолин изохинолин
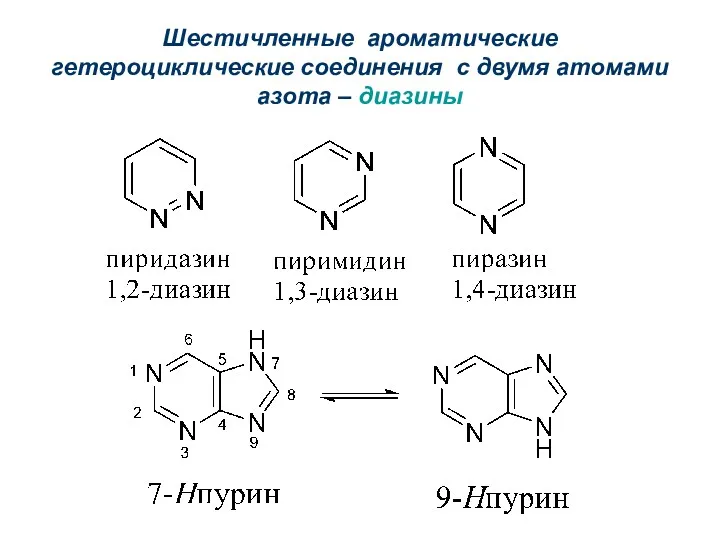
- 32. Шестичленные ароматические гетероциклические соединения с двумя атомами азота – диазины
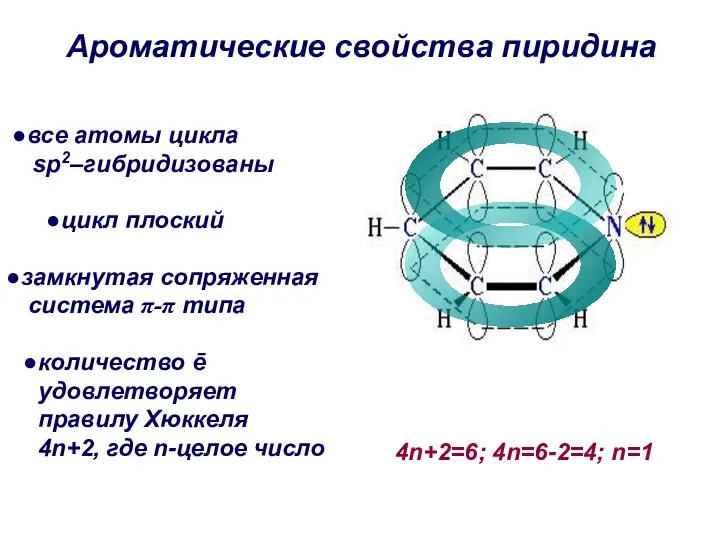
- 33. Ароматические свойства пиридина все атомы цикла sp2–гибридизованы цикл плоский замкнутая сопряженная система π-π типа количество ē
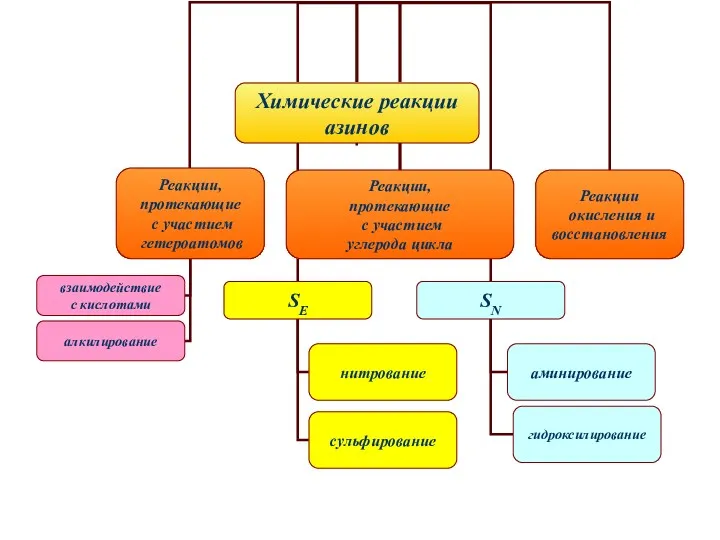
- 35. Реакции, протекающие с участием гетероатомов
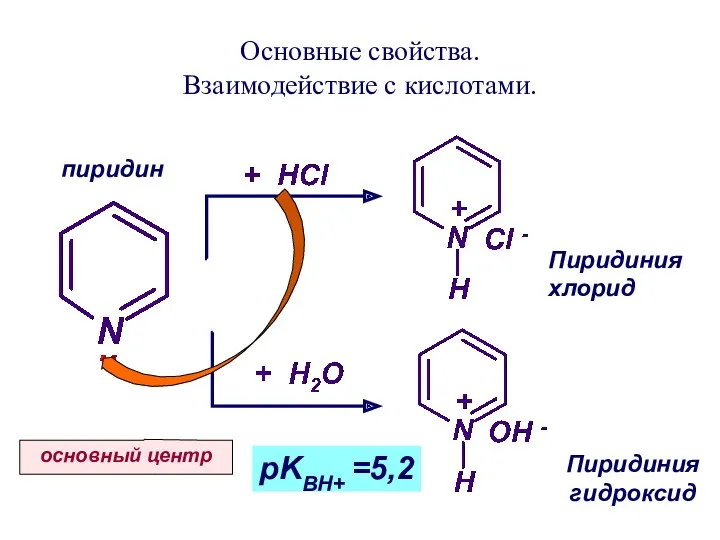
- 36. Основные свойства. Взаимодействие с кислотами. основный центр Пиридиния гидроксид Пиридиния хлорид пиридин pKBH+ =5,2
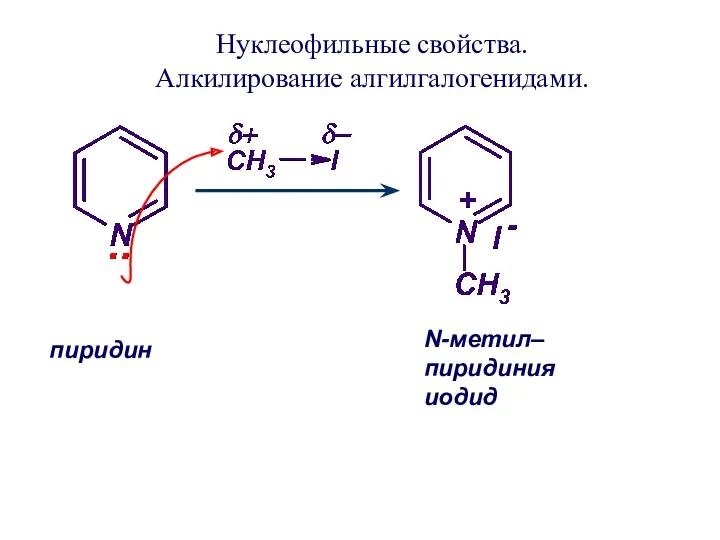
- 37. Нуклеофильные свойства. Алкилирование алгилгалогенидами. пиридин N-метил– пиридиния иодид
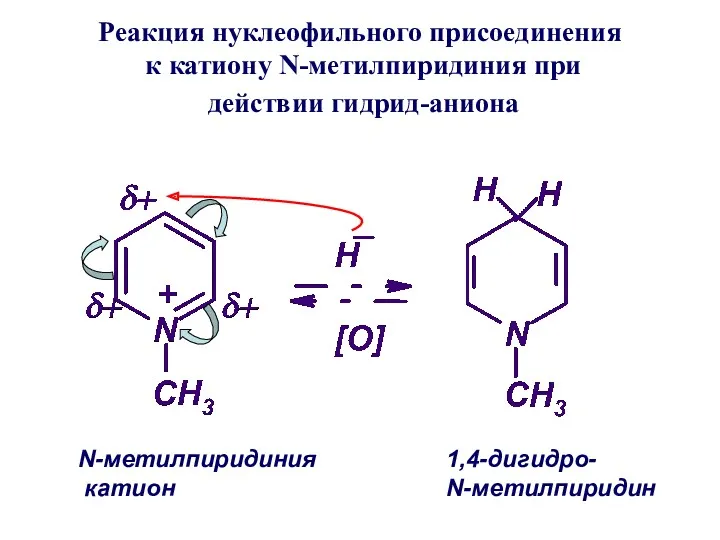
- 38. Реакция нуклеофильного присоединения к катиону N-метилпиридиния при действии гидрид-аниона N-метилпиридиния катион 1,4-дигидро- N-метилпиридин
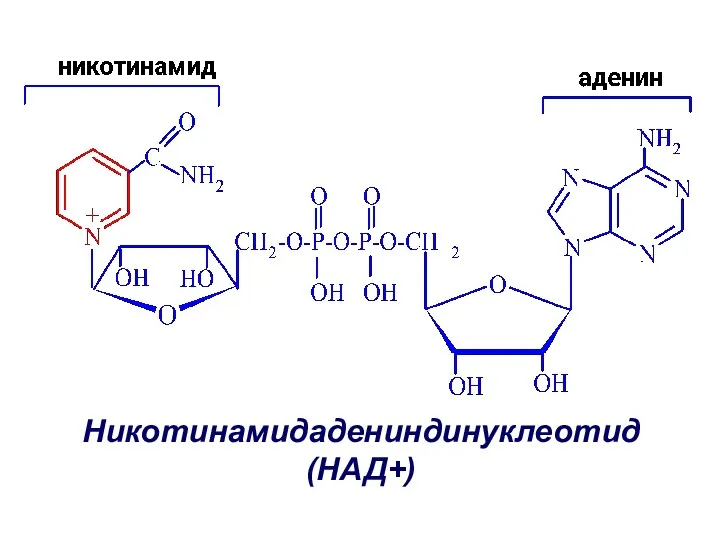
- 39. Никотинамидадениндинуклеотид (НАД+)
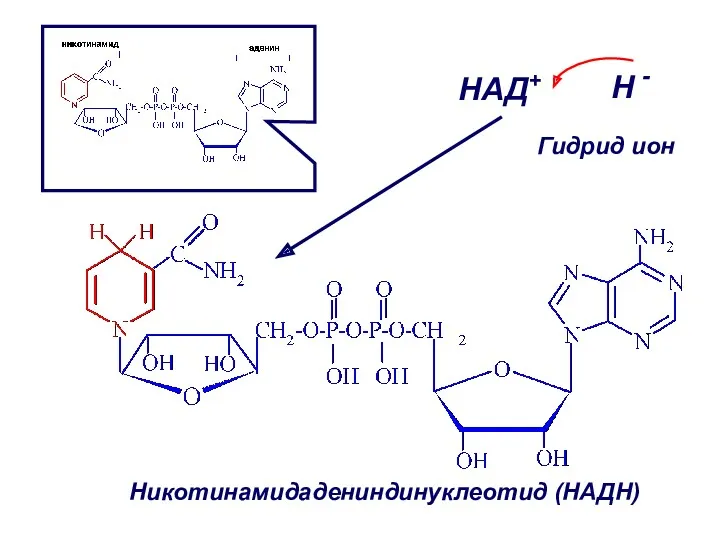
- 40. НАД+ H - Никотинамидадениндинуклеотид (НАДН) Гидрид ион
- 41. Реакции, протекающие с участием углерода цикла
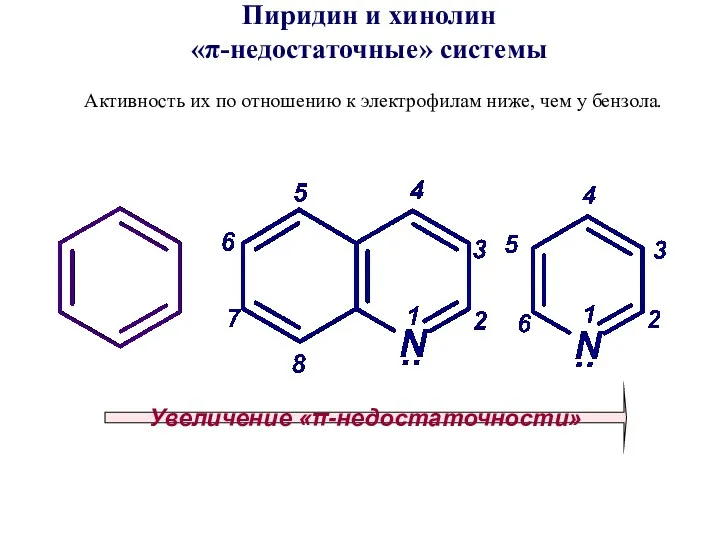
- 42. Пиридин и хинолин «π-недостаточные» системы Активность их по отношению к электрофилам ниже, чем у бензола. Увеличение
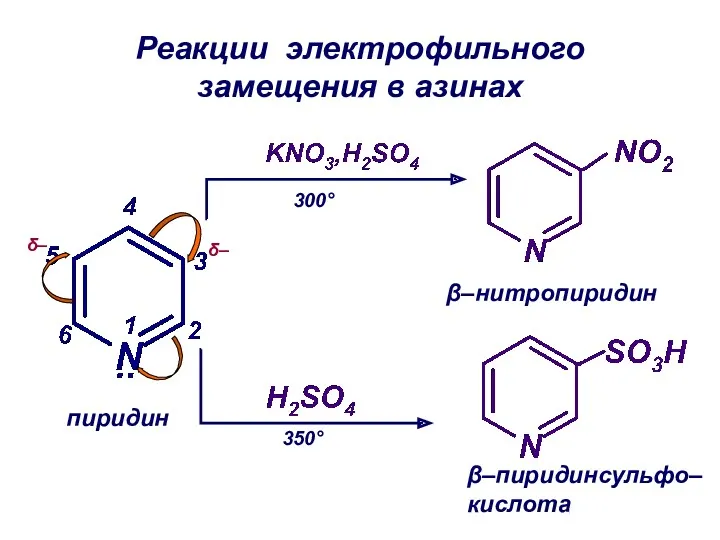
- 43. Реакции электрофильного замещения в азинах δ– δ– β–нитропиридин 300° 350° β–пиридинсульфо–кислота пиридин
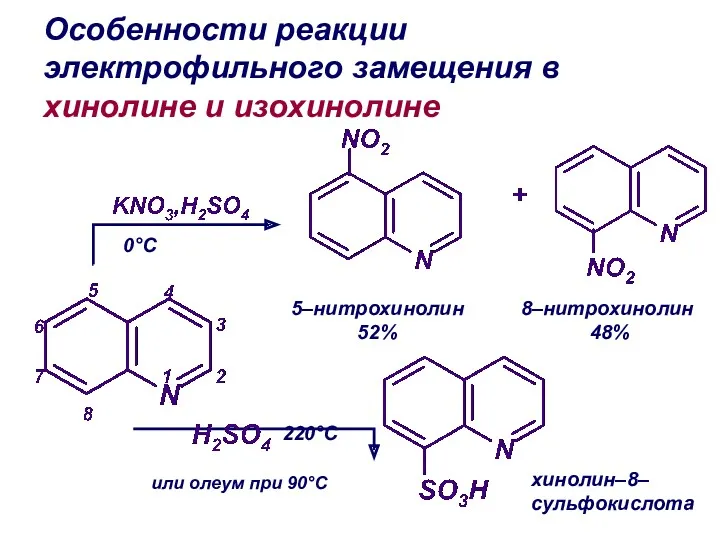
- 44. Особенности реакции электрофильного замещения в хинолине и изохинолине хинолин–8– сульфокислота 5–нитрохинолин 52% 8–нитрохинолин 48% 0°C 220°С
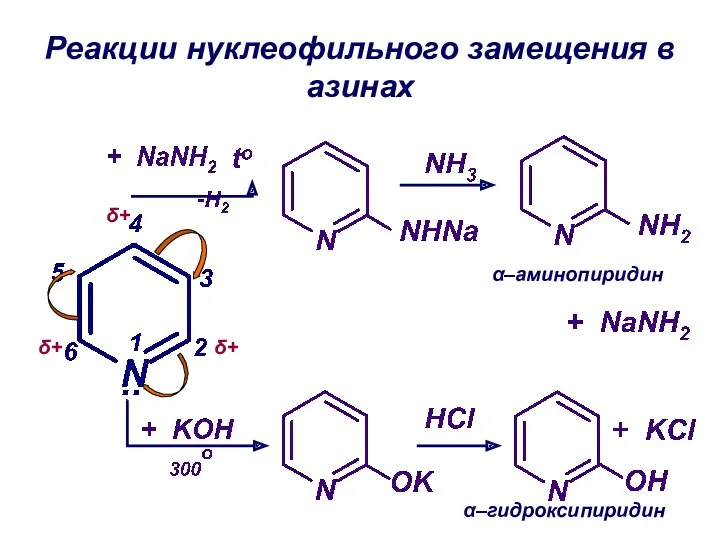
- 45. Реакции нуклеофильного замещения в азинах δ+ δ+ δ+ α–аминопиридин α–гидроксипиридин
- 46. Реакции окисления и восстановления
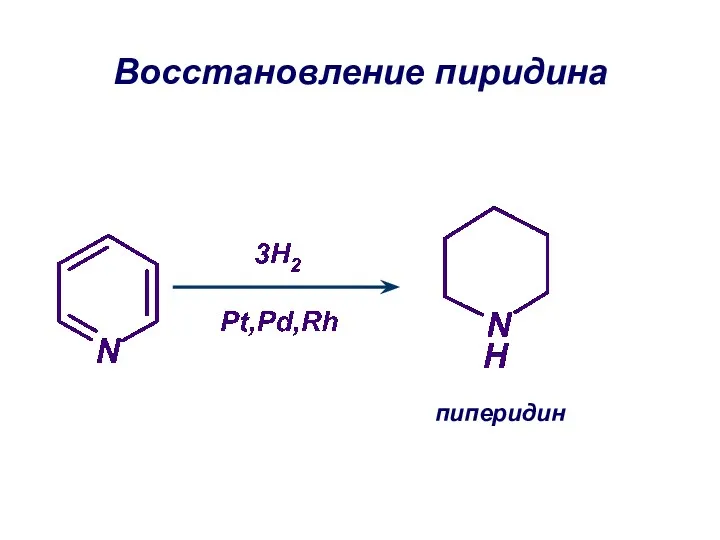
- 47. Восстановление пиридина пиперидин
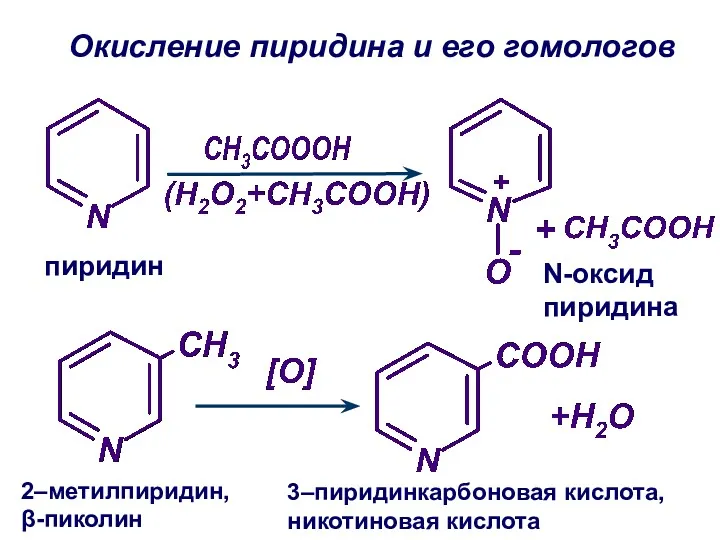
- 48. Окисление пиридина и его гомологов пиридин N-оксид пиридина 2–метилпиридин, β-пиколин 3–пиридинкарбоновая кислота, никотиновая кислота
- 49. Важнейшие представители шестичленных гетероциклов
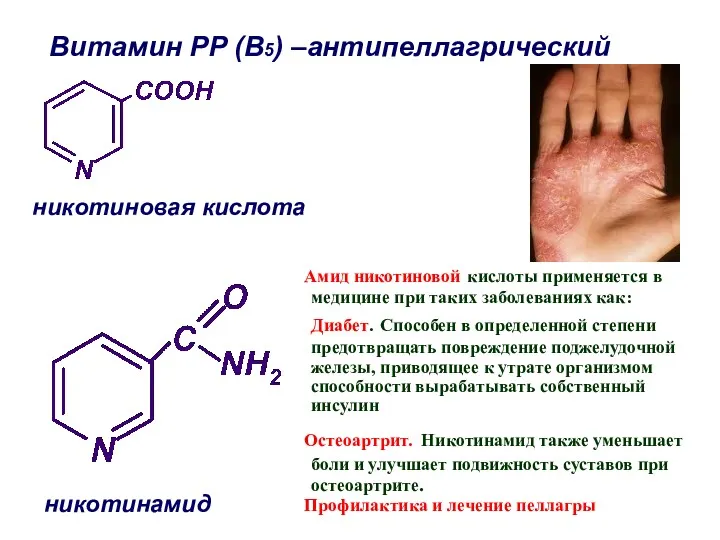
- 50. никотиновая кислота никотинамид Витамин РР (В5) –антипеллагрический Амид никотиновой кислоты применяется в медицине при таких заболеваниях
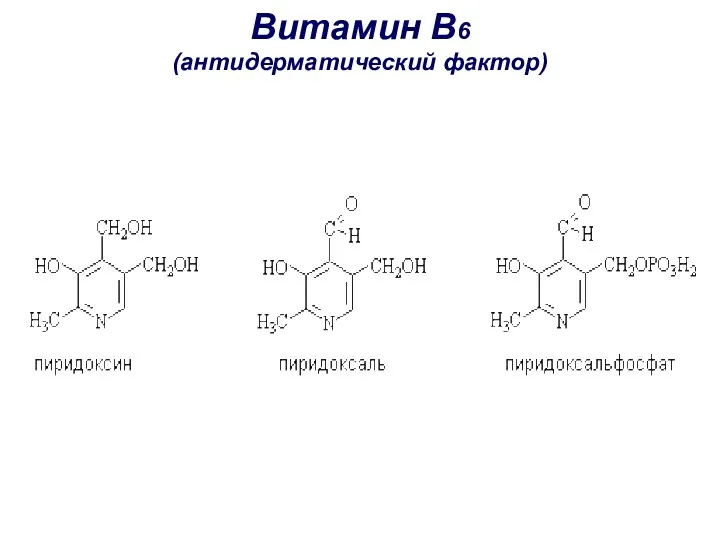
- 51. Витамин B6 (антидерматический фактор)
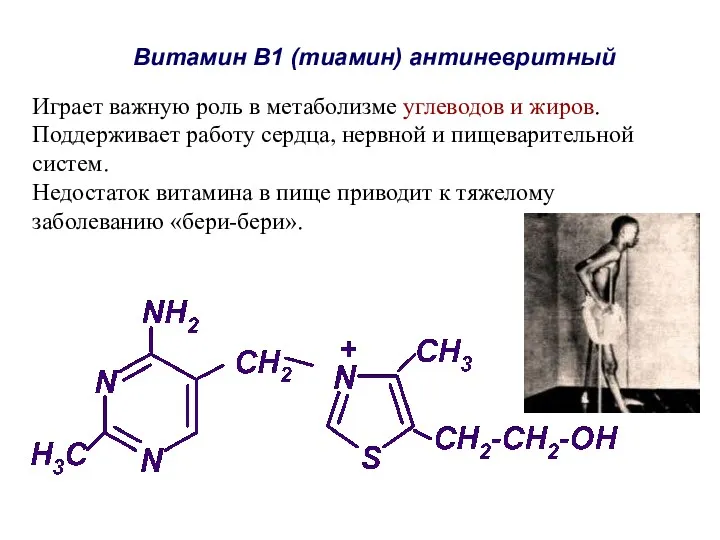
- 52. Витамин B1 (тиамин) антиневритный Играет важную роль в метаболизме углеводов и жиров. Поддерживает работу сердца, нервной
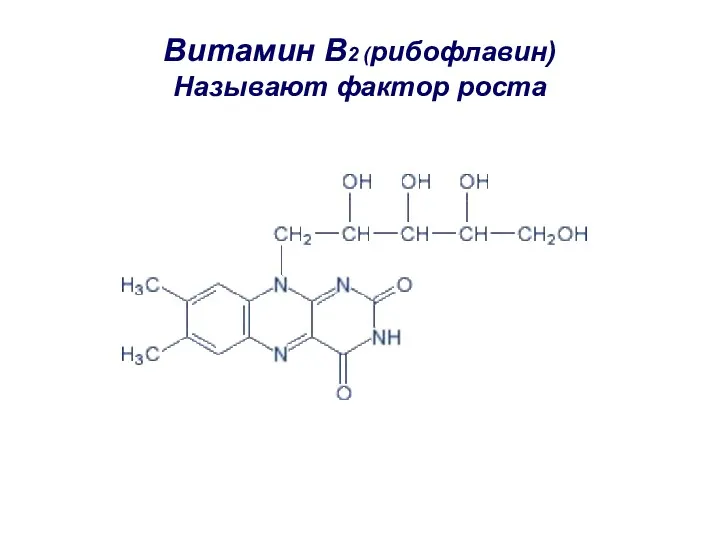
- 53. Витамин B2 (рибофлавин) Называют фактор роста
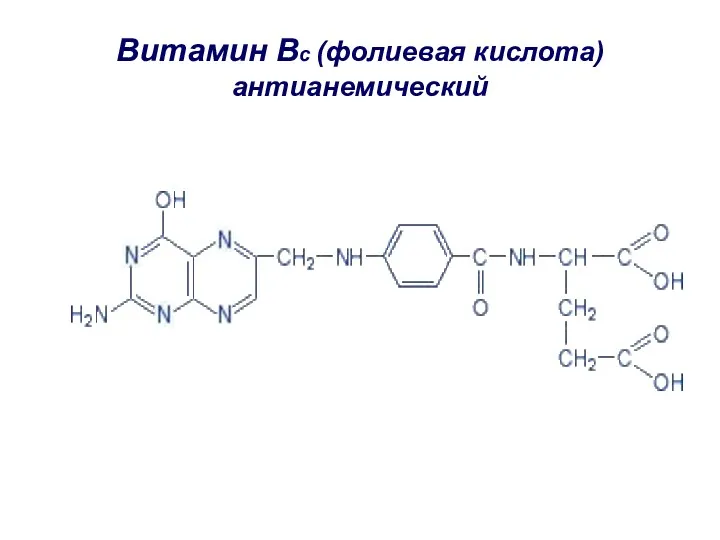
- 54. Витамин Bс (фолиевая кислота) антианемический
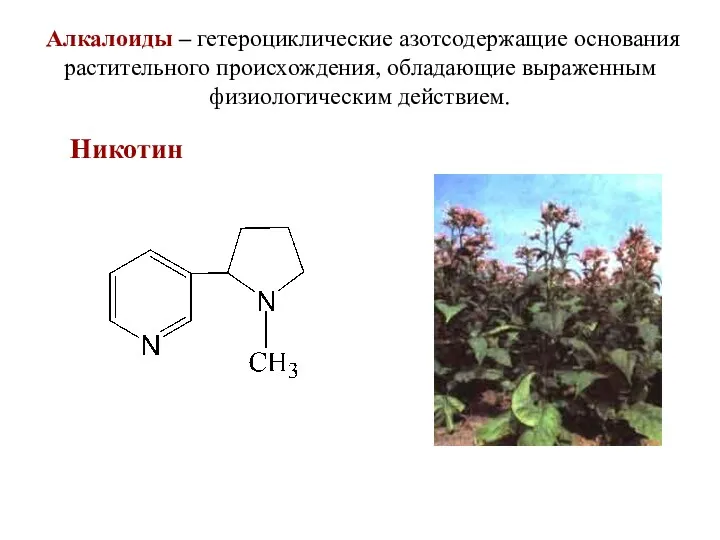
- 55. Алкалоиды – гетероциклические азотсодержащие основания растительного происхождения, обладающие выраженным физиологическим действием. Никотин
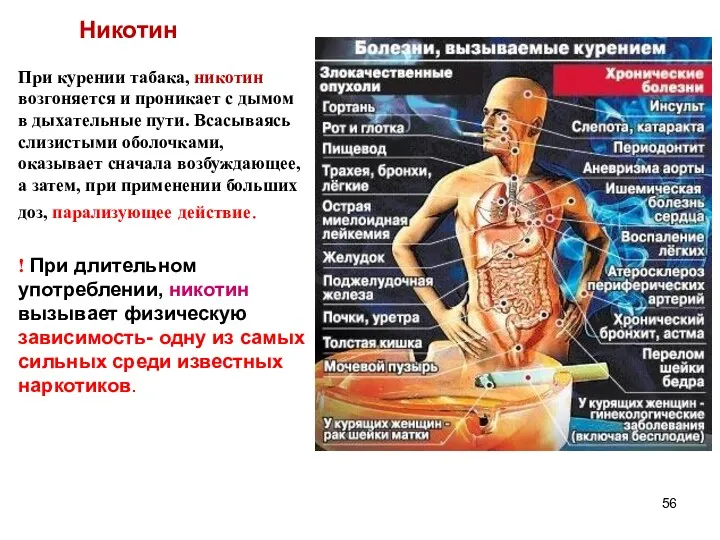
- 56. При курении табака, никотин возгоняется и проникает с дымом в дыхательные пути. Всасываясь слизистыми оболочками, оказывает
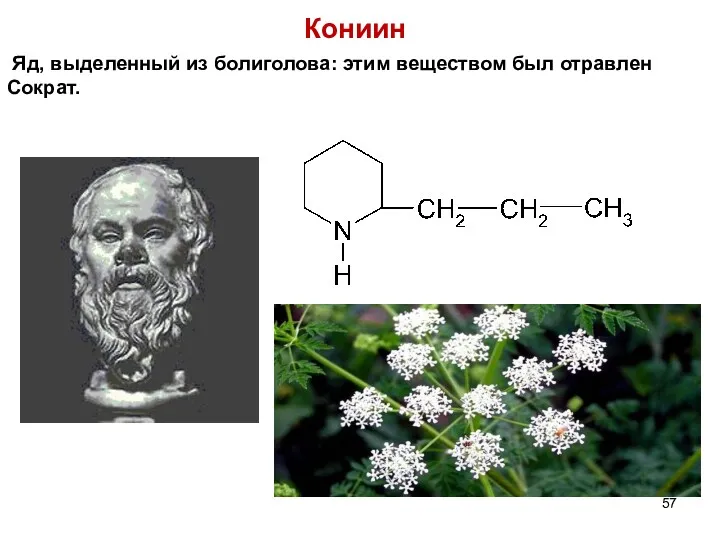
- 57. Кониин Яд, выделенный из болиголова: этим веществом был отравлен Сократ.
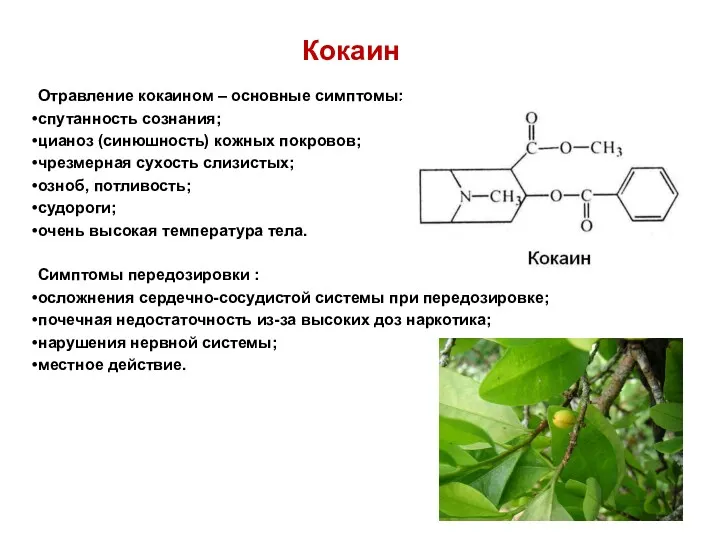
- 58. Кокаин Отравление кокаином – основные симптомы: спутанность сознания; цианоз (синюшность) кожных покровов; чрезмерная сухость слизистых; озноб,
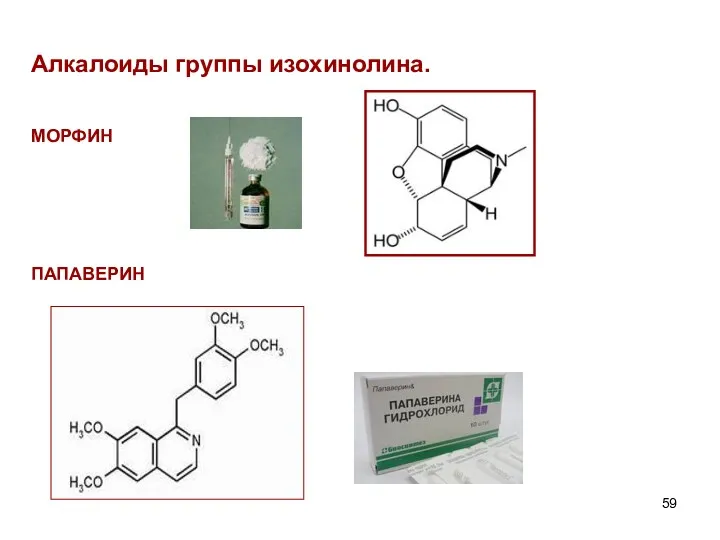
- 59. Алкалоиды группы изохинолина. МОРФИН ПАПАВЕРИН
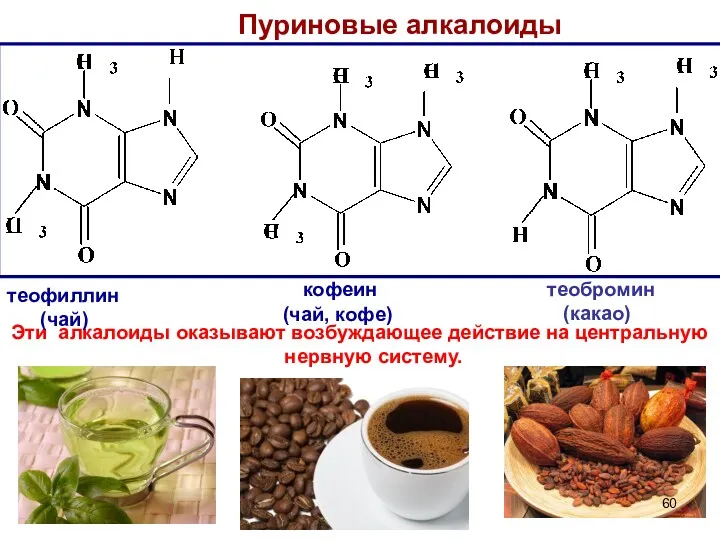
- 60. Пуриновые алкалоиды Эти алкалоиды оказывают возбуждающее действие на центральную нервную систему. теофиллин (чай) кофеин (чай, кофе)
- 61. Нуклеотиды. Нуклеиновые кислоты.
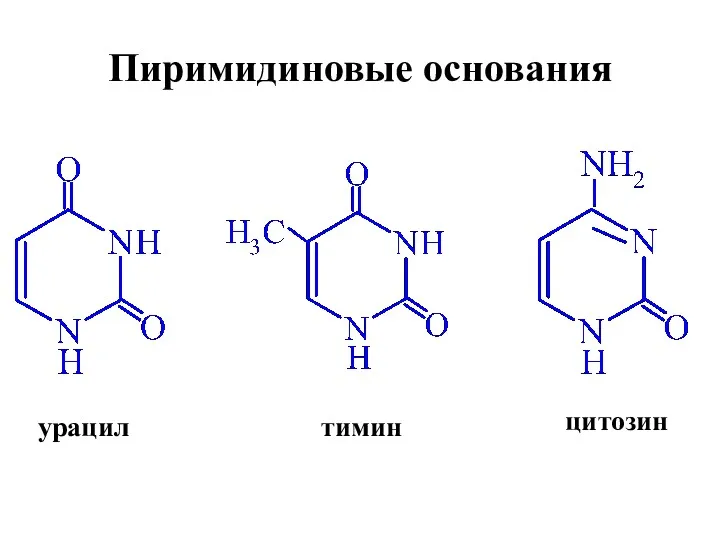
- 62. урацил тимин цитозин Пиримидиновые основания
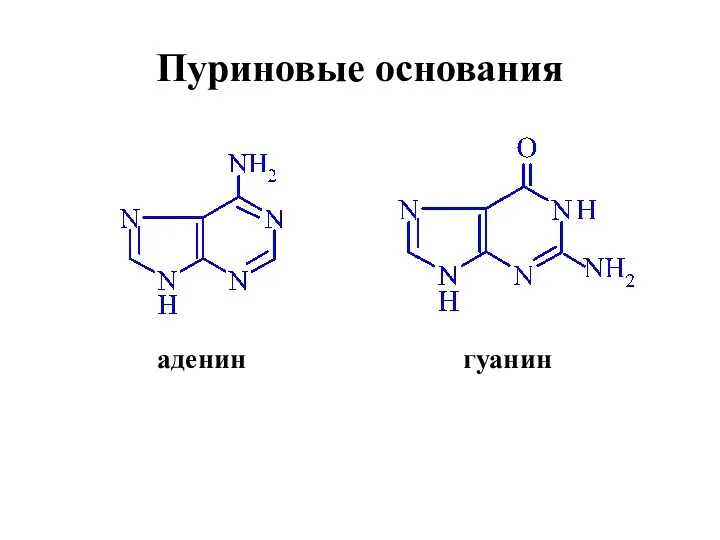
- 63. аденин гуанин Пуриновые основания
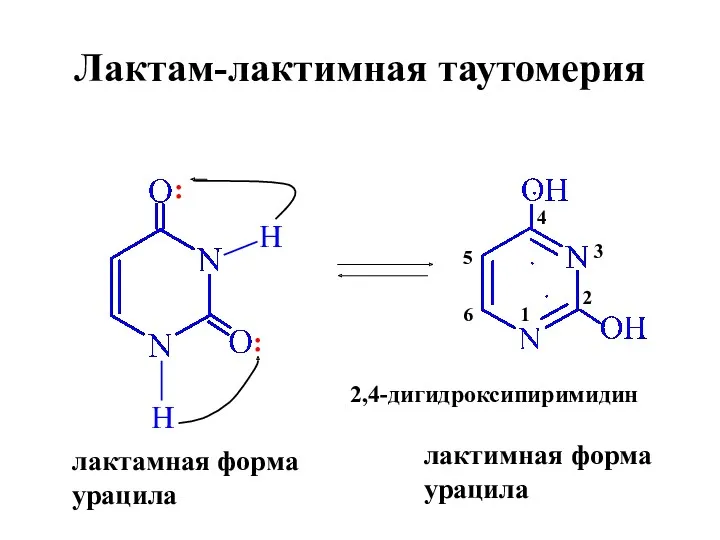
- 64. Лактам-лактимная таутомерия H H : : лактамная форма урацила лактимная форма урацила 2 1 3 4
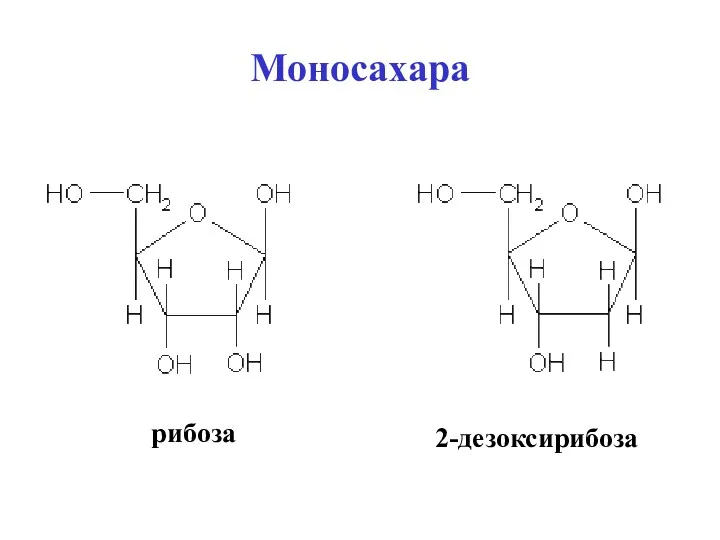
- 65. Моносахара рибоза 2-дезоксирибоза
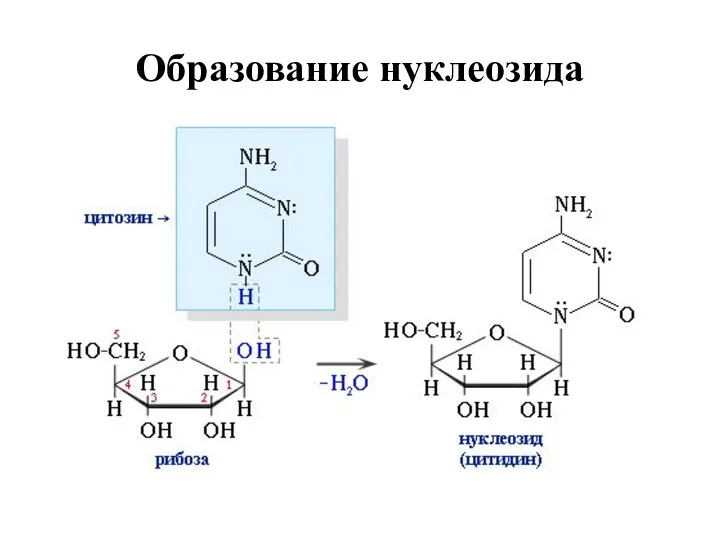
- 66. Образование нуклеозида
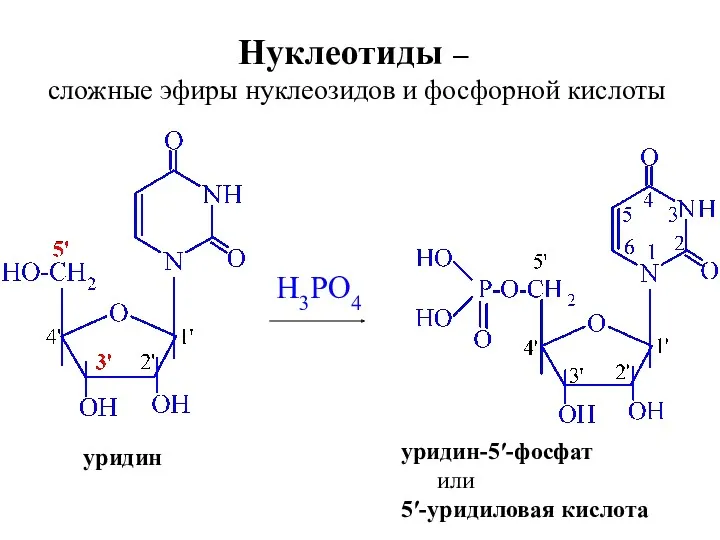
- 67. H3PO4 уридин уридин-5ʹ-фосфат или 5ʹ-уридиловая кислота Нуклеотиды – сложные эфиры нуклеозидов и фосфорной кислоты
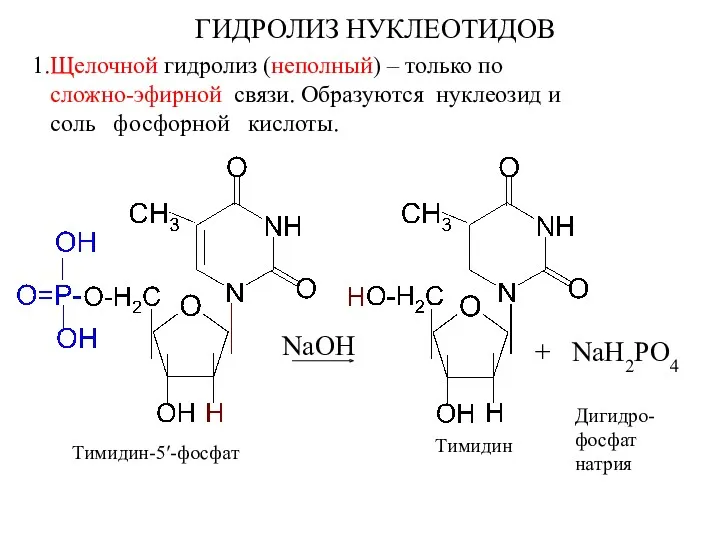
- 68. ГИДРОЛИЗ НУКЛЕОТИДОВ 1.Щелочной гидролиз (неполный) – только по сложно-эфирной связи. Образуются нуклеозид и соль фосфорной кислоты.
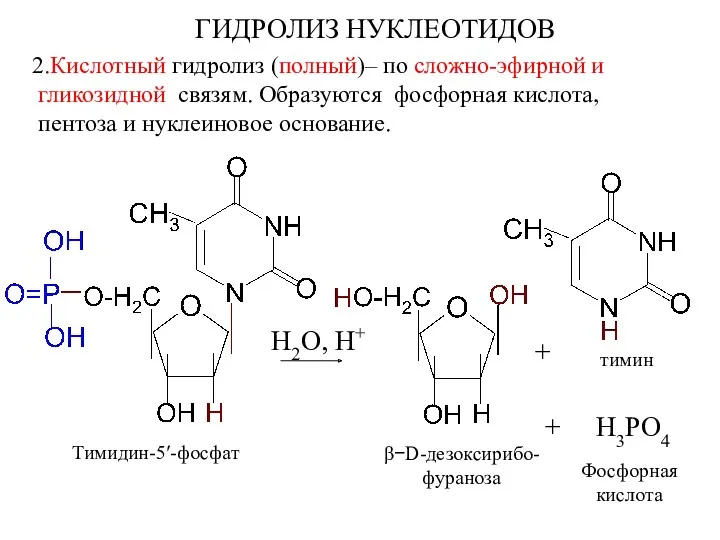
- 69. ГИДРОЛИЗ НУКЛЕОТИДОВ 2.Кислотный гидролиз (полный)– по сложно-эфирной и гликозидной связям. Образуются фосфорная кислота, пентоза и нуклеиновое
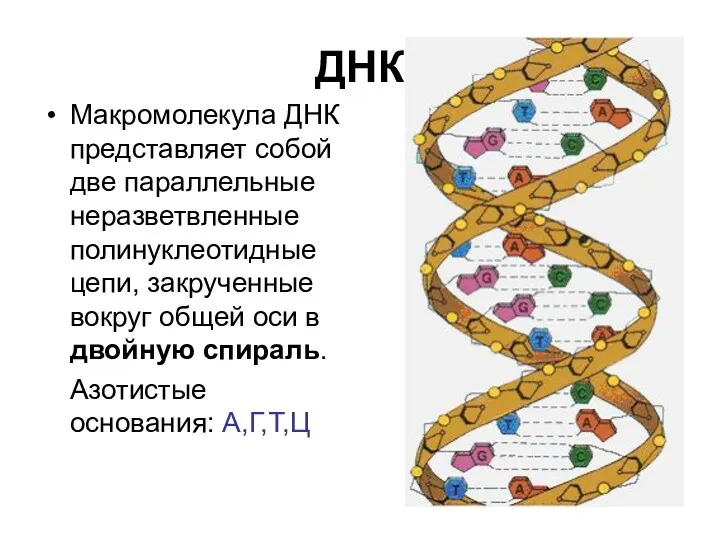
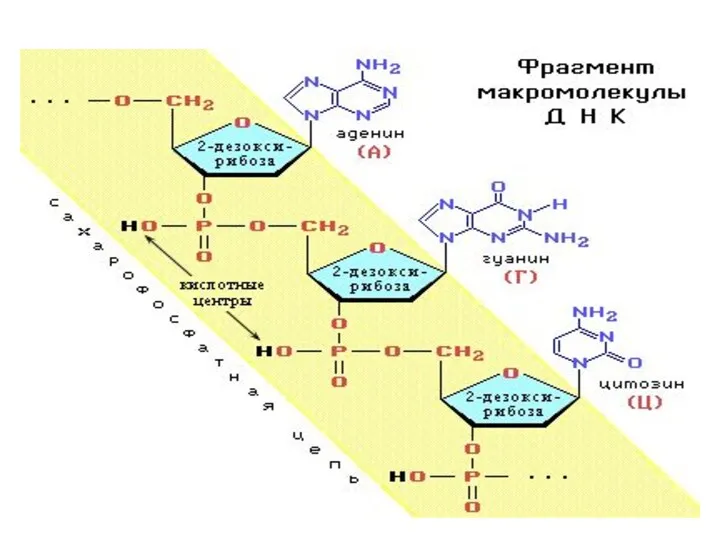
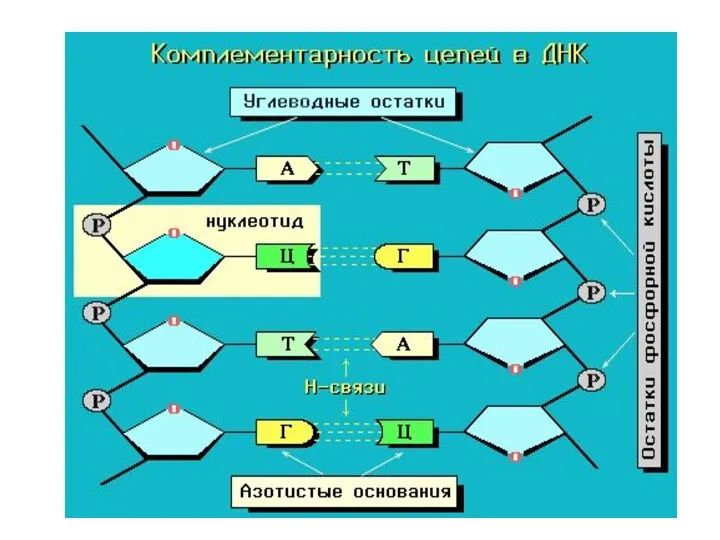
- 70. ДНК Макромолекула ДНК представляет собой две параллельные неразветвленные полинуклеотидные цепи, закрученные вокруг общей оси в двойную
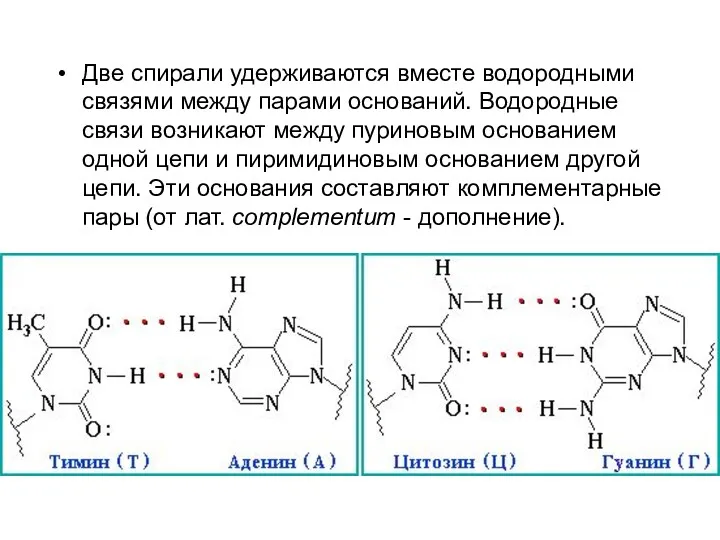
- 72. Две спирали удерживаются вместе водородными связями между парами оснований. Водородные связи возникают между пуриновым основанием одной
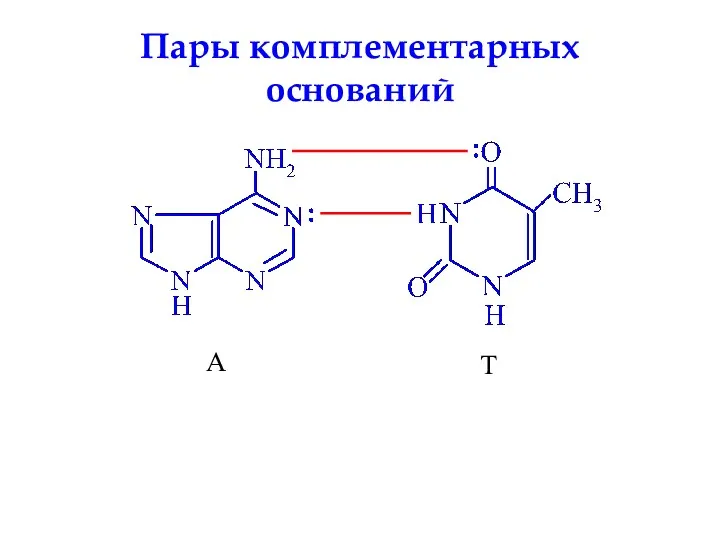
- 73. А Т Пары комплементарных оснований
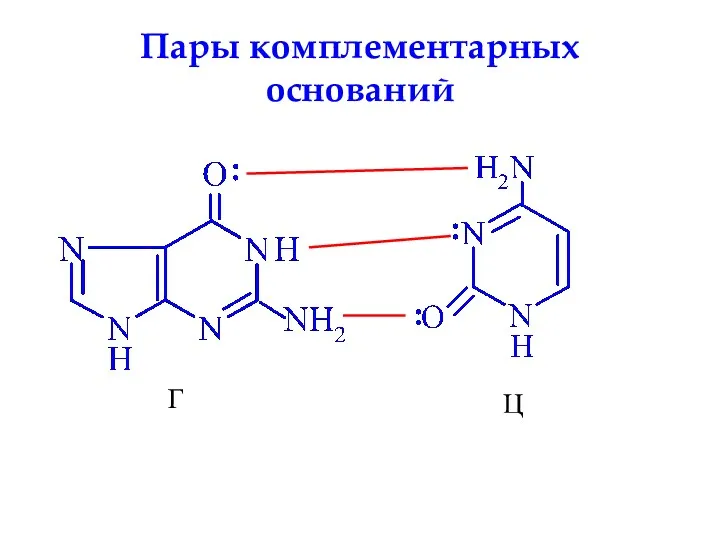
- 74. Пары комплементарных оснований Г Ц
- 76. РНК молекулы РНК состоят из одной полинуклеотидной цепи. Азотистые основания: А,Г,У,Ц Пары комплементарных оснований А –У
- 77. Виды РНК Транспортная (т-РНК) (10% всей РНК клетки) Функция: перенос аминокислоты к месту синтеза белка 2.
- 79. Скачать презентацию







 Морщины как признак старения кожи
Морщины как признак старения кожи Класс Птицы. Внешнее строение сизого голубя
Класс Птицы. Внешнее строение сизого голубя Биохимическая эволюция
Биохимическая эволюция Размножение. Начало новой жизни
Размножение. Начало новой жизни Строение и значение нервной системы
Строение и значение нервной системы Раціональне харчування
Раціональне харчування Мочевыделительная система Предупреждение заболеваний почек. Питьевой режим. 8 класс
Мочевыделительная система Предупреждение заболеваний почек. Питьевой режим. 8 класс ПрезентацияФормула здоровья
ПрезентацияФормула здоровья Закон гомологических рядов в наследственной изменчивости
Закон гомологических рядов в наследственной изменчивости Особенности кровоснабжения головы и шеи
Особенности кровоснабжения головы и шеи Эволюция (1 часть)
Эволюция (1 часть) Развитие жизни на земле
Развитие жизни на земле Орхидеи
Орхидеи Вегетативная нервная система
Вегетативная нервная система осн физ особ у детей-1
осн физ особ у детей-1 Пресс-обзор. Детские журналы о природе
Пресс-обзор. Детские журналы о природе ПРЕЗЕНТАЦИИ 5 КЛАСС 4 ЧЕТВЕРТЬ
ПРЕЗЕНТАЦИИ 5 КЛАСС 4 ЧЕТВЕРТЬ Sotsialno-biol_osnovy_fiz_kultury_1_-2_kurs
Sotsialno-biol_osnovy_fiz_kultury_1_-2_kurs Красная книга России. Растения
Красная книга России. Растения Молекулярные основы наследственности
Молекулярные основы наследственности Тип хордовые
Тип хордовые Жұмыр құрттар
Жұмыр құрттар Физиология бактерий. Метаболизм микробной клетки. Рост. Размножение
Физиология бактерий. Метаболизм микробной клетки. Рост. Размножение klasss
klasss Механізми імунних реакцій організму людини. Алергія. СНІД та його профілактика
Механізми імунних реакцій організму людини. Алергія. СНІД та його профілактика Биотические взаимоотношения популяций в экосистемах
Биотические взаимоотношения популяций в экосистемах Ультразвук в природе
Ультразвук в природе презентацияЗагрязнение воздуха
презентацияЗагрязнение воздуха