Содержание
- 2. Совокупность окислительных реакций, происходящих в биологических объектах и обеспечивающих их энергией и метаболитами для осуществления процессов
- 3. ФУНКЦИИ БИОЛОГИЧЕСКОГО ОКИСЛЕНИЯ Энергетическое обеспечение: а) поддержания температуры тела; б) биолюминесценции (свечения); в) химических синтезов; г)
- 4. ФЕРМЕНТЫ БИОЛОГИЧЕСКОГО ОКИСЛЕНИЯ Разнообразные реакции биологического окисления ускоряются многочисленными ферментами оксидоредуктазами, которые, как правило, встроены в
- 5. ФЕРМЕНТЫ БИОЛОГИЧЕСКОГО ОКИСЛЕНИЯ Аэробные дегидрогеназы (в отличие от оксидаз они могут использовать в качестве акцептора водорода
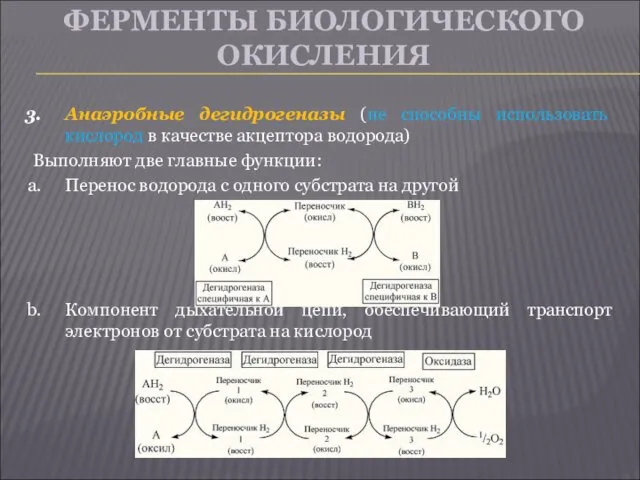
- 6. ФЕРМЕНТЫ БИОЛОГИЧЕСКОГО ОКИСЛЕНИЯ Анаэробные дегидрогеназы (не способны использовать кислород в качестве акцептора водорода) Выполняют две главные
- 7. ФЕРМЕНТЫ БИОЛОГИЧЕСКОГО ОКИСЛЕНИЯ Гидроксипероксидазы (используют в качестве субстрата перекись водорода или органические перекиси) Оксигеназы (катализируют прямое
- 8. ТИПЫ БИОЛОГИЧЕСКОГО ОКИСЛЕНИЯ Существуют 2 типа биологического окисления: Свободное окисление Окисление, не сопряженное с фосфорилированием АДФ
- 9. Свободное окисление
- 10. СВОБОДНОЕ ОКИСЛЕНИЕ Реакции свободного окисления органических соединений в живой природе и ускоряющие их ферментные системы многообразны.
- 11. ОСОБЕННОСТИ МИКРОСОМАЛЬНОЙ ДЫХАТЕЛЬНОЙ ЦЕПИ 1) Несмотря на наличие ферментов цепи переноса электронов, ни в одном пункте
- 12. ФЕРМЕНТЫ СВОБОДНОГО ОКИСЛЕНИЯ
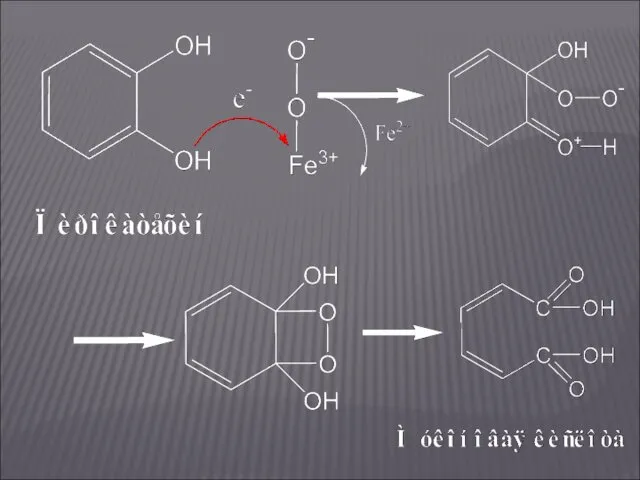
- 13. ПРИМЕРЫ ДИОКСИГЕНАЗНЫХ РЕАКЦИЙ Пирокатехаза (катехол: кислород-1,2-оксидоредуктаза дециклизующая) Она содержит в активном центре два прочно связанных атома
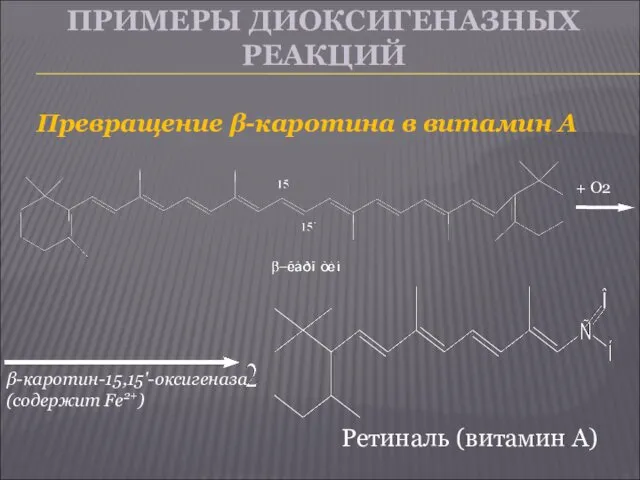
- 15. ПРИМЕРЫ ДИОКСИГЕНАЗНЫХ РЕАКЦИЙ Превращение β-каротина в витамин А + О2 β-каротин-15,15'-оксигеназа (содержит Fe2+) Ретиналь (витамин А)
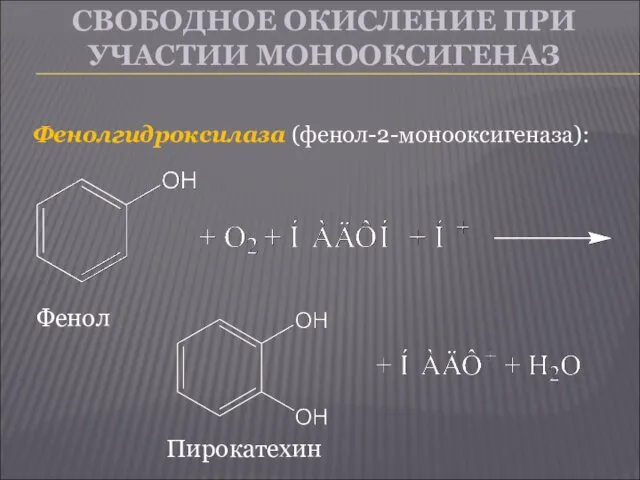
- 16. СВОБОДНОЕ ОКИСЛЕНИЕ ПРИ УЧАСТИИ МОНООКСИГЕНАЗ Фенолгидроксилаза (фенол-2-монооксигеназа): Фенол Пирокатехин
- 17. Окисление, сопряженное с фосфорилированием АДФ
- 19. Субстратное фосфорилирование
- 20. Субстратное фосфорилирование – такой вид биологического окисления, при котором: макроэргическая связь возникает в момент непосредственного окисления
- 21. ПРИМЕРЫ РЕАКЦИЙ СУБСТРАТНОГО ФОСФОРИЛИРОВАНИЯ При окислении 3-фосфоглицеринового альдегида (3-ФГА) в 2-фосфоглицериновую кислоту (2-ФГК) – гликолиз; При
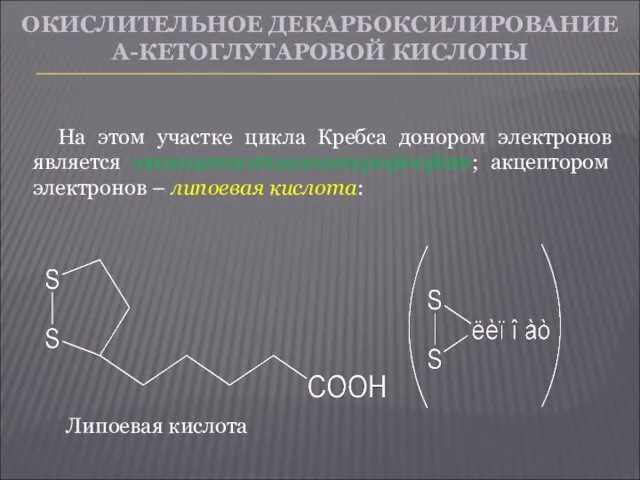
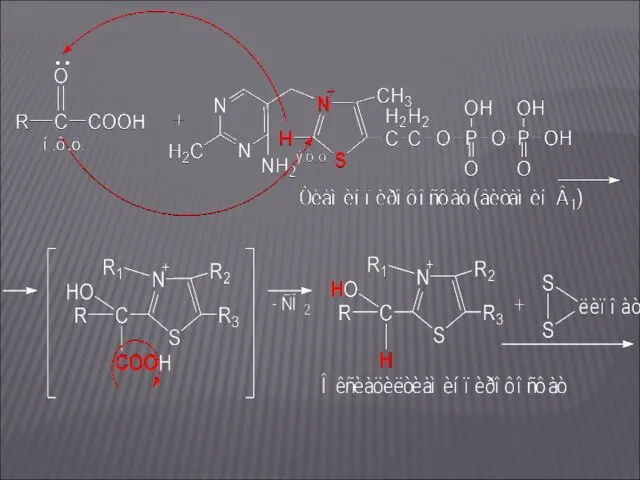
- 22. ОКИСЛИТЕЛЬНОЕ ДЕКАРБОКСИЛИРОВАНИЕ Α-КЕТОГЛУТАРОВОЙ КИСЛОТЫ На этом участке цикла Кребса донором электронов является оксиацетилтиаминпирофосфат; акцептором электронов –
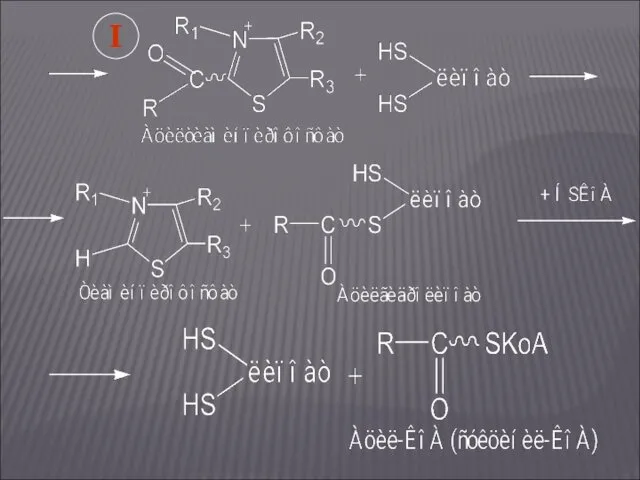
- 24. I
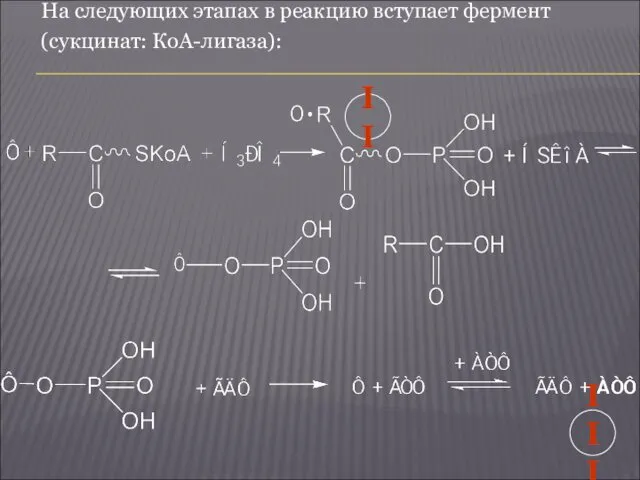
- 25. На следующих этапах в реакцию вступает фермент (сукцинат: КоА-лигаза): II III
- 26. Окислительное фосфорилирование
- 27. ОКИСЛИТЕЛЬНОЕ ФОСФОРИЛИРОВАНИЕ Это сопряжение окисления с синтезом АТФ, когда атомы водорода с коферментов дегидрогеназ, принимающих участие
- 28. Окислительно- восстановительные ферменты
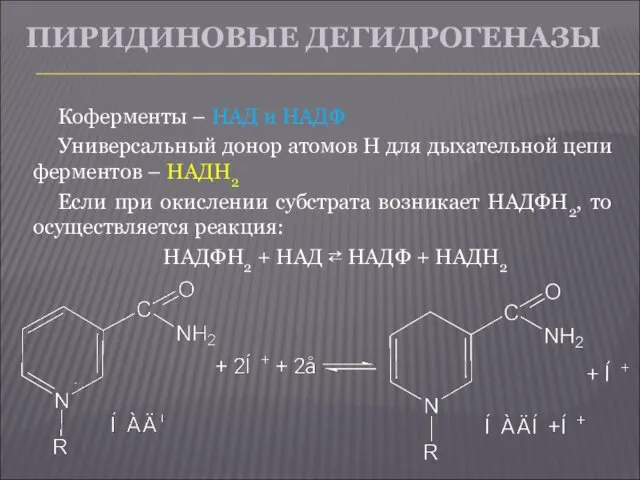
- 29. ПИРИДИНОВЫЕ ДЕГИДРОГЕНАЗЫ Коферменты – НАД и НАДФ Универсальный донор атомов Н для дыхательной цепи ферментов –
- 30. ОСОБЕННОСТИ РЕАКЦИЙ С УЧАСТИЕМ ПИРИДИНОВЫХ ДЕГИДРОГЕНАЗ Легкая обратимость. Коферменты легко отделяются от белковой части, обладают высокой
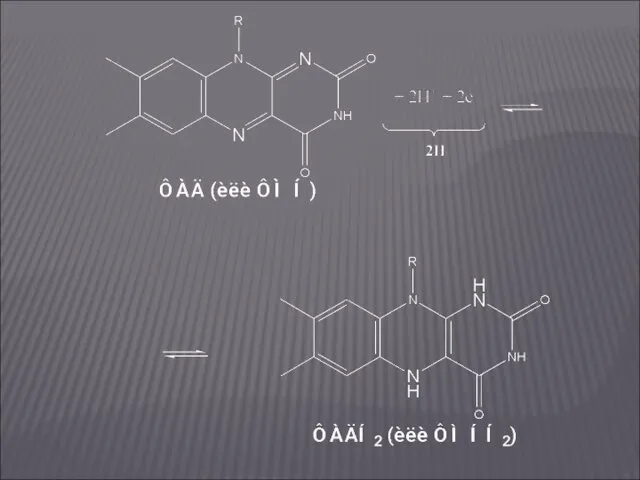
- 31. ФЛАВИНОВЫЕ ДЕГИДРОГЕНАЗЫ Коферменты – ФМН и ФАД. Флавиновые ферменты являются акцепторами атомов водорода и осуществляют перенос
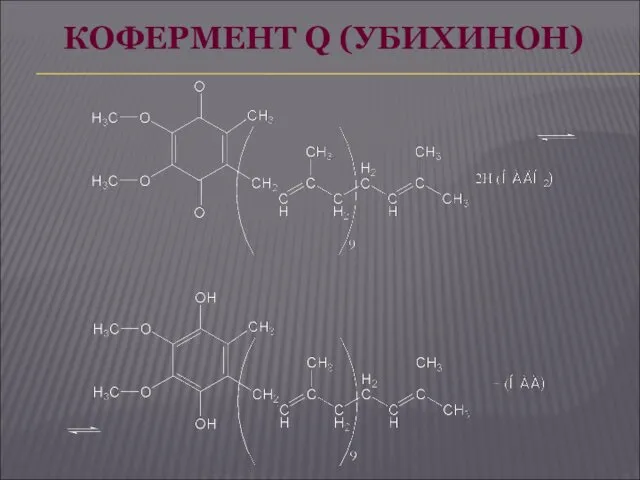
- 33. КОФЕРМЕНТ Q (УБИХИНОН)
- 34. ЦИТОХРОМЫ Дальнейший перенос электронов от КоQ на кислород осуществляет система цитохромов, состоящая из ряда гемопротеидов, расположенных
- 35. Схема дыхательной цепи
- 36. Самой примечательной особенностью дыхательной цепи ферментов является наличие в ней участков, где соседние компоненты резко отличаются
- 37. ХЕМИОСМОТИЧЕСКАЯ ГИПОТЕЗА Питер Митчелл, Владимир Петрович Скулачев Реакции, сопровождающиеся расходованием или образованием Н+, протекают на внутренней
- 39. Скачать презентацию
























 Генетические аспекты спортивного отбора
Генетические аспекты спортивного отбора АТФ и другие органические соединения клетки
АТФ и другие органические соединения клетки Вторичный метаболизм высших растений. Алкалоиды. Часть 1
Вторичный метаболизм высших растений. Алкалоиды. Часть 1 Класс Млекопитающие или Звери. Отряды: Однопроходные, Сумчатые, Насекомоядные, Рукокрылые
Класс Млекопитающие или Звери. Отряды: Однопроходные, Сумчатые, Насекомоядные, Рукокрылые Происхождение современного человека. (Тема 3)
Происхождение современного человека. (Тема 3) Механизмы старения и его профилактика
Механизмы старения и его профилактика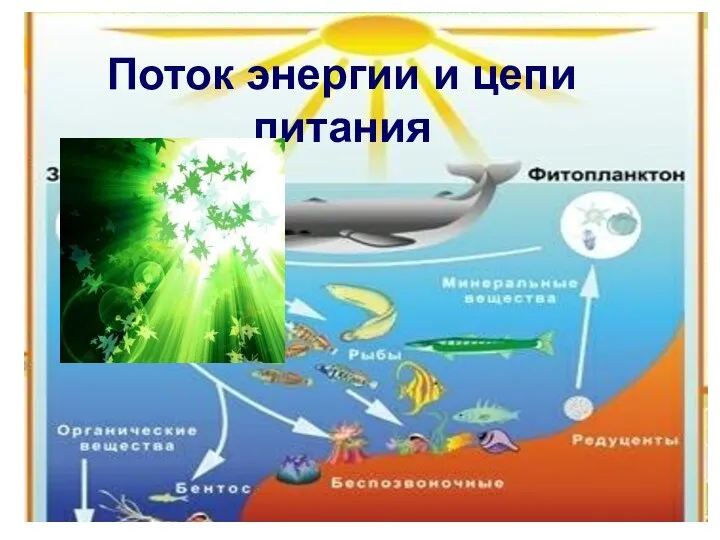 Поток энергии и цепи питания
Поток энергии и цепи питания Бактериология. Классификация бактерий. Морфология бактерий и методы её изучения. (Лекция 9)
Бактериология. Классификация бактерий. Морфология бактерий и методы её изучения. (Лекция 9) Материальные основы наследственности
Материальные основы наследственности Свойства ферментов. Механизм действия. Лекция 2
Свойства ферментов. Механизм действия. Лекция 2 Растения Мотовилихинского пруда
Растения Мотовилихинского пруда Структурная организация белка
Структурная организация белка Сообщество, экосистема, биогеоценоз
Сообщество, экосистема, биогеоценоз Биофизика фоторецепции
Биофизика фоторецепции Грибы, одно из царств живых организмов (ранее относились к низшим растениям)
Грибы, одно из царств живых организмов (ранее относились к низшим растениям) 373acb0e4cd14e079a5c6c48d3803fbf
373acb0e4cd14e079a5c6c48d3803fbf Строение и физиология слуховой системы человека
Строение и физиология слуховой системы человека песчаная эфа
песчаная эфа Биология клетки
Биология клетки Ферменты в генетической инженерии. Тема 2
Ферменты в генетической инженерии. Тема 2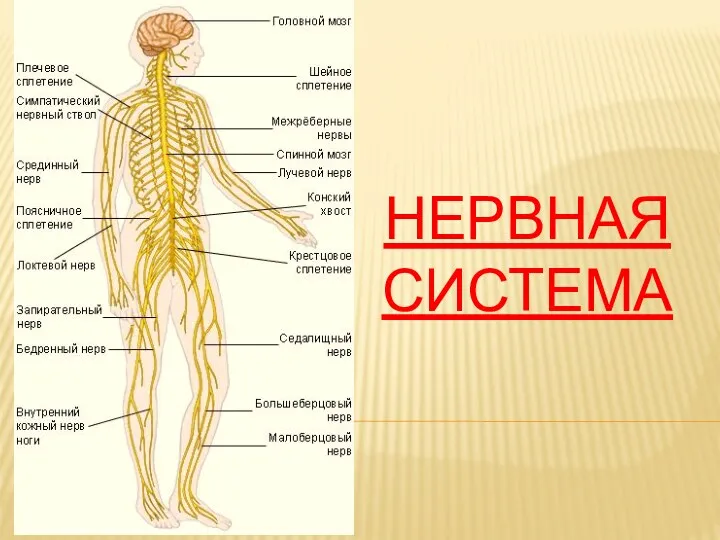 Нервная система
Нервная система Презентация к уроку биологии с использованием модульных технологий по теме Органические вещества клетки. нуклеиновые кислоты.
Презентация к уроку биологии с использованием модульных технологий по теме Органические вещества клетки. нуклеиновые кислоты. Основные взаимосвязи в организме, образующиеся при мышечной деятельности. Тема 1
Основные взаимосвязи в организме, образующиеся при мышечной деятельности. Тема 1 Выращивание кактуса в домашних условиях
Выращивание кактуса в домашних условиях Царство животные
Царство животные Чудо-доктора. Лекарственные растения Лутугинского района
Чудо-доктора. Лекарственные растения Лутугинского района Органогенез. Постэмбриональное развитие.
Органогенез. Постэмбриональное развитие. Биохимия нервной ткани. Биологические мембраны
Биохимия нервной ткани. Биологические мембраны