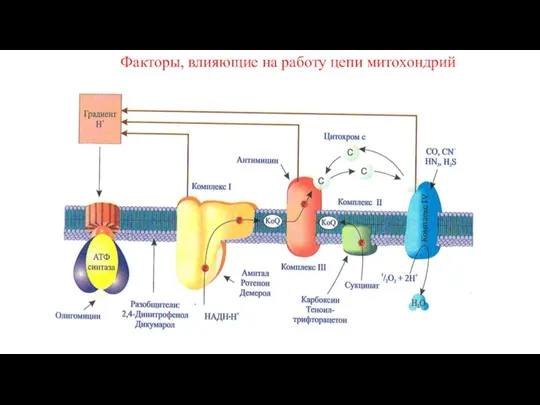
Внутренняя мембрана митохондрий
матрикс
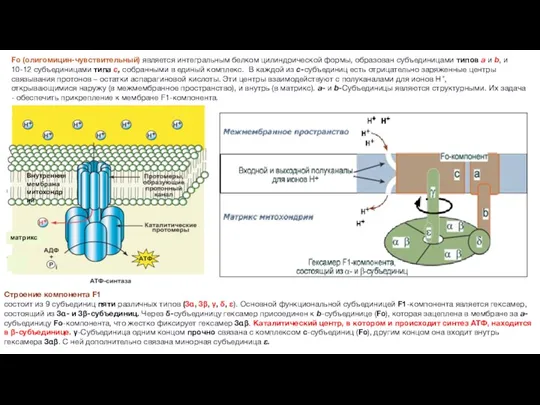
Строение компонента F1
состоит из 9 субъединиц пяти различных типов (3α, 3β, γ,
δ, ε). Основной функциональной субъединицей F1-компонента является гексамер, состоящий из 3α- и 3β-субъединиц. Через δ-субъединицу гексамер присоединен к b-субъединице (Fo), которая зацеплена в мембране за a-субъединицу Fo-компонента, что жестко фиксирует гексамер 3αβ. Каталитический центр, в котором и происходит синтез АТФ, находится в β-субъединице. γ-Субъединица одним концом прочно связана с комплексом c-субъединиц (Fo), другим концом она входит внутрь гексамера 3αβ. С ней дополнительно связана минорная субъединица ε.
Fо (олигомицин-чувствительный) является интегральным белком цилиндрической формы, образован субъединицами типов a и b, и 10-12 субъединицами типа с, собранными в единый комплекс. В каждой из c-субъединиц есть отрицательно заряженные центры связывания протонов – остатки аспарагиновой кислоты. Эти центры взаимодействуют с полуканалами для ионов H+, открывающимися наружу (в межмембранное пространство), и внутрь (в матрикс). a- и b-Субъединицы являются структурными. Их задача - обеспечить прикрепление к мембране F1-компонента.







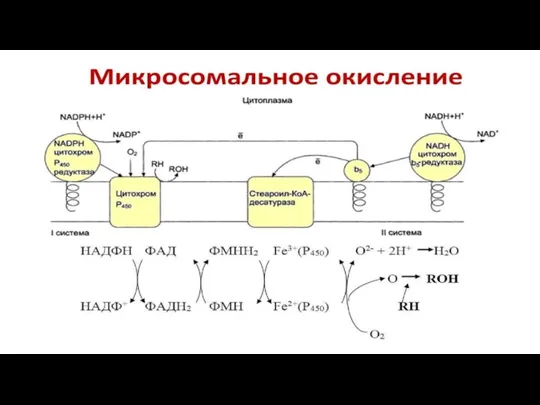
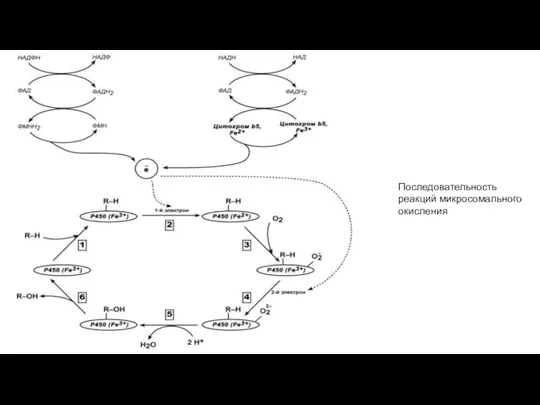



 Терморегуляция
Терморегуляция Растения леса
Растения леса Есте сақтау қабілетінің биохимиялық механизмі
Есте сақтау қабілетінің биохимиялық механизмі Бактерии. Группы настоящих бактерий
Бактерии. Группы настоящих бактерий Задания ОГЭ по биологии по теме Размножение организмов.
Задания ОГЭ по биологии по теме Размножение организмов. Угольная рыба
Угольная рыба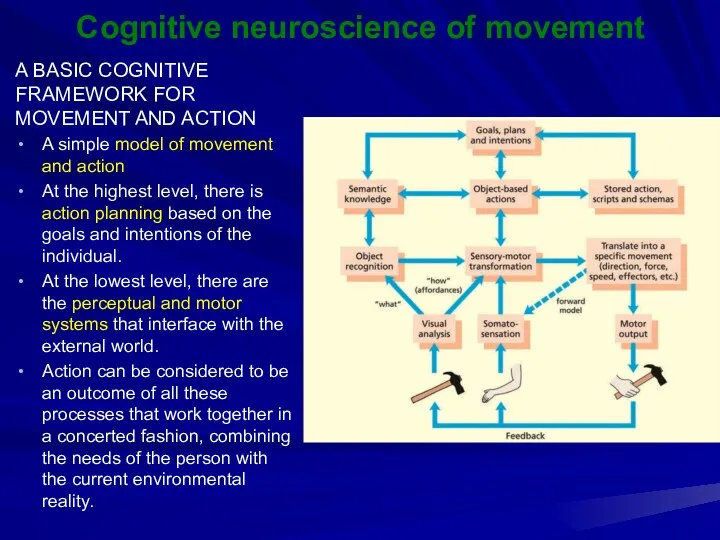 Cognitive neuroscience of movement
Cognitive neuroscience of movement Кора больших полушарий
Кора больших полушарий Размножение - воспроизведение себе подобных, обеспечивающее непрерывность и преемственность жизни
Размножение - воспроизведение себе подобных, обеспечивающее непрерывность и преемственность жизни Вирустардың генетикалық аппаратының ерекшеліктері
Вирустардың генетикалық аппаратының ерекшеліктері Дикие животные Крыма
Дикие животные Крыма Потоки вещества и энергии, динамика экосистем
Потоки вещества и энергии, динамика экосистем Перелётные птицы России
Перелётные птицы России Кабинет биологии, фото
Кабинет биологии, фото Жасуша туралы мәлімет
Жасуша туралы мәлімет Класс Паукообразные
Класс Паукообразные Вирусы – неклеточные формы жизни
Вирусы – неклеточные формы жизни Птицы Рязанской области. Знакомство с уникальными видами птиц
Птицы Рязанской области. Знакомство с уникальными видами птиц Голонасінні рослини
Голонасінні рослини Глаза – органы зрения
Глаза – органы зрения Эволюция приматов
Эволюция приматов Пчелы
Пчелы Беловежская пуща
Беловежская пуща Стебель, его значение и строение. Многообразие стеблей
Стебель, его значение и строение. Многообразие стеблей Человек – предмет изучения анатомии и физиологии человека
Человек – предмет изучения анатомии и физиологии человека Гуморальная регуляция
Гуморальная регуляция презентация для 7 класса по теме: Хрящевые рыбы
презентация для 7 класса по теме: Хрящевые рыбы Влияние диапаузы на развитие колоний муравьев в домашних условиях
Влияние диапаузы на развитие колоний муравьев в домашних условиях