Содержание
- 2. Существуют две формы депонированного энергетического материала – гликоген и жиры, которые различаются по очередности мобилизации. При
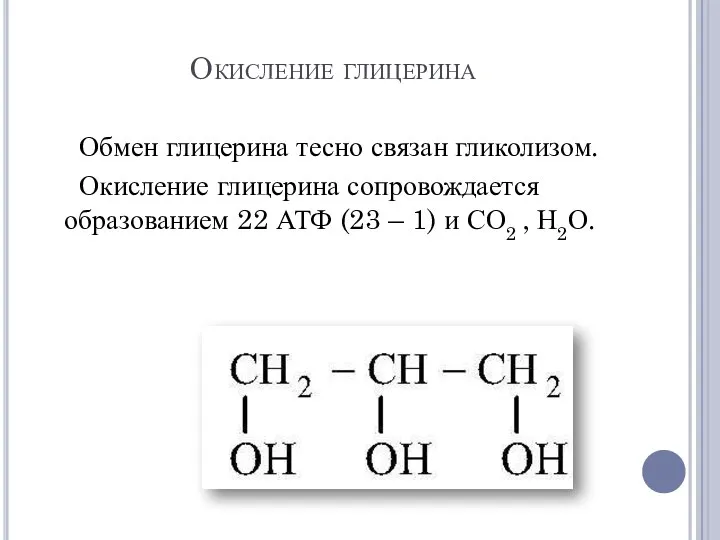
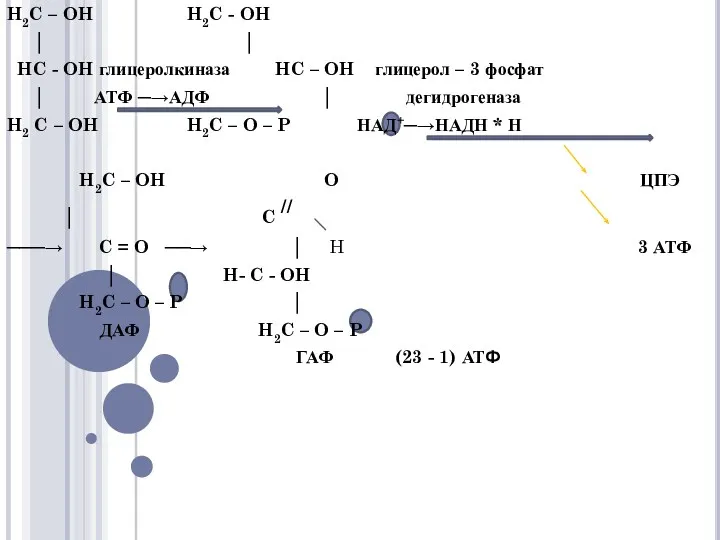
- 3. Окисление глицерина Обмен глицерина тесно связан гликолизом. Окисление глицерина сопровождается образованием 22 АТФ (23 – 1)
- 4. H2C – OH H2C - OH │ │ HC - OH глицеролкиназа HC – OH глицерол
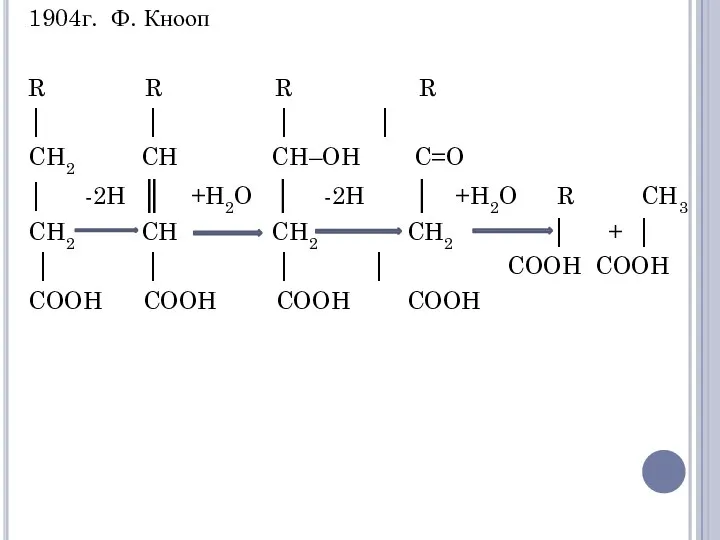
- 5. Окисление жирных кислот (β-окисление) В 1904 г. Ф. Кнооп высказал предположение, что окисление молекулы жирной кислоты
- 6. 1904г. Ф. Кнооп R R R R │ │ │ │ CH2 CH CH–OH C=O │
- 7. В 1948 – 1949 г. Кеннеди и Ленинджер установили что: Окисление жирных кислот происходит в митохондриях;
- 8. Регуляция окисления и синтеза жирных кислот в печени В печени окисление и синтез жирных кислот идут
- 9. По мере исчерпания резервов углеводного обмена включается липидный обмен, т.е.печень начинает использовать жиры в качестве источника
- 10. Современные представления об окислении жирных кислот При β-окислении жирных кислот 2 атома углерода одновременно отщепляются от
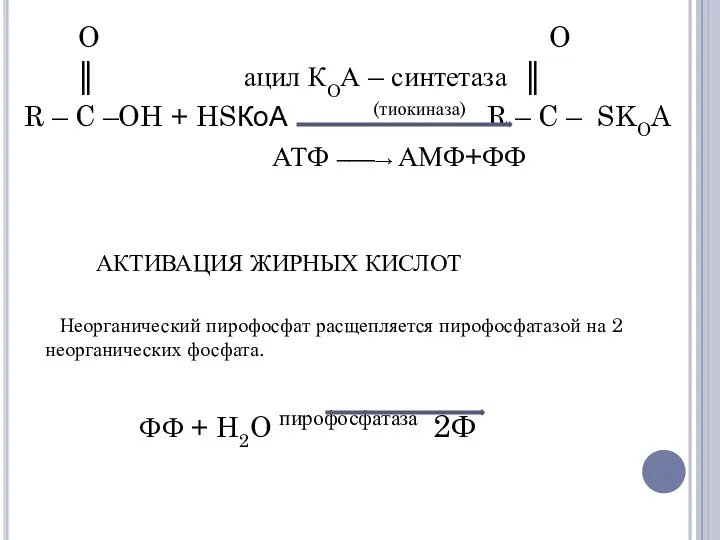
- 11. Три этапа окисления: Активация; β-окисление; Цикл трикарбоновых кислот. I этап – Активация – происходит в цитоплазме.
- 12. O O ║ ацил КОА – синтетаза ║ R – C –OH + HSКоА (тиокиназа) R
- 13. Роль карнитина в окислении жирных кислот Карнитин (γ-триметиламино-β-гидроксибутират). Особенно много в мышцах. Образуется из лизина и
- 14. На внутренней стороне мембраны находится фермент — карнитинпальмитоил-трансфераза II, который катализирует обратную реакцию с образованием свободных
- 15. После проникновения ацильного фрагмента через мембрану митохондрий происходит отщепление двух атомов Н в положении α (2)
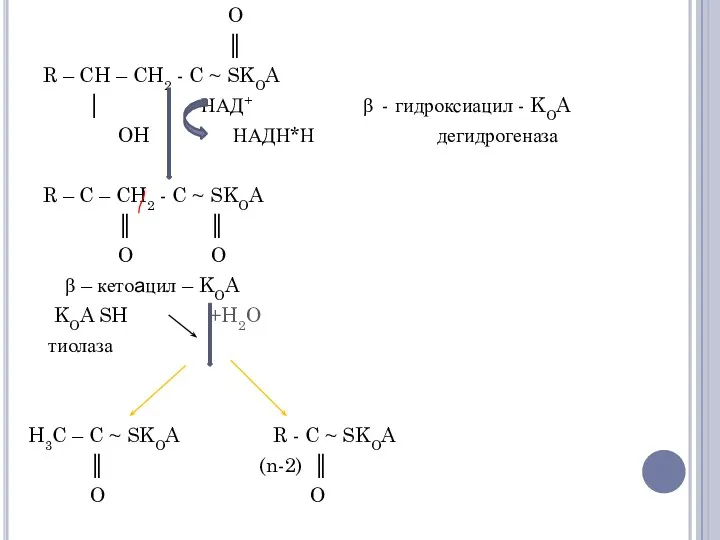
- 16. Эти тиолитические расщепления требуют еще одной молекулы КоА. Образующийся укороченный ацил-КоА вновь вступает в цикл β-окисления.
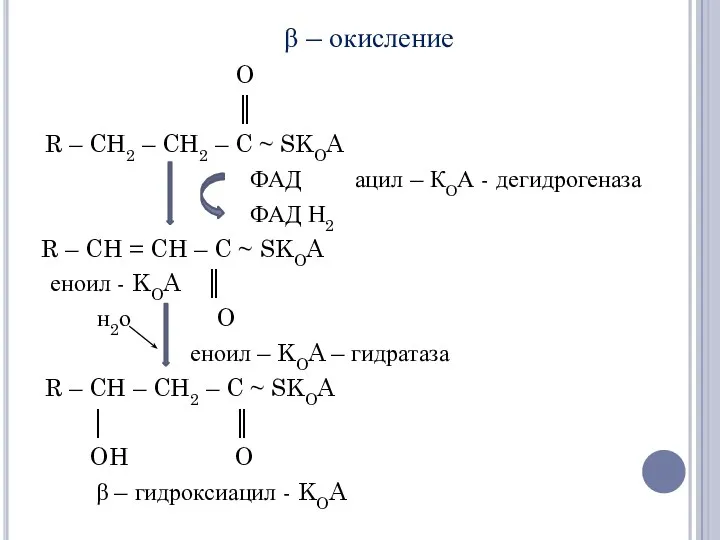
- 17. β – окисление O ║ R – CH2 – CH2 – C ~ SKOA ФАД ацил
- 18. O ║ R – CH – CH2 - C ~ SKOA │ НАД+ β - гидроксиацил
- 19. Количество энергии, получаемое при окислении пальмитиновой кислоты (С - 16) Если ж.к. содержит n С, то
- 20. Количество энергии получаемое при окислении ТАГ (на примере трипальмитата). 3 молекулы пальмитиновой кислоты дают 130 *
- 21. Особенности окисления жирных кислот с нечетным числом углеродных атомов В организме преобладают жирные кислоты с четным
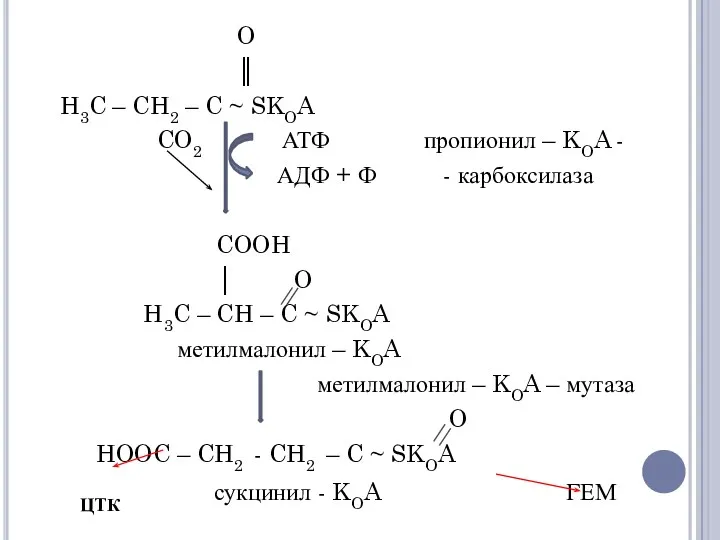
- 22. Окисление пропионил-КоА Вначале происходит карбоксилирование с образованием метил-малонил-КоА. Фермент называется пропионил-КоА-карбоксилаза, в качестве кофермента содержит биотин.
- 23. O ║ H3C – CH2 – C ~ SKOA CO2 АТФ пропионил – KOA - АДФ
- 24. Патология: при недостатке витамина В12 метилмалоновая кислота накапливается в организме и выводится с мочой. Определение ее
- 25. Особенности окисления ненасыщенных жирных кислот Определятся: 1. положением; 2. числом двойных связей. До места двойных связей
- 26. ∆3,4 – цис - ∆2,3 – транс – еноил - KOA – изомераза
- 27. Скорость окисления ненасыщенных жирных кислот выше, чем насыщенных. Например: скорость окисления арахидоновой кислоты в 200 раз
- 28. Β-окисление жирных кислот в пероксисомах Жирные кислоты находятся в модифицированном виде. Обеспечивает окисление ж.к. с очень
- 29. α- и ω- окисление жирных кислот α-окисление обнаружено в тканях мозга. Заключается в последовательном отщеплении одноуглеродных
- 30. ω-окисление жирных кислот в норме весьма незначительно. Этот тип окисления катализируется гидролазами при угнетении цитохрома Р-450.
- 31. Клинические аспекты Увеличение скорости окисления жирных кислот, особенно при недостатке углеводов происходит при: Приеме богатой жирами
- 32. Снижение скорости окисления жирных кислот наблюдается при: 1.Недостатке карнитина. Наблюдается у новорожденных, чаще всего недоношенных детей.
- 33. 2. Снижение активности карнитин-пальмитоил-трансферазы. В печени приводит к гипогликемии и понижению содержания кетоновых тел в плазме
- 34. 4. Ямайская рвотная болезнь. Возникает у людей после употребления в пищу незрелых плодов АКИ, которые содержат
- 35. Синдром Цельвегера (цереброгепаторенальный синдром) Является редким наследственным заболеванием, при котором во всех тканях отсутствуют пероксисомы. У
- 36. Болезнь Рефсума Редкое неврологическое заболевание связано с врожденным нарушением системы α- окисления, что приводит к накоплению
- 38. Скачать презентацию



























 Болезни мелких животных
Болезни мелких животных История развития генетики
История развития генетики Відозміна листка
Відозміна листка Отделы головного мозга
Отделы головного мозга Красный волк
Красный волк Интерактивный тест Свойства воздуха
Интерактивный тест Свойства воздуха Позвоночные. Все классы животинок, имеющих внутренний скелет
Позвоночные. Все классы животинок, имеющих внутренний скелет Мікроклімат приміщень
Мікроклімат приміщень Cellular biophysics
Cellular biophysics В гостях у красной книги
В гостях у красной книги Люминесцентная (флуоресцентная) микроскопия
Люминесцентная (флуоресцентная) микроскопия Насекомые
Насекомые Биология развития
Биология развития Органы выделения
Органы выделения презентация по теме Грибы-паразиты
презентация по теме Грибы-паразиты Как звери ухаживают за детенышами
Как звери ухаживают за детенышами Разработка урока с презентацией Способы передвижения животных. Полости тела
Разработка урока с презентацией Способы передвижения животных. Полости тела Надцарство прокариоты или доядерные организмы. Бактерии и цианобионты
Надцарство прокариоты или доядерные организмы. Бактерии и цианобионты Исследовательский проект Удивительные свойства дерева
Исследовательский проект Удивительные свойства дерева Многообразие растений. Высшие споровые растения. Часть 2
Многообразие растений. Высшие споровые растения. Часть 2 Экосистемы морей и океанов
Экосистемы морей и океанов Нуклеин қышқылдары
Нуклеин қышқылдары Вода – важный фактор окружающей среды. Значение, состав, свойства воды
Вода – важный фактор окружающей среды. Значение, состав, свойства воды Общий обзор пищеварительной системы
Общий обзор пищеварительной системы Генетика. Методи генетики
Генетика. Методи генетики Царство растения. Водоросли
Царство растения. Водоросли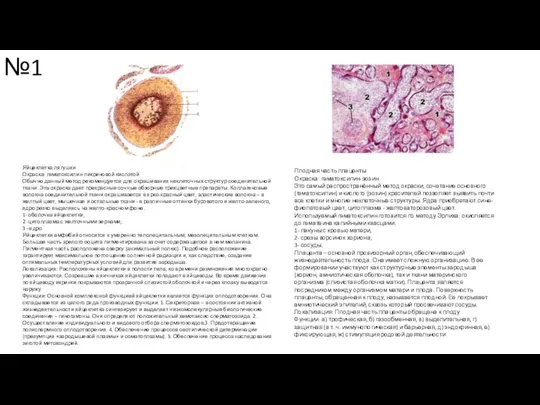 Яйцеклетка лягушки
Яйцеклетка лягушки Класс Млекопитающие
Класс Млекопитающие